
- •Лекция 11.
- •Часть 1. Гальванические элементы
- •Условная схема гальванического элемента
- •Аккумуляторы
- •Часть 2. Коррозия металлов. Способы защиты металлов от коррозии
- •Механизм электрохимической коррозии
- •Электрохимическая коррозия с водородной деполяризацией
- •Электрохимическая коррозия в кислородной деполяризацией
- •Способы защиты металлов от коррозии
- •4Электрохимическая защита.
- •Контрольная работа №11 (3 балла)
- •Лекция 13. Качественный анализ.
- •Типы реакций, применяемые в аналитической химии
- •Качественный анализ
- •Условия проведения реакций
- •Определение и регулирование рН в ходе анализа
- •Способы выполнения реакций
- •Реакции “сухим” способом
- •Реакции “мокрым” способом
- •Микрокристаллоскопический метод анализа
- •Методы определения качественного состава раствора
- •Дробный метод анализа.
- •Систематический метод анализа
- •Аналитические классификации ионов
- •Фильтрование
- •Центрифугирование
- •Осаждение ( седиментация)
- •Маскирование
- •5. Хроматографическое разделение
- •Экстракция
- •Электрохимические методы разделения
- •Флотация
- •Разделение и обнаружение газов
- •Реакции обнаружения анионов
- •Качественный анализ минерала (этот материал дополнительный, приведен для ознакомления)
- •Прямые методы анализа
- •Непрямые методы анализа
- •Аппаратура, химическая посуда, материалы
- •Подготовка образца к анализу
- •Выбор растворителя
- •Растворение в воде
- •Кислотное растворение
- •Растворение в разбавленной hCl
- •Растворение в концентрированной hCl
- •Растворение в азотной кислоте и смеси кислот
- •Бескислотное растворение
- •Контроьные задания
- •Задание №1,6,11,16
- •Задание №2,7,12,17
- •Задание №3,8,13,18
- •Задание №4,9,14,19
- •Задание №5,10,15,20
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •9. Применение комплексных соединений
- •Лекция 10. Окислительно-восстановительные реакции (овр)
- •Правила для определения степени окисления атомов:
- •Определение степени окисления атомов в сложных соединениях и ионах
- •Основные окислители и восстановители
- •Метод электронного баланса
- •2. Метод полуреакций или ионно-электронный метод
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций Электродные потенциалы
- •Сущность возникновения электродного потенциала
- •Ряд стандартных электродных потенциалов
- •Информация, заложенная в ряду стандартных электродных потенциалов:
- •Стандартные электродные потенциалы металлов
- •Определение направления протекания овр
- •Лекция № 8 Общие свойства растворов.
- •Основные способы выражения концентрации растворов:
- •Понижение давления насыщенного пара
- •Примеры решения задач
- •Повышение температуры кипения растворов
- •Примеры решения задач
- •Понижение температуры замерзания растворов
- •Осмотическое давление раствора
- •Лекция 9 Растворы электролитов
- •Механизм электролитической диссоциации
- •1. Диссоциация веществ с ионной связью
- •2. Диссоциация соединения с полярной ковалентной связью (полярные молекулы)
- •Количественный критерий процесса диссоциации
- •Слабые электролиты
- •Сильные электролиты
- •Взаимосвязь между кд и . Закон разбавления Оствальда
- •Диссоциация воды. Водородный показатель
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации
- •Реакции ионного обмена (рио)
- •Условия необратимого протекания реакций ионного обмена (рио)
- •Гидролиз солей
- •Произведение растворимости.
- •Лекция № 7 химическая кинетика и химическое равновесие
- •Факторы, влияющие на скорость реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Особенности закона действия масс
- •Зависимость скорости реакции от температуры
- •Ограниченность правила Вант-Гоффа:
- •Катализаторы
- •Химическое равновесие
- •Механизмы химических реакций
- •Лекция 12. Электролиз
- •Электролиз водных растворов солей
- •Особенности катодных процессов в водных растворах
- •Примеры решения задач
- •Электролиз расплавов электролитов
- •Законы Фарадея
- •Практическое применение электролиза
- •Электрохимический ряд напряжений металлов
- •Стандартные электродные потенциалы металлов
- •Перенапряжение
- •Стандартные электродные потенциалы окислительно-восстановительных систем
- •Окислительно-восстановительные потенциалы некоторых систем (инертный электрод – платина)
- •Контрольная работа №12
- •Лекция № 6 основные положения химической термодинамики и основы термохимии
- •Термодинамическая система
- •Процессы
- •Первое начало термодинамики ( I н т/д )
- •Правила знаков в термодинамике
- •Основы термохимии (т/х) Закон Гесса. Термохимические расчеты
- •Второе начало термодинамики (II н т/д)
- •Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
- •Одно из основных уравнений химической термодинамики
- •Термодинамические расчеты
- •Третье начало термодинамики
- •Приложение Примеры решения задач
Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
Как мы показали, изменения S являются критерием направленности процесса в изолированных системах. Однако, на практике чаще всего приходится иметь дело с неизолированными системами. Причем, чаще процессы протекают в условиях Т, Р = const. Вопрос: Какая термодинамическая функция в этом случае может служить критерием направленности процесса и характеризовать его состояние равновесия?
Чтобы ответить на этот вопрос, вернемся к уравнению I и II начала термодинамики, но при этом опять же упростим нашу задачу, высказав ряд предположений. Исходные посылки:
1) Система неизолированная
2) Условие протекания процесса Т = const , Р = const, т.о. изобарно-изотермические условия.
3) Система совершает только механическую работу (работу расширения) Амех = Р ∆V
T ∆S ≥ ∆U + AМЕХ
T ∆S ≥ ∆U + Р ∆V
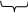
= ∆Н
Для самопроизвольных процессов в условиях Т = const и Р = const
T ∆S ≥ ∆Н
∆Н - T ∆S ≤ 0
Н2 – Н1 – Т(S2 – S1) ≤ 0
Н2 – Н1 – ТS2 –TS1 ≤ 0
(Н2 - ТS2 ) + ( Н1 – TS1 ) ≤ 0
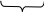
G2 G1
Выведем новую функцию:
G = Н – TS
G – свободная энергия Гиббса (или изобарно-изотермический потенциал)
G2 - G1 ≤ 0 , ∆G ≤ 0

∆G ≤ 0
- новый критерий направленности процесса, и критерий равновесия в неизолированной системе
∆G < 0 – условие возможности самопроизвольного протекания процесса.
(т.е. самопроизвольно протекают процессы, которые сопровождаются уменьшением свободной энергии Гиббса).
∆G = 0 – система находится в состоянии равновесия.
∆G = 0 , ∆G = G2 = G1 = 0 , т.е. G2 = G1 = G min (т.е. в состоянии равновесия G1 = G min ).
∆G > 0 - невозможен самопроизвольный процесс.
Состояние термодинамического равновесия – это такое состояние, которое принимает система после окончания в ней всех самопроизвольных процессов и которое длительно сохраняется во времени при отсутствии вмешательства извне.
∆G = ∆Н - T ∆S
Одно из основных уравнений химической термодинамики
Проанализируем это уравнение для состояния равновесия более подробно:
∆G зависит от двух слагаемых, которые можно рассматривать как два фактора.
1) Энтальпийный фактор (∆Н) – отражает стремление частиц к объединению за счет образования более прочных связей, что приводит к уменьшению Н, то есть ∆Н < 0.
2) Энтропийный фактор (T ∆S) – отражает стремление частиц к разъединению, к беспорядку, что приводит к увеличению S, то есть ∆S > 0 и T ∆S > 0 .
Соотношение двух этих факторов определяет значение ∆G, а следовательно, возможность процесса.
Характер изменения ∆G позволяет судить о принципиальной возможности процесса. Соотношение ∆Н и T ∆S определяет знак ∆G, а следовательно – возможность процесса:
1) при ∆Н < 0, T ∆S > 0 , следовательно, ∆G < 0 ,
2) при других сочетаниях характера изменения ∆Н и T ∆S , возможность процесса определяет либо энтропийный, либо энтальпийный факторы.
а) ∆Н < 0 (экзотермическая реакция), если / ∆Н / > / T ∆S / , то
∆G < 0 – возможность реакции определяется энтальпийным фактором.
б) ∆Н > 0 (эндотермическая реакция), если / ∆Н / < / T ∆S / , то
∆G < 0 – возможность реакции определяется энтропийным фактором.
