
- •Лекция 11.
- •Часть 1. Гальванические элементы
- •Условная схема гальванического элемента
- •Аккумуляторы
- •Часть 2. Коррозия металлов. Способы защиты металлов от коррозии
- •Механизм электрохимической коррозии
- •Электрохимическая коррозия с водородной деполяризацией
- •Электрохимическая коррозия в кислородной деполяризацией
- •Способы защиты металлов от коррозии
- •4Электрохимическая защита.
- •Контрольная работа №11 (3 балла)
- •Лекция 13. Качественный анализ.
- •Типы реакций, применяемые в аналитической химии
- •Качественный анализ
- •Условия проведения реакций
- •Определение и регулирование рН в ходе анализа
- •Способы выполнения реакций
- •Реакции “сухим” способом
- •Реакции “мокрым” способом
- •Микрокристаллоскопический метод анализа
- •Методы определения качественного состава раствора
- •Дробный метод анализа.
- •Систематический метод анализа
- •Аналитические классификации ионов
- •Фильтрование
- •Центрифугирование
- •Осаждение ( седиментация)
- •Маскирование
- •5. Хроматографическое разделение
- •Экстракция
- •Электрохимические методы разделения
- •Флотация
- •Разделение и обнаружение газов
- •Реакции обнаружения анионов
- •Качественный анализ минерала (этот материал дополнительный, приведен для ознакомления)
- •Прямые методы анализа
- •Непрямые методы анализа
- •Аппаратура, химическая посуда, материалы
- •Подготовка образца к анализу
- •Выбор растворителя
- •Растворение в воде
- •Кислотное растворение
- •Растворение в разбавленной hCl
- •Растворение в концентрированной hCl
- •Растворение в азотной кислоте и смеси кислот
- •Бескислотное растворение
- •Контроьные задания
- •Задание №1,6,11,16
- •Задание №2,7,12,17
- •Задание №3,8,13,18
- •Задание №4,9,14,19
- •Задание №5,10,15,20
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •9. Применение комплексных соединений
- •Лекция 10. Окислительно-восстановительные реакции (овр)
- •Правила для определения степени окисления атомов:
- •Определение степени окисления атомов в сложных соединениях и ионах
- •Основные окислители и восстановители
- •Метод электронного баланса
- •2. Метод полуреакций или ионно-электронный метод
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций Электродные потенциалы
- •Сущность возникновения электродного потенциала
- •Ряд стандартных электродных потенциалов
- •Информация, заложенная в ряду стандартных электродных потенциалов:
- •Стандартные электродные потенциалы металлов
- •Определение направления протекания овр
- •Лекция № 8 Общие свойства растворов.
- •Основные способы выражения концентрации растворов:
- •Понижение давления насыщенного пара
- •Примеры решения задач
- •Повышение температуры кипения растворов
- •Примеры решения задач
- •Понижение температуры замерзания растворов
- •Осмотическое давление раствора
- •Лекция 9 Растворы электролитов
- •Механизм электролитической диссоциации
- •1. Диссоциация веществ с ионной связью
- •2. Диссоциация соединения с полярной ковалентной связью (полярные молекулы)
- •Количественный критерий процесса диссоциации
- •Слабые электролиты
- •Сильные электролиты
- •Взаимосвязь между кд и . Закон разбавления Оствальда
- •Диссоциация воды. Водородный показатель
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации
- •Реакции ионного обмена (рио)
- •Условия необратимого протекания реакций ионного обмена (рио)
- •Гидролиз солей
- •Произведение растворимости.
- •Лекция № 7 химическая кинетика и химическое равновесие
- •Факторы, влияющие на скорость реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Особенности закона действия масс
- •Зависимость скорости реакции от температуры
- •Ограниченность правила Вант-Гоффа:
- •Катализаторы
- •Химическое равновесие
- •Механизмы химических реакций
- •Лекция 12. Электролиз
- •Электролиз водных растворов солей
- •Особенности катодных процессов в водных растворах
- •Примеры решения задач
- •Электролиз расплавов электролитов
- •Законы Фарадея
- •Практическое применение электролиза
- •Электрохимический ряд напряжений металлов
- •Стандартные электродные потенциалы металлов
- •Перенапряжение
- •Стандартные электродные потенциалы окислительно-восстановительных систем
- •Окислительно-восстановительные потенциалы некоторых систем (инертный электрод – платина)
- •Контрольная работа №12
- •Лекция № 6 основные положения химической термодинамики и основы термохимии
- •Термодинамическая система
- •Процессы
- •Первое начало термодинамики ( I н т/д )
- •Правила знаков в термодинамике
- •Основы термохимии (т/х) Закон Гесса. Термохимические расчеты
- •Второе начало термодинамики (II н т/д)
- •Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
- •Одно из основных уравнений химической термодинамики
- •Термодинамические расчеты
- •Третье начало термодинамики
- •Приложение Примеры решения задач
Лекция 13. Качественный анализ.
Аналитическая химия - это наука о принципах, способах и методах определения химического состава и структуры химических соединений и материалов.
Под химическим составом веществ понимается состав элементный (элементарный), молекулярный, фазовый, изотопный. Определение отдельных элементов в анализируемом веществе называют элементным анализом; определение функциональных групп - функциональным анализом; определение молекулярной массы - молекулярным анализом.
Аналитические методы часто дают возможность узнать, в какой форме данный компонент присутствует в веществе, какая степень окисления элемента. Например. Элемент хром входит в состав следующих соединений K2CrO4, CrCl3. В хромате калия K2CrO4 хром имеет степень окисления шесть, а в хлориде хрома CrCl3 хром имеет степень окисления три.
Практическое значение аналитической химии разнообразно и велико. Аналитическая химия способствует развитию естественных наук: геохимии, геологии, минералогии, агрохимии, металлургии, химической технологии, медицины и др. Аналитические определения необходимы при выполнении научной работы по химии, геохимии, геологии и др. Большое значение имеют аналитическая химия и химический анализ в производстве для предупреждения брака, обнаружения нежелательных примесей в полупродуктах и готовой продукции. По результатам анализа судят о качестве готового продукта.
Химический анализ нужен геологам при оценке месторождений полезных ископаемых. На основании данных химического анализа предлагаются рекомендации о целесообразности разработки месторождения.
В аналитической химии существует большое число методов, разработанных с учетом специфических особенностей объектов исследования. Каждый метод имеет свои преимущества и недостатки. Для студентов - геологов, изучающих аналитическую химию, отобраны методы, отличающиеся простотой оборудования, надежностью, несложностью и достаточной быстротой выполнения.
Аналитическая химия представлена классическими и современными методами анализа, которые дают надежные и точные результаты.
Методы и реакции, при помощи которых устанавливают, какие ионы (элементы) входят в состав анализируемого вещества, называют качественным анализом.
Методы и реакции, при помощи которых определяют количества ионов (элементов) в анализируемом образце, называют количественным анализом.
Типы реакций, применяемые в аналитической химии
Не все химические реакции могут быть использованы в качественном анализе. Аналитическими реакциями могут быть только такие реакции, которые сопровождаются каким - либо внешним эффектом, проходят быстро и полно. Для обнаружения какого-либо компонента обычно используют так называемый аналитический сигнал. Аналитический сигнал – это видимые изменения в самом объекте исследования (образование осадка, изменение окраски и т.д.) или изменение параметров измерительных приборов (отклонение стрелки прибора, изменение цифрового отсчета, появление линии в спектре и пр.).
Реакции, которые сопровождаются внешним аналитическим эффектом :
Образование или растворение осадка
Например.
AgNO3
+ HCl
 AgCl
AgCl
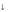 + HNO3 ( реакция
обмена )
+ HNO3 ( реакция
обмена )
AgCl + 2 NH3 H2O [Ag(NH3)2]Cl + 2 H2O ( реакция комплексообразования )
белый осадок бесцветный раствор
Изменение цвета раствора или образование окрашенного соединения
Например. Реакция окисления - восстановления
2 Mn ( NO3 )2 + 5 NaBiO3 + 4 HNO3 = 2 NaMnO4 + 5 (BiO) NO3 + 3 NaNO3 + 2 H2O
бесцветный кристаллы розовый раствор
раствор
восстановитель окислитель
Выделение газа
Например.
Na2CO3
+ 2 HCl = 2 NaCl
+ H2CO3
; H2CO3

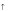 + H2O
+ H2O
