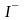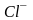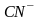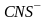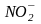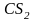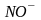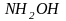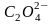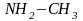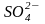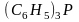- •Лекция 11.
- •Часть 1. Гальванические элементы
- •Условная схема гальванического элемента
- •Аккумуляторы
- •Часть 2. Коррозия металлов. Способы защиты металлов от коррозии
- •Механизм электрохимической коррозии
- •Электрохимическая коррозия с водородной деполяризацией
- •Электрохимическая коррозия в кислородной деполяризацией
- •Способы защиты металлов от коррозии
- •4Электрохимическая защита.
- •Контрольная работа №11 (3 балла)
- •Лекция 13. Качественный анализ.
- •Типы реакций, применяемые в аналитической химии
- •Качественный анализ
- •Условия проведения реакций
- •Определение и регулирование рН в ходе анализа
- •Способы выполнения реакций
- •Реакции “сухим” способом
- •Реакции “мокрым” способом
- •Микрокристаллоскопический метод анализа
- •Методы определения качественного состава раствора
- •Дробный метод анализа.
- •Систематический метод анализа
- •Аналитические классификации ионов
- •Фильтрование
- •Центрифугирование
- •Осаждение ( седиментация)
- •Маскирование
- •5. Хроматографическое разделение
- •Экстракция
- •Электрохимические методы разделения
- •Флотация
- •Разделение и обнаружение газов
- •Реакции обнаружения анионов
- •Качественный анализ минерала (этот материал дополнительный, приведен для ознакомления)
- •Прямые методы анализа
- •Непрямые методы анализа
- •Аппаратура, химическая посуда, материалы
- •Подготовка образца к анализу
- •Выбор растворителя
- •Растворение в воде
- •Кислотное растворение
- •Растворение в разбавленной hCl
- •Растворение в концентрированной hCl
- •Растворение в азотной кислоте и смеси кислот
- •Бескислотное растворение
- •Контроьные задания
- •Задание №1,6,11,16
- •Задание №2,7,12,17
- •Задание №3,8,13,18
- •Задание №4,9,14,19
- •Задание №5,10,15,20
- •Лекция 14.Комплексные соединения
- •1.Понятие о комплексном соединении
- •2.Структура комплексных соединений
- •3.Номенклатура комплексных соединений
- •4.Классификация комплексных соединений
- •4.1.Комплексные соединения, содержащие
- •4.2.Комплексные соединения, содержащие ионные лиганды
- •4.3. Циклические комплексные соединения
- •4.4. Многоядерные комплексные соединения
- •5.Изомерия комплексных соединений
- •6.Равновесия в растворах комплексных соединений
- •7.Квантово-механические методы трактовки химической связи в комплексных соединениях
- •7.1. Метод валентных связей
- •7.2. Теория кристаллического поля
- •9. Применение комплексных соединений
- •Лекция 10. Окислительно-восстановительные реакции (овр)
- •Правила для определения степени окисления атомов:
- •Определение степени окисления атомов в сложных соединениях и ионах
- •Основные окислители и восстановители
- •Метод электронного баланса
- •2. Метод полуреакций или ионно-электронный метод
- •Типы окислительно-восстановительных реакций
- •Направление окислительно-восстановительных реакций Электродные потенциалы
- •Сущность возникновения электродного потенциала
- •Ряд стандартных электродных потенциалов
- •Информация, заложенная в ряду стандартных электродных потенциалов:
- •Стандартные электродные потенциалы металлов
- •Определение направления протекания овр
- •Лекция № 8 Общие свойства растворов.
- •Основные способы выражения концентрации растворов:
- •Понижение давления насыщенного пара
- •Примеры решения задач
- •Повышение температуры кипения растворов
- •Примеры решения задач
- •Понижение температуры замерзания растворов
- •Осмотическое давление раствора
- •Лекция 9 Растворы электролитов
- •Механизм электролитической диссоциации
- •1. Диссоциация веществ с ионной связью
- •2. Диссоциация соединения с полярной ковалентной связью (полярные молекулы)
- •Количественный критерий процесса диссоциации
- •Слабые электролиты
- •Сильные электролиты
- •Взаимосвязь между кд и . Закон разбавления Оствальда
- •Диссоциация воды. Водородный показатель
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации
- •Реакции ионного обмена (рио)
- •Условия необратимого протекания реакций ионного обмена (рио)
- •Гидролиз солей
- •Произведение растворимости.
- •Лекция № 7 химическая кинетика и химическое равновесие
- •Факторы, влияющие на скорость реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ
- •Особенности закона действия масс
- •Зависимость скорости реакции от температуры
- •Ограниченность правила Вант-Гоффа:
- •Катализаторы
- •Химическое равновесие
- •Механизмы химических реакций
- •Лекция 12. Электролиз
- •Электролиз водных растворов солей
- •Особенности катодных процессов в водных растворах
- •Примеры решения задач
- •Электролиз расплавов электролитов
- •Законы Фарадея
- •Практическое применение электролиза
- •Электрохимический ряд напряжений металлов
- •Стандартные электродные потенциалы металлов
- •Перенапряжение
- •Стандартные электродные потенциалы окислительно-восстановительных систем
- •Окислительно-восстановительные потенциалы некоторых систем (инертный электрод – платина)
- •Контрольная работа №12
- •Лекция № 6 основные положения химической термодинамики и основы термохимии
- •Термодинамическая система
- •Процессы
- •Первое начало термодинамики ( I н т/д )
- •Правила знаков в термодинамике
- •Основы термохимии (т/х) Закон Гесса. Термохимические расчеты
- •Второе начало термодинамики (II н т/д)
- •Свободная энергия Гиббса. Критерий направленности процесса в неизолированных системах
- •Одно из основных уравнений химической термодинамики
- •Термодинамические расчеты
- •Третье начало термодинамики
- •Приложение Примеры решения задач
3.Номенклатура комплексных соединений
Основы номенклатуры комплексных соединений были разработаны А.Вернером. Общепринятая сегодня номенклатура основана на рекомендациях Международного союза по теоретической и прикладной химии (ИЮПАК) и лишь незначительно отличается от номенклатуры А.Вернера.
Первым, независимо от заряда координационной сферы, в именительном падеже называют анион, а затем в родительном падеже - катион, как это делается в названиях обычных солей.
В названии координационной сферы (вне зависимости от того, заряжена она или нет) перечисляются все ее составные части справа налево, при этом сначала называют число лигандов, затем сами лиганды и, наконец, комплексообразователь с указанием его степени окисления.
Для обозначения числа лигандов используют греческие численные: 1 - моно, 2 - ди, 3 - три, 4 - тетра, 5 - пента, 6 - гекса, 7 - гепта (приставка моно обычно опускается).
Первыми
среди лигандов называют отрицательно
заряженные, затем нейтральные и в конце
- положительно заряженные. Отрицательно
заряженные лиганды называют добавляя
к их латинскому названию окончание - О.
Например:
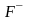 - фторо;
- фторо;
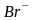 - бромо и т.д. Нейтральные лиганды
называют, как и соответствующие молекулы.
Исключения:
- бромо и т.д. Нейтральные лиганды
называют, как и соответствующие молекулы.
Исключения:
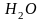 - аква,
- аква,
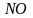 - нитрозил,
- нитрозил,
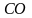 - карбонил,
- карбонил,
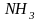 - аммин. Положительные лиганды называют
путем добавления к их названию окончания
- ий. Например:
- аммин. Положительные лиганды называют
путем добавления к их названию окончания
- ий. Например:
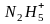 - гидрозиний. Название некоторых
распространенных лигандов приведены
в таблице 5.1.
- гидрозиний. Название некоторых
распространенных лигандов приведены
в таблице 5.1.
Распространенные лиганды и их названия
в координационной сфере
Лиганды |
Название |
Лиганды |
Название |
|
иодо |
CO |
Карбонил |
|
хлоро |
NO |
Нитрозил |
|
циано |
|
Аква |
|
тиоцианато |
|
Аммин |
|
гидроксо |
|
Гидразин |
|
нитро |
|
Сероуглерод |
|
нитрозо |
|
Гидроксиламин |
|
оксалато |
|
Метиламин |
|
сульфато |
|
Трифенилфосфин |
|
перхлорато |
|
Пиридин |
Последним называется комплексообразователь.
Если комплексообразователь входит в состав катиона, то его называют по-русски в родительном падеже и в скобках указывают римскими цифрами степень его окисления.
Например:
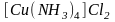 - хлорид тетраамминмеди
(II);
- хлорид тетраамминмеди
(II);
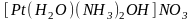 - нитрат
гидроксодиамминакваплатины (II);
- нитрат
гидроксодиамминакваплатины (II);
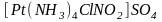 - сульфат
нитрохлоротетраамминплатины (IV).
- сульфат
нитрохлоротетраамминплатины (IV).
Если координационная сфера имеет нулевой заряд, комплексообразователь называют по-русски, но в именительном падеже. При этом степень окисления комплексообразователя можно не указывать. Например:
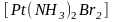 - дибромодиамминплатина;
- дибромодиамминплатина;
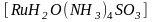 - сульфитотетраамминакварутений;
- сульфитотетраамминакварутений;
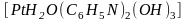 -
тригидроксодипиридинаква-
-
тригидроксодипиридинаква-
платина.
Если комплексообразователь входит в состав аниона, то его называют по-латински, при этом последние буквы - ум
( иум ) в латинском названии заменяют на буквы - ат. Затем в скобках римскими цифрами указывают степень окисления комплексообразователя. Например:
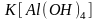 - тетрагидроксоалюминат (III)
калия;
- тетрагидроксоалюминат (III)
калия;
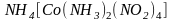 - тетранитродиамминкобальтат (III)
аммония;
- тетранитродиамминкобальтат (III)
аммония;
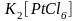 - гексахлороплатинат (IV)
калия.
- гексахлороплатинат (IV)
калия.
Таким образом, формулы комплексных соединений читают строго справа налево, соблюдая указанный в формуле порядок распоряжения лигандов. Запись формулы комплексного соединения осуществляется в порядке обратном рассмотренному выше.