
- •Основные обозначения
- •Введение
- •СПЕКТРАЛЬНЫЕ (ОПТИЧЕСКИЕ) МЕТОДЫ АНАЛИЗА
- •Основные характеристики электромагнитного излучения
- •Спектр электромагнитных колебаний
- •Глава 1. Абсорбционная спектроскопия
- •1.1. Законы поглощения света
- •1.2.2. Спектры поглощения
- •1.2.3. Устройство приборов
- •1.2.4. Практическое применение
- •1. Определение фенолов.
- •2. Определение аминов.
- •3. Определение кетонов.
- •1.2.5. Практические работы
- •Работа 1. Определение хрома дифенилкарбазидным методом
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •1.3. Инфракрасная (колебательная) спектроскопия
- •1.3.1. Элементарная теория колебательных спектров
- •1.3.2. Спектры поглощения
- •Количественный анализ по инфракрасным спектрам.
- •1.3.4. Устройство приборов
- •1.3.5. Практические работы
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 2. Эмиссионная спектроскопия
- •2.3. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- •Глава 3. Кондуктометрия
- •3.1. Электропроводность растворов электролитов
- •3.1.1. Удельная электропроводность
- •3.1.2. Эквивалентная электропроводность
- •3.2. Электропроводность природных вод
- •3.3. Кондуктометрическое титрование
- •Титрование сильной кислоты сильным основанием
- •Титрование слабой кислоты сильным основанием
- •3.4. Практические работы
- •Кондуктометр ОК 102/1
- •Порядок работы на приборе
- •Выполнение работы
- •Работа 2. Определение удельной электропроводности воды
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 4. Потенциометрия
- •4.1. Электродный потенциал
- •4.2. Электроды сравнения
- •4.3. Диффузионный потенциал
- •4.4. Прямая потенциометрия
- •4.4.2. Ионоселективные электроды
- •4.5. Потенциометрическое титрование
- •4.7. Практические работы
- •Порядок работы
- •Ход работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 5. Вольтамперометрия
- •5.1. Кривая ток-потенциал
- •5.2. Полярографический фон
- •5.3. Диффузионный ток
- •5.4. Количественный полярографический анализ
- •5.5. Качественный полярографический анализ
- •5.6. Полярографическая установка
- •5.7. Хроноамперометрия с линейной разверткой потенциала
- •5.8. Инверсионная вольтамперометрия
- •5.9. Практическое применение
- •5.10. Практические работы
- •Работа 1. Обнаружение ионов Cu2+, Cd2+, Zn2+, Mn2+
- •Выполнение работы
- •Работа 2. Обнаружение ионов Pb2+ и Tl+
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 6. Электрофорез
- •6.1. Общие принципы электрофореза
- •1. Форма и величина белковой молекулы.
- •2. Электрическое поле.
- •3. Характер буфера и его ионная сила.
- •4. Природа носителя.
- •6.2. Электрофорез на бумаге и ацетате целлюлозы
- •6.3. Электрофорез в гелях
- •6.4. Диск-электрофорез
- •6.5. Применение метода диск-электрофореза
- •6.6. Практические работы
- •Выполнение работы
- •Проведение электрофореза
- •Обнаружение белковых фракций
- •Хранение и реставрация гелей
- •Техника безопасности при работе методом электрофореза
- •Контрольные вопросы
- •Литература
- •6.8. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Выполнение работы
- •Контрольные вопросы
- •Контрольные вопросы
- •Литература
- •ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- •Глава 7. Общие принципы хроматографии
- •7.2. Классификация хроматографических методов
- •7.3. Применение методов хроматографии
- •Контрольные вопросы
- •Литература
- •Глава 8. Жидкостная хроматография
- •8.1.1. Хроматография на колонке
- •8.1.2. Тонкослойная хроматография (ТСХ)
- •8.1.3. Практические работы
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.2. Жидкостно-жидкостная (распределительная) хроматография
- •8.2.1. Теоретические основы метода
- •8.2.2. Хроматография на бумаге
- •8.2.3. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.3. Ионообменная хроматография
- •8.3.1. Теоретические основы метода
- •Контрольные вопросы
- •Литература
- •8.4. Проникающая или эксклюзионная хроматорафия
- •8.4.1. Теоретические основы метода
- •8.4.2. Практические работы
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.5. Высокоэффективная жидкостная хроматография (ВЭЖХ)
- •8.5.1. Теоретические основы метода
- •8.5.2. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.6. Понятие об аффинной или биоспецифической хроматографии
- •Контрольные вопросы
- •Литература
- •Глава 9. Газовая хроматография
- •9.1. Теоретические основы метода
- •9.2. Аппаратурное оформление газовой хроматографии
- •9.3. Качественный и количественный анализ
- •9.4. Применение газовой хроматографии
- •9.5. Практические работы
- •Контрольные вопросы
- •Литература
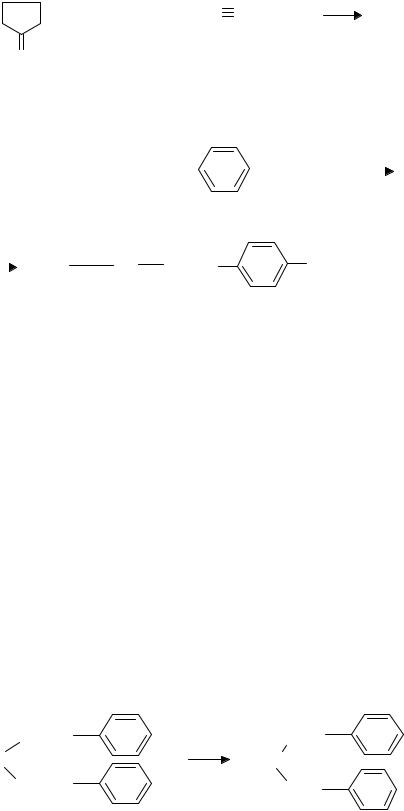
+ [O2N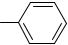
 N+ N ]Cl -
N+ N ]Cl -
O
 O2N
O2N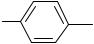 N
N  N
N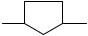 N
N  N
N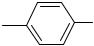 NO2 + HCl
NO2 + HCl
Метилэтилкетон дает моноазокраситель красного цвета.
|
|
O |
+ |
|
|
|
|
|
|
|
+ |
- |
|
|
||||||||||
H3C |
|
|
|
|
|
C2H5 |
|
[O2N |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
N |
|
N]Cl |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
NO2 + HCl |
||||||
|
|
|
|
H5C2 |
|
|
|
|
CH2 |
|
N |
|
|
N |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
Рассмотренный метод применяют для определения кислот, альдегидов, нитросоединений, спиртов и др.
Реагенты находят применение в органической химии, особенно в тех случаях, когда необходимо обнаружить и количественно определить микропримеси веществ; в промышленной санитарии (определение вредных соединений, отравляющих веществ в воздухе), в биологии.
1.2.5. Практические работы
Работа 1. Определение хрома дифенилкарбазидным методом
Принцип определения основан на том, что бихромат калия, имеющий низкий коэффициент ослабления (≈500), окисляет в кислой среде дифенилкарбазид, превращая его в бис-азокраситель с коэффициентом ослабления около 104. Дифенилкарбазид, являющийся реагентом на хром, требуется брать в избытке по отношенияю к бихромату, поскольку необходимо, чтобы во взятой пробе весь бихромат провзаимодействовал с реагентом.
NH-NH |
K2Cr2O7 |
N=N |
O=C |
|
O=C |
NH-NH |
|
N=N |
дифенилкарбазид бис-азокраситель
Азокраситель имеет фиолетово-красную окраску, его максимальное поглощение лежит в зеленой области спектра, что определяет выбор зеленого светофильтра.
26
Выполнение работы
Раствор дифенилкарбазида готовят перед употреблением, растворяя 0,1 г реагента в 15 мл ацетона в мерной колбе на 50 мл и доводят водой до метки.
Для построения калибровочной кривой отбирают из бюретки 1, 2, 3, 4 и 5 мл раствора бихромата калия с концентрацией 6,8 10-5 моль/л в колбочки на 50 мл, добавляют в каждую по 2 мл раствора дифенилкарбазида и по 2 мл серной кислоты с концентрацией 5 моль/л.
Растворы разбавляют дистиллированной водой, доводят до метки, тщательно перемешивают и измеряют оптические плотности.
Для измерения абсорбции вещества кюветы заполняют на 2/3 высоты, соответственно, раствором и растворителем (дистиллированная вода). Кюветы осушают снаружи фильтровальной бумагой и помещают в держатели для кювет. Не следует касаться пальцами стенок кюветы, сквозь которые проходят световые лучи.
Результаты измерения абсорбции растворов заносят в таблицу, где указывают рассчитанную концентрацию бихромата калия в каждой пробе, а затем строят калибровочную кривую. Получают анализируемую пробу в колбочке на 50 мл, добавляют, как прежде, серную кислоту, реагент, доводят колбу водой до метки и измеряют оптическую плотность. Концентрацию анализируемой пробы находят по калибровочной кривой.
Расчет концентрации производят по формуле:
Ск = Сб ½ Vб/Vк ,
где Ск, Сб – молярные концентрации (моль/л) в колбе и бюретке, соответсвенно; Vб – объем расвора, отобранного из бюретки; Vк – объем колбы.
Работа 2. Определение концентрации аминокислот спектрофотометрическим методом
Реактивы и посуда:
1)водный раствор тирозина, С = 2,92 10-4 моль/л,
2)водный раствор триптофана, С = 6,07 10-5 моль/л,
3)кварцевые кюветы (2 шт.),
4)спектрофотометр.
Выполнение работы
Кювету заполняют раствором аминокислоты (в кювету сравнения налить воду). Записывают спектр поглощения аминокислоты в области 200-350 нм и определяют расположение максимума поглощения. Разбавляя исходный раствор аминокислоты соответственно в 2, 4, 6, 8 и 10 раз, измеряют абсорбцию полученных растворов при максимуме поглощения. Строят кривую зависимости абсорбции растворов (при макси-
27
