
- •Основные обозначения
- •Введение
- •СПЕКТРАЛЬНЫЕ (ОПТИЧЕСКИЕ) МЕТОДЫ АНАЛИЗА
- •Основные характеристики электромагнитного излучения
- •Спектр электромагнитных колебаний
- •Глава 1. Абсорбционная спектроскопия
- •1.1. Законы поглощения света
- •1.2.2. Спектры поглощения
- •1.2.3. Устройство приборов
- •1.2.4. Практическое применение
- •1. Определение фенолов.
- •2. Определение аминов.
- •3. Определение кетонов.
- •1.2.5. Практические работы
- •Работа 1. Определение хрома дифенилкарбазидным методом
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •1.3. Инфракрасная (колебательная) спектроскопия
- •1.3.1. Элементарная теория колебательных спектров
- •1.3.2. Спектры поглощения
- •Количественный анализ по инфракрасным спектрам.
- •1.3.4. Устройство приборов
- •1.3.5. Практические работы
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 2. Эмиссионная спектроскопия
- •2.3. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- •Глава 3. Кондуктометрия
- •3.1. Электропроводность растворов электролитов
- •3.1.1. Удельная электропроводность
- •3.1.2. Эквивалентная электропроводность
- •3.2. Электропроводность природных вод
- •3.3. Кондуктометрическое титрование
- •Титрование сильной кислоты сильным основанием
- •Титрование слабой кислоты сильным основанием
- •3.4. Практические работы
- •Кондуктометр ОК 102/1
- •Порядок работы на приборе
- •Выполнение работы
- •Работа 2. Определение удельной электропроводности воды
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 4. Потенциометрия
- •4.1. Электродный потенциал
- •4.2. Электроды сравнения
- •4.3. Диффузионный потенциал
- •4.4. Прямая потенциометрия
- •4.4.2. Ионоселективные электроды
- •4.5. Потенциометрическое титрование
- •4.7. Практические работы
- •Порядок работы
- •Ход работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 5. Вольтамперометрия
- •5.1. Кривая ток-потенциал
- •5.2. Полярографический фон
- •5.3. Диффузионный ток
- •5.4. Количественный полярографический анализ
- •5.5. Качественный полярографический анализ
- •5.6. Полярографическая установка
- •5.7. Хроноамперометрия с линейной разверткой потенциала
- •5.8. Инверсионная вольтамперометрия
- •5.9. Практическое применение
- •5.10. Практические работы
- •Работа 1. Обнаружение ионов Cu2+, Cd2+, Zn2+, Mn2+
- •Выполнение работы
- •Работа 2. Обнаружение ионов Pb2+ и Tl+
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •Глава 6. Электрофорез
- •6.1. Общие принципы электрофореза
- •1. Форма и величина белковой молекулы.
- •2. Электрическое поле.
- •3. Характер буфера и его ионная сила.
- •4. Природа носителя.
- •6.2. Электрофорез на бумаге и ацетате целлюлозы
- •6.3. Электрофорез в гелях
- •6.4. Диск-электрофорез
- •6.5. Применение метода диск-электрофореза
- •6.6. Практические работы
- •Выполнение работы
- •Проведение электрофореза
- •Обнаружение белковых фракций
- •Хранение и реставрация гелей
- •Техника безопасности при работе методом электрофореза
- •Контрольные вопросы
- •Литература
- •6.8. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Выполнение работы
- •Контрольные вопросы
- •Контрольные вопросы
- •Литература
- •ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
- •Глава 7. Общие принципы хроматографии
- •7.2. Классификация хроматографических методов
- •7.3. Применение методов хроматографии
- •Контрольные вопросы
- •Литература
- •Глава 8. Жидкостная хроматография
- •8.1.1. Хроматография на колонке
- •8.1.2. Тонкослойная хроматография (ТСХ)
- •8.1.3. Практические работы
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.2. Жидкостно-жидкостная (распределительная) хроматография
- •8.2.1. Теоретические основы метода
- •8.2.2. Хроматография на бумаге
- •8.2.3. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.3. Ионообменная хроматография
- •8.3.1. Теоретические основы метода
- •Контрольные вопросы
- •Литература
- •8.4. Проникающая или эксклюзионная хроматорафия
- •8.4.1. Теоретические основы метода
- •8.4.2. Практические работы
- •Выполнение работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.5. Высокоэффективная жидкостная хроматография (ВЭЖХ)
- •8.5.1. Теоретические основы метода
- •8.5.2. Практические работы
- •Выполнение работы
- •Контрольные вопросы
- •Литература
- •8.6. Понятие об аффинной или биоспецифической хроматографии
- •Контрольные вопросы
- •Литература
- •Глава 9. Газовая хроматография
- •9.1. Теоретические основы метода
- •9.2. Аппаратурное оформление газовой хроматографии
- •9.3. Качественный и количественный анализ
- •9.4. Применение газовой хроматографии
- •9.5. Практические работы
- •Контрольные вопросы
- •Литература
ление клеточного материала и уплотнение белков. В нижнем геле происходит разделение белков.
6.4. Диск-электрофорез
Электрофорез в ПААГе часто называют диск-электофорезом. Это название происходит от двух английских слов – discontinuity, обозначающего в данном случае неоднородность электрофоретической среды, и discoid – дискоообразный. Дело в том, что по случайному совпадению при стандартных условиях проведения опыта разделенные зоны имеют форму дисков.
Для диск-электрофореза характерны скачкообразные изменения pH, концентрации геля и градиента напряжения. Как известно, нижняя часть трубки заполнена разделяющим гелем с порами, которые действуют как молекулярное сито по отношению к разделяемым молекулам. Над разделяющим гелем имеется концентрирующий гель, имеющий крупные поры и поэтому не обладающий свойствами молекулярного сита, а еще выше располагается стартовый гель, содержащий пробу и краситель, использующийся в качестве свидетеля. Смысл диск-электрофореза состоит
всоздании очень узкой стартовой зоны, которая обеспечивает высокую разрешающую способность. Как это достигается?
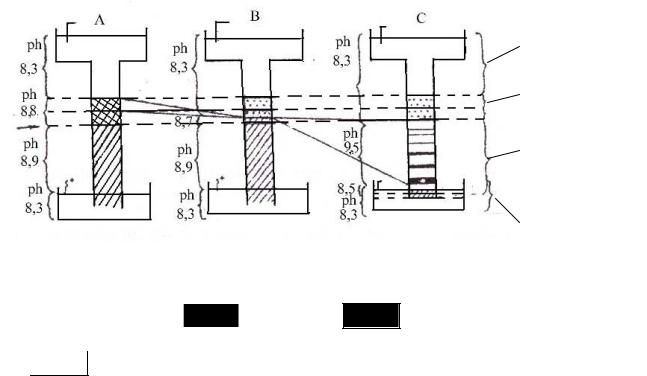
Дело в том, что в состав как электродного буфера, так и буфера концентрирующего геля входит слабое аминное основание - трис, но в электродный буфер к трису прибавлена слабая кислота глицин (трисглициновый буфер, pH = 8,3), а концентрирующий гель содержит соляную кислоту, что дает буферную систему трис-HCl, pH = 6,7 (рис. 6.1.).
Глицин при pH = 8,3 находится в виде цвиттериона (биполярного иона) и только 5% приходится на долю глицинатного аниона. В электрическом поле глицинатные ионы, движущиеся из верхнего резервуара
вконцентрирующий гель, имеют гораздо меньшую подвижность, чем ионы хлора, и, следовательно, ”тянутся” позади них. В среде верхнего геля при pH=6,7 подвижность глицинатных ионов становится еще меньше, так как в результате дополнительного протонирования увеличивается количество цвиттерионов (изоэлектрическая точка глицина). Ионы хлора, наоборот, продвигаются очень быстро, и между этими двумя разновидностями ионов возникает граница раздела. Так как и ионы хлора, и глицинатные ионы представляют собой часть одной и той же электрической системы, то в области локализации менее подвижных глицинатных ионов напряжение увеличивается, а в области более подвижных ионов хлора – уменьшается. Следовательно, замыкающие ионы будут стремиться догнать ведущие, а белковые анионы, промежуточные по подвижности, будут располагаться между первыми и вторыми иона-
102
ми. В итоге происходит концентрирование белковых анионов позади ведущих ионов. Образуется чрезвычайно узкая белковая полоса, которая подходит к разделяющему гелю вслед за ионами хлора.
глициновый
буфер
исходный объем пробы концентрирующий гель мелкопористый гель глициновый буфер
Рис. 6.1. Разделение белков с помощью диск-электрофореза
- |
глицин, |
|
, |
- |
 крупнопористая противоконвекционная среда
крупнопористая противоконвекционная среда
Когда замыкающие глицинатные ионы доходят до нижнего геля, их число и подвижность увеличиваются, поскольку значение pH = 9,5 приближается к pK глицина. Теперь подвижность глицинатных ионов становится выше, чем у белковых анионов, подвижность которых замедляется в разделительном геле вследствие эффекта молекулярного сита. Глицинатные ионы перегоняют все белковые молекулы и догоняют анионы хлора. Как только последний ион хлора уходит из нижнего геля, pH повышается, потому что ионы хлора заменяются более основными глицинатными, и вместо исходной буферной системы трис-HCI образуется трис-глициновый буфер. Вследствие этого возрастает отрицательный заряд белковых анионов, и их движение происходит в соответствии с величинами отношения заряд/масса.
103
