
- •Основные газовые законы. Определение молекулярных масс газообразных веществ.
- •Определение молекулярных масс газообразных веществ
- •Основные стехиометрические законы.
- •Понятие о химическом эквиваленте и эквивалентной массе простых и сложных веществ. Закон химических эквивалентов.
- •Волновые свойства электрона. Квантовые числа s-, p-, d-, f-состояния электрона. Электронные орбитали. Проскок электрона.
- •Принцип Паули. Определение электронной емкости уровней, подуровней и орбиталей. Правило Хунда.
- •Порядок заполнения подуровней электронами. Правила Клечковского, электронные и электронографические формулы.
- •Периодический закон д.И. Менделеева и периодическая система элементов: ряды, периоды, подгруппы, порядковый номер. Электронные аналоги.
- •Периодическое изменение свойств химических элементов. Радиус атомов, сродство к электрону, энергия ионизации, электроотрицательность.
- •Оксиды. Классификация, способы получения, химические свойства.
- •Кислоты. Классификация, способы получения, химические свойства.
- •Основания. Классификация, способы получения, химические свойства.
- •Соли. Классификация, способы получения, химические свойства.
- •Образование химической связи. Энергия связи и длина связи. Типы химической связи. Межмолекулярное взаимодействие. Водородная связь.
- •Ковалентная (атомная) связь. Метод валентных связей. Возбужденные состояния атомов.
- •Валентность и степень окисления. Способы определения степени окисления. Основные окислители и восстановители. Уравнять окислительно-восстановительную реакцию ионно-электронным методом.
- •Направленность ковалентной связи. Σ и π-связи. Гибридизация атомных орбиталей.
- •Полярность связи. Ионная (электронная) связь. Полярность молекул и их дипольный момент.
- •Донорно-акцепторный механизм ковалентной связи. Комплексные соединения.
- •Основные положения метода молекулярных орбиталей. Связывающие и разрыхляющие орбитали. Энергетические диаграммы.
- •Металлическая связь. Роль металлической связи в формировании физических и химических свойств металлов.
- •Система. Фаза. Компонент. Параметры системы. Правило фаз Гиббса.
- •Функции состояния: внутренняя энергия и стандартная энтальпия образования химических веществ
- •Первое начало термодинамики. Теплота, работа. Закон Гесса. Следствия из закона Гесса. Термохимические расчеты.
- •Зависимость теплового эффекта химической реакции от температуры (закон Кирхгоффа). Теплоемкость.
- •Второе начало термодинамики. Понятие об энтропии. Расчет энтропии. Изменение энтропии при химических процессах и фазовых переходах.
- •Объединенная формула первого и второго начала термодинамики. Свободная энергия Гиббса и Гельмгольца.
- •Третий закон термодинамики. Постулат Планка.
- •Постулат Планка
- •Условия самопроизвольного протекания химических реакций.
- •Константа химического равновесия. Расчет кр и кс.
- •Скорость химической реакции. Закон действующих масс. Константы скорости гомогенной и гетерогенной химических реакций. Связь константа скорости с константой равновесия
- •Закон действующих масс (з.Д.М.)
- •Кинетическая классификация по степени сложности. Молекулярность и порядок реакции. Обратимые и необратимые реакции. Классификация реакций по степени сложности
- •Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса. Зависимость скорости реакции от температуры.
- •Энергия активации химической реакции. Аналитический и графический метод расчета энергии активации.
- •Катализ. Сущность гомогенного и гетерогенного катализа. Стадии гетерогенного катализа.
- •Растворы (разбавленные, концентрированные, насыщенные, пересыщенные). Способы выражения концентраций растворов.
- •Способы выражения концентрации растворов
- •Растворимость. Произведение растворимости. Изменение энтальпии и энтропии при растворении.
- •Физические и химические процессы при растворении. Растворимость твердых тел и жидкостей в жидкостях. Физические и химические процессы при растворении.
- •Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
- •Законы Рауля.
- •Э лектролитическая диссоциация. Степень диссоциации. Слабые электролиты.
- •Константа диссоциации. Закон разведения Оствальда.
- •Сильные электролиты. Понятие активности и коэффициента активности. Ионная сила раствора.
- •Электролитическая диссоциация воды. Ионное произведение воды. Водородный показатель. Понятие об индикаторах.
- •Гидролиз солей. Константа и степень гидролиза.
- •Окислительно-восстановительные реакции. Ионно-электродный метод подбора коэффициентов в окислительно-восстановительных реакциях.
- •Возникновение скачка потенциала на границе раздела "металл-раствор".
- •Равновесный электродный потенциал.
- •Медно-цинковый гальванический элемент Якоби-Даниеля. Процессы на электродах. Понятие об эдс.
- •Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
- •Стандартный водородный электрод. Формула Нерста. Стандартный потенциал. Ряд напряжений металла.
- •Типы электродов. Стеклянный электрод.
- •Электролиз. Последовательность разряда ионов на катоде и аноде.
- •Законы Фарадея. Выход по току
- •Коррозия металлов. Химическая и электрохимическая коррозия
- •Основные методы борьбы с коррозией. Почвенная коррозия.
- •Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •Сущность термографического анализа. Основные принципы построения диаграммы плавкости бинарных систем.
- •Диаграмма состояния однокомпонентной системы на примере воды.
- •Эвтектическая диаграмма плавкости (без образования твердых растворов).
- •Диаграмма плавкости непрерывных твердых растворов. Правило рычага.
- •Диаграмма плавкости бинарной системы с ограниченными твердыми растворами.
- •Диаграммы плавкости бинарных систем с образованием химических соединений.
- •Адсорбция и абсорбция. Хемосорбция.
- •Агрегатные состояния вещества. Стеклообразное и жидкокристаллическое состояния вещества.
Сущность термографического анализа. Основные принципы построения диаграммы плавкости бинарных систем.
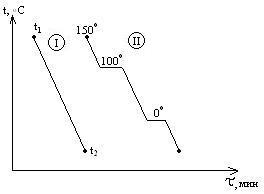 Термографический
анализ – кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния) строят
исходя из кривых охлаждения, которые
изображаются в координатах: температура(Оу),
время(Ох). Рассмотрим кривые охлаждения
двух систем. Система I в
интервале t1-t2
не испытывает никаких фазовых превращений,
температура меняется монотонно. Кривая
II отвечают охлаждению
воды от 150 o C
(пар при атмосферном давлении) до 0 o
C и ниже. При 100 o
C наблюдается горизонтальный
участок, отвечающий фазовому переходу
– процессу конденсации пара, температура
поддерживается неизменной, пока не
исчезнет весь пар. Постоянство температуры
обеспечивается за счёт выделения в
процессе конденсации пара теплоты
испарения воды. От 100 o
C до 0 o
C наблюдается монотонный
ход кривой охлаждения – остывает жидкая
вода. При 0 o
C наблюдается второй
горизонтальный участок, отвечающий
фазовому переходу – процессу
кристаллизации. Температура поддерживается
постоянной за счет выделения теплоты
плавления.
Термографический
анализ – кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния) строят
исходя из кривых охлаждения, которые
изображаются в координатах: температура(Оу),
время(Ох). Рассмотрим кривые охлаждения
двух систем. Система I в
интервале t1-t2
не испытывает никаких фазовых превращений,
температура меняется монотонно. Кривая
II отвечают охлаждению
воды от 150 o C
(пар при атмосферном давлении) до 0 o
C и ниже. При 100 o
C наблюдается горизонтальный
участок, отвечающий фазовому переходу
– процессу конденсации пара, температура
поддерживается неизменной, пока не
исчезнет весь пар. Постоянство температуры
обеспечивается за счёт выделения в
процессе конденсации пара теплоты
испарения воды. От 100 o
C до 0 o
C наблюдается монотонный
ход кривой охлаждения – остывает жидкая
вода. При 0 o
C наблюдается второй
горизонтальный участок, отвечающий
фазовому переходу – процессу
кристаллизации. Температура поддерживается
постоянной за счет выделения теплоты
плавления.
Р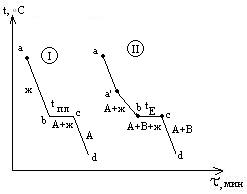 ассмотрим
кривые охлаждения чистого
металла (I) и сплава с так
называемой эвтектикой (II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc, отвечающая
процессу кристаллизации металла. При
tпл в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.
ассмотрим
кривые охлаждения чистого
металла (I) и сплава с так
называемой эвтектикой (II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc, отвечающая
процессу кристаллизации металла. При
tпл в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.
Кривая II отвечает охлаждению сплава А-В. От “а” до “a’ “ температура меняется монотонно, остывает жидкая фаза. При достижении точки a’ из жидкой фазы начинают выпадать кристаллы А – одного из компонентов сплава, при этом жидкая фаза за счет этого начнет обогащаться компонентом В. Таким образом, в интервале a’-b в равновесии находятся жидкая и твердая фазы различного состава, площадки на кривой охлаждения не наблюдается. За счет выделения при кристаллизации А теплоты плавления этого компонента темп охлаждения сплава замедляется, и на кривой наблюдается перелом. Выпадение кристаллов А продолжается до тех пор, пока жидкая фаза не достигнет так называемого “эвтектического состава”. Основной особенностью эвтектического сплава является то, что он кристаллизуется подобно чистому компоненту – на кривой охлаждения наблюдается площадка.
Из жидкой фазы одновременно выпадают кристаллы А и В и, таким образом при tЕ (отрезок bc) в равновесии находятся жидкая и твердая фазы одинакового состава. Отрезок cd отвечают охлаждению твердого сплава.
Остановки в падении температуры могут наблюдаться и на кривой охлаждения уже твердого металла, указываю на переходы металла из одной аллотропной формы в другую
Диаграмма состояния однокомпонентной системы на примере воды.
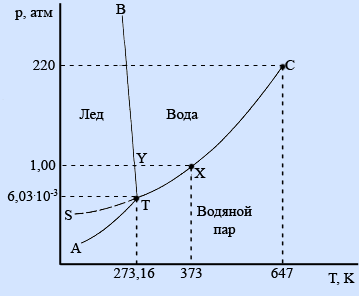
Области фазовой диаграммы, ограниченные кривыми, соответствуют тем условиям (температурам и давлениям), при которых устойчива только одна фаза вещества. Например, при любых значениях температуры и давления, которые соответствуют точкам диаграммы, ограниченным кривыми ВТ и ТС, вода существует в жидком состоянии. При любых температуре и давлении, соответствующих точкам диаграммы, которые расположены ниже кривых АТ и ТС, вода существует в парообразном состоянии.
Кривые фазовой диаграммы соответствуют условиям, при которых какие-либо две фазы находятся в равновесии друг с другом. Например, при температурах и давлениях, соответствующих точкам кривой ТС, вода и ее пар находятся в равновесии. Это и есть кривая давления пара воды. В точке Х на этой кривой жидкая вода и пар находятся в равновесии при температуре 373 К (100°С) и давлении 1 атм (101,325 кПа); точка Х представляет собой точку кипения воды при давлении 1 атм.
Кривая АТ является кривой давления пара льда; такую кривую обычно называют кривой сублимации.
Кривая ВТ представляет собой кривую плавления. Она показывает, как давление влияет на температуру плавления льда: если давление возрастает, температура плавления немного уменьшается. Такая зависимость температуры плавления от давления встречается редко. Обычно возрастание давления благоприятствует образованию твердого вещества. В случае воды повышение давления приводит к разрушению водородных связей, которые в кристалле льда связывают между собой молекулы воды, заставляя их образовывать громоздкую структуру. В результате разрушения водородных связей происходит образование более плотной жидкой фазы.
В точке Y на кривой ВТ лед находится в равновесии с водой при температуре 273 К (0°С) и давлении 1 атм. Она представляет собой точку замерзания воды при давлении 1 атм.
Кривая SТ указывает давление пара воды при температурах ниже ее точки замерзания. Поскольку вода в нормальных условиях не существует в виде жидкости при температурах ниже ее точки замерзания, каждая точка на этой кривой соответствует воде, находящейся в метастабильном состоянии. Это означает, что при соответствующих температуре и давлении вода находится не в своем наиболее устойчивом (стабильном) состоянии. Явление, которое соответствует существованию воды в метастабильном состоянии, описываемом точками этой кривой, называется переохлаждением.
На фазовой диаграмме имеются две точки, представляющие особый интерес. Прежде всего, отметим, что кривая давления пара воды заканчивается точкой С. Она называется критической точкой воды. При температурах и давлениях выше этой точки пары воды не могут быть превращены в жидкую воду никаким повышением давления. Другими словами, выше этой точки паровая и жидкая формы воды перестают быть различимыми. Критическая температура воды равна 647 К, а критическое давление составляет 220 атм.
Точка Т фазовой диаграммы называется тройной точкой. В этой точке лед, жидкая вода и пары воды находятся в равновесии друг с другом. Этой точке соответствуют температура 273,16 К и давление 6,03 10-3 атм. Лишь при указанных значениях температуры и давления все три фазы воды могут существовать вместе, находясь в равновесии друг с другом.
