
- •Основные газовые законы. Определение молекулярных масс газообразных веществ.
- •Определение молекулярных масс газообразных веществ
- •Основные стехиометрические законы.
- •Понятие о химическом эквиваленте и эквивалентной массе простых и сложных веществ. Закон химических эквивалентов.
- •Волновые свойства электрона. Квантовые числа s-, p-, d-, f-состояния электрона. Электронные орбитали. Проскок электрона.
- •Принцип Паули. Определение электронной емкости уровней, подуровней и орбиталей. Правило Хунда.
- •Порядок заполнения подуровней электронами. Правила Клечковского, электронные и электронографические формулы.
- •Периодический закон д.И. Менделеева и периодическая система элементов: ряды, периоды, подгруппы, порядковый номер. Электронные аналоги.
- •Периодическое изменение свойств химических элементов. Радиус атомов, сродство к электрону, энергия ионизации, электроотрицательность.
- •Оксиды. Классификация, способы получения, химические свойства.
- •Кислоты. Классификация, способы получения, химические свойства.
- •Основания. Классификация, способы получения, химические свойства.
- •Соли. Классификация, способы получения, химические свойства.
- •Образование химической связи. Энергия связи и длина связи. Типы химической связи. Межмолекулярное взаимодействие. Водородная связь.
- •Ковалентная (атомная) связь. Метод валентных связей. Возбужденные состояния атомов.
- •Валентность и степень окисления. Способы определения степени окисления. Основные окислители и восстановители. Уравнять окислительно-восстановительную реакцию ионно-электронным методом.
- •Направленность ковалентной связи. Σ и π-связи. Гибридизация атомных орбиталей.
- •Полярность связи. Ионная (электронная) связь. Полярность молекул и их дипольный момент.
- •Донорно-акцепторный механизм ковалентной связи. Комплексные соединения.
- •Основные положения метода молекулярных орбиталей. Связывающие и разрыхляющие орбитали. Энергетические диаграммы.
- •Металлическая связь. Роль металлической связи в формировании физических и химических свойств металлов.
- •Система. Фаза. Компонент. Параметры системы. Правило фаз Гиббса.
- •Функции состояния: внутренняя энергия и стандартная энтальпия образования химических веществ
- •Первое начало термодинамики. Теплота, работа. Закон Гесса. Следствия из закона Гесса. Термохимические расчеты.
- •Зависимость теплового эффекта химической реакции от температуры (закон Кирхгоффа). Теплоемкость.
- •Второе начало термодинамики. Понятие об энтропии. Расчет энтропии. Изменение энтропии при химических процессах и фазовых переходах.
- •Объединенная формула первого и второго начала термодинамики. Свободная энергия Гиббса и Гельмгольца.
- •Третий закон термодинамики. Постулат Планка.
- •Постулат Планка
- •Условия самопроизвольного протекания химических реакций.
- •Константа химического равновесия. Расчет кр и кс.
- •Скорость химической реакции. Закон действующих масс. Константы скорости гомогенной и гетерогенной химических реакций. Связь константа скорости с константой равновесия
- •Закон действующих масс (з.Д.М.)
- •Кинетическая классификация по степени сложности. Молекулярность и порядок реакции. Обратимые и необратимые реакции. Классификация реакций по степени сложности
- •Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса. Зависимость скорости реакции от температуры.
- •Энергия активации химической реакции. Аналитический и графический метод расчета энергии активации.
- •Катализ. Сущность гомогенного и гетерогенного катализа. Стадии гетерогенного катализа.
- •Растворы (разбавленные, концентрированные, насыщенные, пересыщенные). Способы выражения концентраций растворов.
- •Способы выражения концентрации растворов
- •Растворимость. Произведение растворимости. Изменение энтальпии и энтропии при растворении.
- •Физические и химические процессы при растворении. Растворимость твердых тел и жидкостей в жидкостях. Физические и химические процессы при растворении.
- •Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
- •Законы Рауля.
- •Э лектролитическая диссоциация. Степень диссоциации. Слабые электролиты.
- •Константа диссоциации. Закон разведения Оствальда.
- •Сильные электролиты. Понятие активности и коэффициента активности. Ионная сила раствора.
- •Электролитическая диссоциация воды. Ионное произведение воды. Водородный показатель. Понятие об индикаторах.
- •Гидролиз солей. Константа и степень гидролиза.
- •Окислительно-восстановительные реакции. Ионно-электродный метод подбора коэффициентов в окислительно-восстановительных реакциях.
- •Возникновение скачка потенциала на границе раздела "металл-раствор".
- •Равновесный электродный потенциал.
- •Медно-цинковый гальванический элемент Якоби-Даниеля. Процессы на электродах. Понятие об эдс.
- •Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
- •Стандартный водородный электрод. Формула Нерста. Стандартный потенциал. Ряд напряжений металла.
- •Типы электродов. Стеклянный электрод.
- •Электролиз. Последовательность разряда ионов на катоде и аноде.
- •Законы Фарадея. Выход по току
- •Коррозия металлов. Химическая и электрохимическая коррозия
- •Основные методы борьбы с коррозией. Почвенная коррозия.
- •Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •Сущность термографического анализа. Основные принципы построения диаграммы плавкости бинарных систем.
- •Диаграмма состояния однокомпонентной системы на примере воды.
- •Эвтектическая диаграмма плавкости (без образования твердых растворов).
- •Диаграмма плавкости непрерывных твердых растворов. Правило рычага.
- •Диаграмма плавкости бинарной системы с ограниченными твердыми растворами.
- •Диаграммы плавкости бинарных систем с образованием химических соединений.
- •Адсорбция и абсорбция. Хемосорбция.
- •Агрегатные состояния вещества. Стеклообразное и жидкокристаллическое состояния вещества.
Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
Растворимость газов в жидкостях.
Растворимость газов с повышением температуры уменьшается.
Согласно закону Генри, растворимость газа при постоянной температуре пропорциональна давлению газа над раствором.
![]()
где Г- константа Генри.
Закону Генри строго подчиняются те газы, растворимость которых невелика и которые не вступают в химическое взаимодействие с растворителем
Закон Джона Дальтона.
В случае растворения смеси газов в жидкости каждый их них растворяется пропорционально своему парциальному давлению.
Закон распределения и коэффициент распределения
В систему из дух несмешивающихся жидкостей I и II введено вещество III, концентрация которого в жидкостях с1 и с2. Согласно закону распределения, соотношение концентраций при Т = const есть величина постоянная, именуемая коэффициентом распределения L:
![]()
L константа, не зависящая от количества растворённого вещества в обеих жидкостях. Она определяется природой растворителей, природой растворённого вещества и температурой.
Закон Генри частный случай более общего закона распределения.
Законы Рауля.
Согласно первому закону Рауля, давление пара растворителя над раствором пропорционально мольной доле растворителя в растворе.
![]()
Относительное понижение давления пара растворителя над раствором равно мольной доли растворённого вещества.
Это вторая формулировка 1-го закона Рауля.
Графическое изображение 1-го закона Рауля.
Если система полностью подчиняется закону Рауля, на графике будут наблюдаться прямолинейные зависимости.
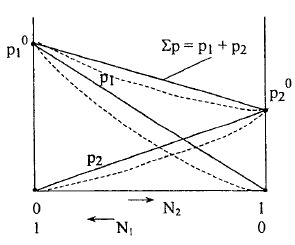 Температура
замерзания раствора ниже температуры
замерзания растворителя, а температуры
кипения
выше.
Температура
замерзания раствора ниже температуры
замерзания растворителя, а температуры
кипения
выше.
Согласно второму закону Рауля, повышение температуры кипения раствора и понижение температуры его замерзания пропорциональны моляльной концентрации раствора.
![]()
![]() не зависит от природы растворённого
вещества, а определяется природой
растворителя и моляльностью, т.е. числом
растворённых молекул в определённого
количестве растворителя.
не зависит от природы растворённого
вещества, а определяется природой
растворителя и моляльностью, т.е. числом
растворённых молекул в определённого
количестве растворителя.
С
помощью закона Рауля можно определять
неизвестные молекулярные массы
растворённых веществ. Если определяется
![]() раствора, то метод носит название
эбулиоскопия,
если
раствора, то метод носит название
эбулиоскопия,
если ![]() - криосокпия.
- криосокпия.
Э лектролитическая диссоциация. Степень диссоциации. Слабые электролиты.

Константа диссоциации. Закон разведения Оствальда.
Сильные электролиты. Понятие активности и коэффициента активности. Ионная сила раствора.
В растворах сильных электролитов в результате их практически полной диссоциации создается высокая концентрация ионов.
Между катионами и анионами возникает электростатическое притяжение и эффективная, (то есть экспериментально определенная) концентрация этих ионов оказывается меньше, чем их истинная концентрация.
Для оценки способности ионов
к химическому взаимодействию в растворах
сильных электролитов используют понятие
активности ( ![]() ).
).
Активностью иона называют эффективную или условную концентрацию его, соответственно которой он действует в химических реакциях.
Между активностью иона (
)
и его действительной концентрацией
( ![]() )
существует зависимость
)
существует зависимость
![]() ,
,
где ![]() -
коэффициент активности;
-
коэффициент активности; ![]()
Таким образом, коэффициент
активности
это отношение активности иона к его
общей концентрации. Так как ![]() ,
то
,
то ![]() ,
поэтому при точных расчетах в уравнение
закона действующих масс должны входить
активности ионов, а не их концентрации.
Если диссоциацию электролита изобразить
схемой
,
поэтому при точных расчетах в уравнение
закона действующих масс должны входить
активности ионов, а не их концентрации.
Если диссоциацию электролита изобразить
схемой
![]() ,-
,-
то константа диссоциации ![]() будет
выражаться следующим образом:
будет
выражаться следующим образом:
![]()
В этом случае называют термодинамической константой.
Понятие активности применимо
не только к отдельным ионам, но и к
электролиту в целом. Для электролита ![]() средняя
активность и средний коэффициент
активности связаны с активностями и
коэффициентами активности катионов
средняя
активность и средний коэффициент
активности связаны с активностями и
коэффициентами активности катионов ![]() и
анионов
и
анионов ![]() следующими
соотношениями:
следующими
соотношениями:
![]()
![]()
Коэффициенты активности
ионов зависят не только от концентрации
сильного электролита, но и от концентрации
всех других ионов, присутствующих в
растворе. Мерой электростатического
взаимодействия между ионами является ионная
сила раствора- ![]() ,
которая вычисляется по формуле:
,
которая вычисляется по формуле:
![]()
где ![]() концентрации
различных ионов, моль/л;
концентрации
различных ионов, моль/л;
![]() заряды
этих ионов.
заряды
этих ионов.
