
- •Часть 1. История и общая микробиология.
- •Эндогенные:
- •31) Индикация и идентификация вирусов при различных методах культивирования.
- •§ 96 % Спирт (30 мин.).
- •Часть 2. Инфекция и иммунитет.
- •2. Клеточные факторы врожденного иммунитета. Фагоцитоз.
- •3. Иммунная система организма. Основные клетки иммунной системы и их характеристика.
- •4. Гуморальные факторы врождённого иммунитета.
- •Часть 3. Частная микробиология.
- •Микробиологическая диагностика менингококковой инфекции
- •Бактериологический метод
- •1 Этап – вчк.
- •Морфологические и тинкториальные свойств
- •Культуральные свойства
- •Биохимические свойства
- •Антигенная структура
- •Фагочувствительность
- •Резистентность холерного вибриона
- •Эпидемиология
- •Факторы патогенности холерного вибриона
- •Патогенез холеры
- •Клиническая картина холеры
- •Диагностика
- •Иммунитет
- •Лечение холеры
- •Профилактика холеры
- •Пищевые отравления.
- •Пищевые отравления микробной этиологии
- •Лабораторная диагностика пищевых токсикоинфекций (пти).
- •Профилактика отравлений микробной природы Профилактика токсикоинфекций включает:
- •Профилактика стафилококковых токсикозов:
- •Общая вирусология
- •1. Таксономия, классификация
- •2. Морфология, размеры, особенности генома
- •3. Этапы репродукции
- •4. Эпидемиология
- •5. Патогенез и клинические проявления;
- •6. Лабораторная диагностика, характер исследуемого материала;
- •7. Особенности вирусологического метода диагностики (культивирование, индикация, идентификация вируса);
- •8. Противовирусный иммунитет;
- •9. Специфическая профилактика;
- •10. Лечение
- •5. Терминальная стадия.
- •1. Прямые методы диагностики.
- •2. Косвенные методы диагностики.
- •1. Этиотропное лечение
- •1. Вирусологический (культуральный) метод
- •2. Молекулярно-генетические методы
- •4. Методы детекции антител
- •1. Этиотропное лечение
- •2. Патогенетическая терапия
- •3. Симптоматическая терапия часть 4. Санитарная микробиология.
- •Методы косвенной индикации возможного присутствия возбудителя во внешней среде.
- •Часть 5. Микробиология инфекций, связанных с оказанием медицинской помощи (исмп).
- •Лабораторная диагностика гнойно-воспалительных заболеваний (гвз)
- •Микробиологическое исследование крови
- •Этиологическая структура бактериемий
- •Микробиологическое исследование мочи
- •Полуколичественный метод определения степени бактериурии
- •Внутрибольничная пневмония
- •Послеоперационные инфекции
- •Раневые инфекции
5. Терминальная стадия.
ПРИЛОЖЕНИЕ 2
Выделяют СПИД-векторные (индикаторные, сопутствующие, ассоциированные, оппортунистические) заболевания. По этиологическому фактору они подразделяются на следующие группы:
1. Бактериальные инфекции (внелегочный туберкулез, тяжелые пневмонии, инфекции, вызванные атипичными микобактериями и др.).
2. Грибковые инфекции (кандидоз, криптококкоз, гистоплазмоз, пневмоцистная пневмония, кокцидиоидомикоз).
3. Вирусные инфекции (герпесвирусные, цитомегаловирусная, папилломавирусная и др.).
4. Протозойные инфекции (токсоплазмоз, криптоспоридиоз, микроспоридиоз и др.).
5. Другие заболевания (саркома Капоши, лимфомы, ВИЧ-энцефалопатия, ВИЧ-истощающий синдром и др.).
Бешенство. Этиология, принципы лабораторной диагностики, профилактика.
Бешенство - (Rabies,Lyssa,Hydrophobiya). Бешенство или водобоязнь – острое вирусное зоонозное заболевание, поражающее человека, характеризующееся тяжёлыми поражениями нервной системы, молниеносным течением и неизменно летальным исходом.
История. Луи Пастер в 1881-1885 году провёл аттенуацию уличного вируса бешенства в фиксированный путём пассажей через мозг кроликов. Приготовил вакцину и испытал её на собаках, а затем на человеке. В лаборатории Пастера Н.Ф.Гамалея изучил его метод и высказал Пастеру верную мысль о необходимости как можно более быстрого проведения прививок, которые действительны только до проникновения вируса бешенства в центральную нервную систему. Он испытал на себе штамм вируса для доказательства безопасности. Организовал вторую в мире пастеровскую станцию в Одессе. В Перми вакцина против бешенства изготовлена профессором В.М.Здравосмысловым. Первые прививки против бешенства были проведены 15 мая 1898 года в батериологической лаборатории Губернского земства.
Таксономическое положение.
Вирус относится к порядку Mononegavirales, семейству Rhabdoviridae. роду Lyssavirus ,виду Rhabies virus. Выделено 7 генотипов и 4 подобных неклассифицированных вируса.
Структура вирусной частицы.Рис.1.
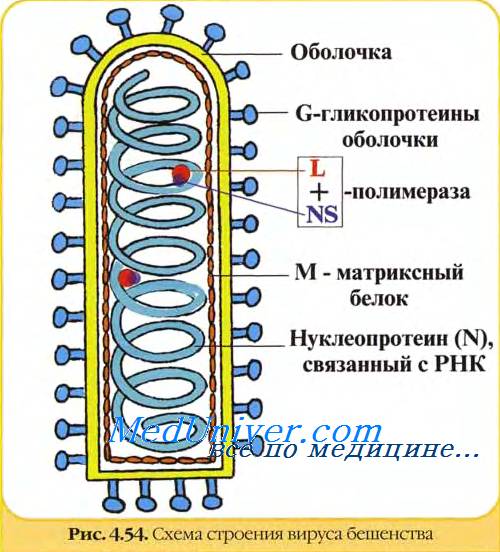 Рис.1.
Рис.1.
Вирусная частица имеет пулевидную форму длиной 180 нм, шириной 70-80 нм. В центре содержится РНК, которая вместе с белком Nр капсида формирует нуклеокапсид спиральной симметрии. Имеется фермент полимераза ( L – транскриптаза, Ns – фосфопротеин). Нуклеокапсид стянут матричным белком M, а снаружи окружён суперкапсидом с шипиками гликопротеидов -G .
Антигенные свойства.
Nр - нуклеопротеин- белок нуклеокапсида - группоспецифический антиген
G - гликопротеин –типоспецифический антиген
Известно несколько серотипов:
К 1 относится «уличный вирус бешенства» и «фиксированный вирус» (PV-11) Ко 2 типу сходные вирусы ( вирус» дикования оленей, песцов и лис в Арктике, вирус летучих мышей в Америке, вирус безумной собаки в Африке, Mocola virus и др.)
Культивирование вируса. Вирус накапливается в организме сирийских хомячков и мышей, в куриных и утиных эмбрионах. Культивирование проводят в первичных (почечный эпителий хомячка), перевиваемых и диплоидных культурах клеток. Репродукция идёт в цитоплазме, выход новых вирусных частиц происходит путём почкования.
В поражённых клетках можно обнаружить включения Бабеша-Негри (эозинофильные тельца размером 5-10 мкм, образованные скоплениями вирусных нуклеокапсидов.
Вирус бешенства обладает гемадсорбирующей и геагглютинирующей активностью.
Резистентность. Несколько недель сохраняется при низкой температуре, в трупах, замёрзшей слюне животного.
Инактивируется: нагреванием (при 56°С в течение 15 мин, при кипячении - за 2 мин.), действии ультрафиолетовых и солнечных лучей, при высушивании через несколько дней. Разрушается кислотами, щелочами, лизолом, этанолом, сулемой, йодом. Быстро инактивируется карболовой кислотой (3-5%), хлорамином (2-3%).
Эпидемиология.
Вирус цикулирует среди диких животных. Резервуаром вируса являются лисы 80% рис.2, волки 1%, еноты 14%, шакалы, барсуки, кабаны, рыси, белки, летучие мыши 4-5%. Животное заразно за 2-10 дней до клинических проявлений. Вирус накапливается в слюнных железах и выделяется со слюной и передается при укусах домашним животным и человеку. В антропургических очагах вирус могут поражаться собаки, кошки, кролики, морские свинки, крысы, мыши, вороны.
 Рис 2.Рыжая лиса-
основной резервуар вируса бешенства.
Рис 2.Рыжая лиса-
основной резервуар вируса бешенства.
Патогенез. Репродукция вируса происходит в поперечнополосатых мышцах в месте внедрения (чувствительны клетки с АХР-рецепторами)
В нервную систему он попадает через нервно-мышечные синапсы и сухожильные рецепторы Гольджи - там имеются уязвимые для вируса безмиелиновые нервные окончания. Далее вирус медленно, со скоростью около 3 мм/ч, продвигается по нервным волокнам в ЦНС. Реплицируется в нейронах передних рогов спинного мозга, стволе мозга, таламусе и базальных ганглиях. После репликации в мозге вирус возвращается обратно на периферию по нервным путям в мышцы, роговицу глаза, слёзные железы, кишечник, поджелудочную железу, мочевой пузырь, сосочки языка, волосяные фолликулы кожи, слюнные железы и др.
Смерть наступает вследствие поражения жизненно важных центров — дыхательного и сосудодвигательного.
Клиника.
Выделяют четыре стадии болезни:
- инкубационный период от 6 суток до 6 лет, средний 1-3 мес
- продромальный период;
- период возбуждения;
- период параличей .
Буйная форма (возбуждение, гидро-, аэро-, фото- и акустофобии, саливация) 2-8 дней
Паралитическая форма (возбудимость, параличи) 30 дней
Профилактика. Профилактические мероприятия проводят согласно санитарным и ветеринарным правилам «Профилактика и борьба с заразными болезнями, общими для человека и животных. Бешенство» (СП 3.1. 096-96, ВП 13.3.1103-96).
Местная обработка раны мыльной водой и четвертичными солями аммония. Введение антирабической вакцины. В России 2 вида антирабических вакцин:
КАВ и КоКАВ - содержат инактивированные вакцинные штаммы вирусов, выращенные в культурах клеток
КАВ – это культуральная антирабическая вакцина, также называется Рабивак.
КоКАВ – это концентрированная культуральная антирабическая вакцина.
КоКАВ, соответственно, меньше по объему, требует меньшего числа доз и обладает большей эффективностью. Для производства вакцин используют
1-й штамм вируса бешенства Внуково -32 (Селимов) выращен на первичной культуре клеток почек сирийских хомяков, концентрирован и очищен методами ультрафильтрации, ультрацентрифугирования, ионообменной хроматографии, инактивирован УФО или гамма-лучами. 2-й Штамм получен в культуре диплоидных клеток
Инактивированная антирабическая вакцина вводится в дозе 1.0 мл на 3, 7, 14 и 28 дни после первой вакцинации.
При тяжёлых укусах комбинированное введение иммуноглобулина однократно и вакцины.
Создание зоны свободной от вируса. Вакцинация домашних и диких животных. Вакцины для животных - живые и инактивированные. (Оралрабивак, мультикан 8 и др.)
Лабораторная диагностика.
Микробиологическая диагностика бешенства у человека чаще проводится посмертно с целью подтверждения клинического диагноза. Для исследования у погибшего берут кусочки головного мозга и подчелюстные слюнные железы и слюну животных и проводят определение телец Бабеша–Негри, антигена в РИФ и РНК в ПЦР.
Для прижизненной диагностики используют отпечатки с роговицы и слюну.
Обнаружение антигена в криостатных срезах кожи в волосяных фолликулах в РИФ. Определение антигенов в ИФА. Определение РНК в слюне, слезах, смж, моче и криостатных срезах кожи в ПЦР
Вирусологическое исследование проводят в специальных вирусологических лабораториях. Выделение вируса возможно внутримозговым заражением белых мышей, сирийских хомячков, морских свинок и в культуре клеток. Идентификацию вируса проводят путём обнаружения телец Бабеша-Негри и при помощи реакции иммунофлюоресценции или ПЦР.
Серодиагностика только для обследования вакцинированных. Выявление антител проводят в непрямой РИФ, РНГА и ИФА.
COVID-19. Характеристика возбудителя, принципы лабораторной диагностики, профилактика.
Коронавирусы относятся к семейству Coronaviridae , название происходит от лат corona – корона, поскольку пепломеры создают вокруг оболочки вириона обрамление, подобное зубцам короны. Коронавирусы распространены повсеместно, могут поражать птиц и млекопитающих, включая человека. Коронавирус человека впервые был выделен в 1965 году D.Tyrrel и M.Bynoe от больных ОРВИ. Позже в 1975 году Э.Каул и С.Кларк выделили коронавирус при детском энтероколите. Коронавирусы имеют узкий спектр хозяев, однако некоторые из них способны преодолевать межвидовой барьер и вызывать эпидемические вспышки. Некоторые примеры такого рода:
1. В 2002 году в КНР в южной провинции Гуандун случилась вспышка ТОРС( или SARS CoV-severe acute respiratory syndrome coronavirus -тяжёлый острый респираторный синдром), тяжёлой атипичной пневмонии у человека. Природным резервуаром SARS-CoV оказались летучие мыши. От летучих мышей заразились циветы — промежуточные хозяева коронавирусной инфекции, через контакт с которыми SARS-CoV попал в человеческую популяцию.
2. Второй случай возникновения способного к передаче от человека к человеку коронавируса произошел на Аравийском полуострове в 2012 году. Инфекцию назвали MERS, то есть Middle East Respiratory Syndrome, или ближневосточный респираторный синдром. В 2015 году в Южной Корее произошла вспышка ближневосточного респираторного синдрома. Естественным резервуаром предковых форм MERS-CoV оказались летучие мыши, а промежуточными хозяевами — одногорбые верблюды. Все случаи заболеваний географически ассоциированы с Аравийским полуостровом. В настоящее время вирус циркулирует и вызывает заболевания. Заболевание MERS-CoV протекает как бессимптомно, так и с развитием тяжелой пневмонии, септическим шоком и полиорганной недостаточностью, что приводит к смерти примерно в 36% случаев.
3. В конце 2019 года произошла вспышка новой коронавирусной инфекции в городе Ухань Китайской Народной Республики, которая перешла в пандемию (греч. πανδημία «весь народ»).
По решению ВОЗ инфекции присвоено официальное название – COVID-19 (new COronaVIrus Disease 2019). («Coronavirus disease 2019» ), а возбудителю - SARS-CoV-2 новый коронавирус. Появление nCOVID-19 было вызвано случайным, но в то же время закономерным попаданием в нашу популяцию из мира животных SARS-CoV-2. Коронавирус SARS-CoV2 является рекомбинантным вирусом между коронавирусом летучих мышей и пока неуточнённым по происхождению коронавирусом (возможно вирусом змеи). SARS-CoV-2 (2019-nCoV) вызывает потенциально тяжёлая острая респираторная инфекция
Классификация коронавирусов
Семейство Coronaviridae включает в себя два подсемейства:
1. Подсемейство Letovirinae состоит из единственного вида Microhyla letovirus 1, который обнаружили в лягушках.
2. Подсемейство Orthocoronavirinae состоит из четырех родов:
- Alphacoronavirus (19 видов),
- Betacoronavirus (14 видов),
- Deltacoronavirus (7 видов),
- Gammacoronavirus (5 видов).
Структура SARS-CoV.
Это оболочечный вирус сферической формы размером 40-160 нм. Рис.1.
Нуклеокапсид вируса представлен спирально свернутой геномной РНК в комплексе с белком N. Геномная (+)РНК коронавируса непосредственно служит матрицей для трансляции вирусных белков. Нуклеокапсид окружен фосфолипидной мембраной-суперкапсидом, в который встроены белки E(от англ. envelope – оболочка) – малый оболочечный протеин, M(от англ. membrane –мембрана). На поверхности суперкапсида находятся выступы в виде шипов S-белка (от англ. Spike-шип), которые создают вокруг вируса оболочку, похожую на солнечную «корону».
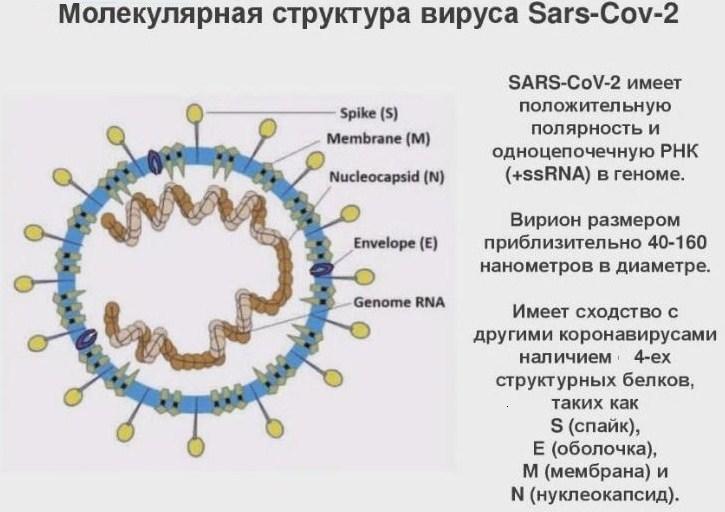
Рис.1.Структура SARS-CoV-2
Резистентность. При комнатной температуре (20-25°) SARS-CoV-2 способен сохранять жизнеспособность на различных объектах окружающей среды в высушенном виде до 3-х суток, в жидкой среде – до 7 суток. При температуре +4°С стабильность вируса сохраняется более 14 дней, при –70°С в течение нескольких лет.
При нагревании до 37°С полная инактивация происходит в течение 1 дня, при 56°С – в течение 45 минут, при 70°С – в течение 5 мин.
Ультрафиолетовое облучение инактивирует вирус в течение 15 минут.
Вирус чувствителен к действию различных дезинфицирующих средств в рабочей концентрации: 70% этанол, гипохлорит натрия 0,01%, хлоргексидин 1%.
Культивирование. Коронавирусы человека культивируются в культурах клеток почек зелёных мартышек и клетках Vero. человеческих диплоидных клетках, в клетках L-132 (клеточные линии из легкого эмбриона человека), в клетках Hela, клетках из почек эмбриона человека, из эпителия носовой полости, трахеи, пищевода эмбриона человека мышиных фибробластов. Вирус SARS-CoV обладает выраженным цитопатическим действием на клетки-мишени и вызывает образование везикул аутофагосом, окруженных двойной мембраной и синцития.
Жизненный цикл коронавирусов
Вирус адсорбируется на клетке-мишени при помощи гликопротеина S и проникает в клетку при слиянии оболочки вируса и цитоплазматической мембраны клетки или посредством рецепторного эндоцитоза. Клеточным рецептором, который используется вирусами SARS-CoV-2 для входа в клетки-мишени, служит ангиотензин-превращающий фермент 2 (ACE2).
Геномная РНК взаимодействует с рибосомами клетки и служит в качестве иРНК. Происходит синтез РНК-зависимой РНК-полимеразы, которая затем считывает геномную РНК, синтезируя минус-нить полной длины. При считывании минус-нити образуется новая геномная плюс-РНК и комплекс из 5-7 субгеномных иРНК. При трансляции каждой субгеномной иРНК образуется один белок.
Белок N связывается в цитоплазме с геномной РНК, в результате чего синтезируется спиральный нуклеокапсид. Гликопротеины S, M, HE и E переносятся в эндоплазматический ретикулум и аппарат Гольджи.
Нуклеотид почкуется через мембраны внутрь шереховатого эндоплазматического ретикулума, содержащего вирусные гликопротеины S и M. Вирионы транспортируются в везикулах к клеточной мембране и выходят из клетки путём экзоцитоза. После выхода вирионов из клетки она погибает.
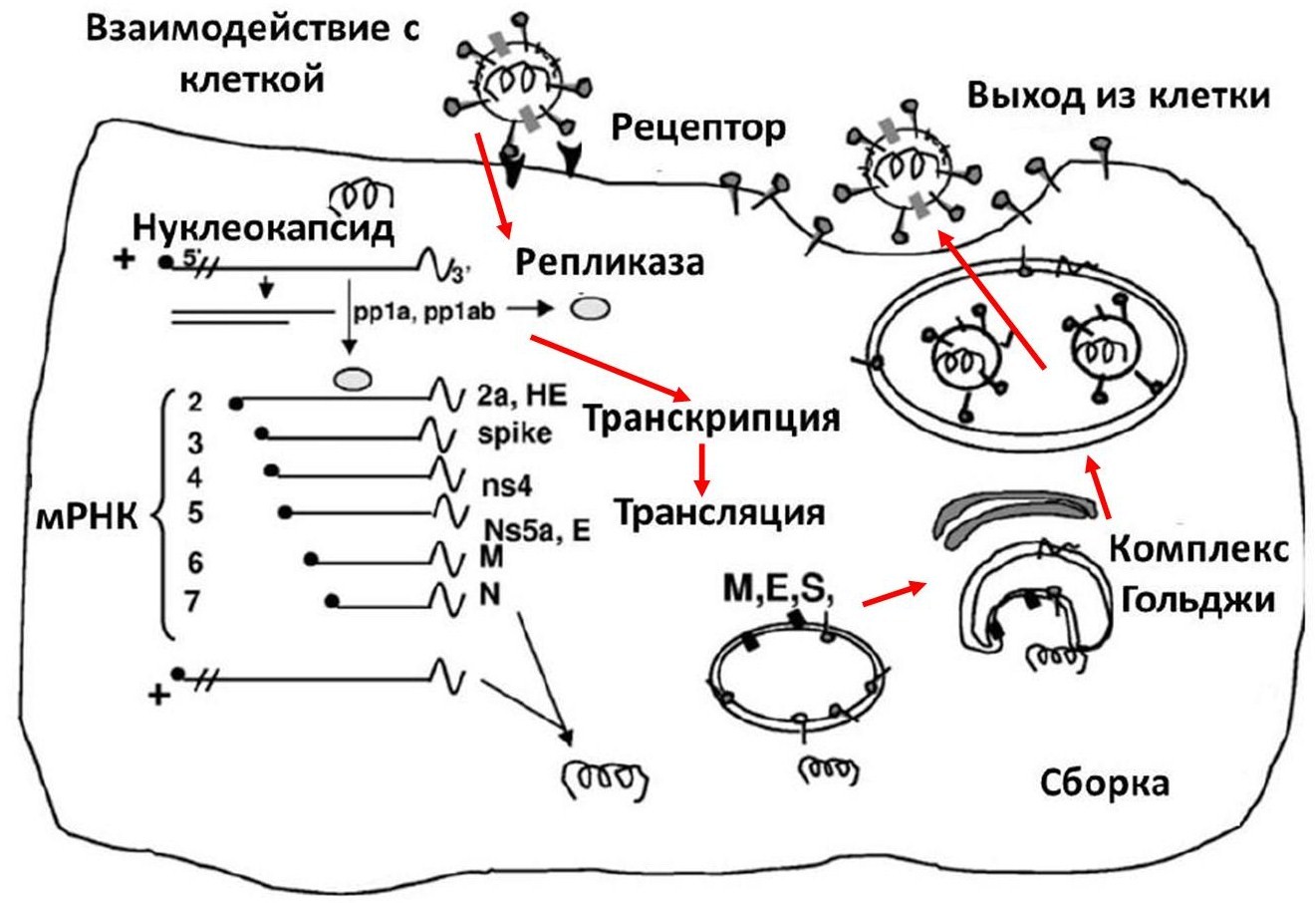
Рис.2 Схема репродукции SARS-CoV-2
Эпидемиология. Основным источником инфекции является больной человек, который наиболее опасен для окружающих в последние два дня инкубационного периода и первые дни болезни. Механизм передачи – аспирационный и контактный. Ведущим путём передачи инфекции является воздушно-капельный при кашле, чихании и разговоре на близком расстоянии (менее 2 метров). Контактно-бытовой путь реализуется через факторы передачи: рукопожатия и другие виды непосредственного контакта с инфицированным человеком, поверхности и предметы, контаминированные возбудителем. Возможен фекально-оральный механизм передачи вируса через воду, пищевые продукты. Показана роль COVID-19 как инфекции, связанной с оказанием медицинской помощи у медицинских работников. В связи с высокой патогенностью вирусы SARS-CoV, MERS-CoV и SARS-CoV-2 отнесены к 2 группе патогенности.
Патогенез.
Входные ворота возбудителя – эпителий верхних дыхательных путей и эпителиоциты желудка и кишечника. Вирус с помощью белка S проникает в клетки–мишени, имеющие рецепторы ангиотензинпревращающего фермента 2-го типа (АПФ2). Затем клеточная трансмембранная сериновая протеаза типа 2 (ТСП-2) способствует связыванию вируса с АПФ-2 активируя его S-протеин. Вирусы могут прикрепляться к рецептору DC-SIGN (CD209) на поверхности дендритных клеток и они превращаются в "разносчиков" вируса по организму. Поражаются альвеолярные клетки легких, эндотелий, миокарда, почек, кишечника, и других органов, лейкоциты с развитием синдрома диссеминированного внутрисосудистого свёртывания (ДВС). Изменение обоняния (аносмия) у больных на ранней стадии заболевания может свидетельствовать как о поражении ЦНС вирусом, проникающим через обонятельный нерв, так и о вирусном поражении клеток слизистой носа.
Особенность иммунного ответа: IgM против белка N вируса SARS-CoV-2 выявляются у пациентов уже на 7-е сутки заболевания, IgG против этого же антигена - после 7-х суток и их уровень возрастает к 10-м суткам У пациентов повышается уровень провоспалительных цитокинов. Такая картина указывает на развитие в ходе инфекции "цитокинового шторма". В свою очередь SARS-CoV-2 подавляют интерфероновый ответ.
Клинические особенности. Инкубационный период составляет от 2 до 14 суток, в среднем 5-7 суток.
Для COVID-19 характерно наличие клинических симптомов ОРВИ: лихорадка, кашель сухой или с небольшим количеством мокроты в 80% случаев; одышка утомляемость ощущение заложенности в грудной клетке миалгия головные боли диарея спутанность сознания Также могут отмечаться боли в горле, насморк, снижение обоняния и вкуса, признаки конъюнктивита, сердцебиение, тошнота, рвота, наличие сыпи на коже. В среднем у 50% инфицированных заболевание протекает бессимптомно, при наличии клинических симптомов инфекция протекает в лёгкой форме у 80% пациентов. Осложнения тяжёлых форм – пневмония, сепсис, септический шок, острый респираторный дистресс-синдром (ОРДС), тромбозы, тромбоэмболии. Общая смертность составляет 2,3%. Сопутствующие хронические заболевания повышают вероятность неблагоприятного исхода (сахарный диабет, гипертоническая болезнь и др.).
Лабораторная диагностика коронавирусной инфекции. Основным видом биоматериала для лабораторного исследования на РНК-SARS-COV-2 является мазок из носоглотки (их двух носовых ходов) и ротоглотки в одну пробирку для большей концентрации вируса. При признаках заболевания нижних дыхательных путей в случае получения отрицательного результата в мазках со слизистой носо– и ротоглотки дополнительно исследуется мокрота или промывные воды бронхов, полученные при фибробронхоскопии (бронхоальвеолярный лаваж), трахеальный и назофариальный аспират. У интубированных пациентов, находящихся на ИВЛ (искусственная вентиляция лёгких), получают и исследуют аспират содержимого трахеи.
В качестве дополнительного материала для исследования могут использоваться биопсийный или аутопсийный материал легких, цельная кровь, сыворотка, фекалии.
