
- •1. Кровь, её функции. Основные физико-химические константы крови в норме и при патологии.
- •2. Белки плазмы крови, классификация, методы разделения.
- •3.Основные небелковые компоненты крови. Остаточный азот, его состав.
- •4.Принципы организации и механизмы регуляции кос.
- •5. Виды, причины и механизм развития алкалоза и ацидоза.
- •6. Эритроциты. Общая характеристика, строение, особенности метаболизма.
- •8. Биосинтез гема. Реакции, ферменты, локализация, регуляция и биологическая роль. Порфирии
- •9. Распад Hb в клетках рэс.
- •10. Метаболизм Fe
- •11. Особенности метаболизма лейкоцитов.
- •12. Особ метаболизма тромбоцитов, роль в гемостазе.
- •13. Механизм и стадии образования мочи.
- •Петля Генле обеспечивает реабсорбцию воды и солей
- •Реабсорбция кальция происходит в дистальном отделе
- •Конечный отдел нефрона определяет объем мочи
- •14. Органические и неорганические компоненты мочи норме/пат.
- •Калий Нормальные величины
- •Нормальные величины
- •Клинико диагностическое значение
- •Хлориды
- •Нормальные величины
- •Клинико диагностическое значение
- •Бикарбонаты
- •Нормальные величины
- •Клинико диагностическое значение
- •Фосфаты
- •Нормальные величины
- •Клинико диагностическое значение
- •Органические компоненты мочи Мочевина
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Креатинин
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Креатин
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Мочевая кислота
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Гиппуровая кислота
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Органические кислоты
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Пигменты
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Глюкоза
- •Нормальные величины
- •Клинико‑диагностическое значение
- •15. Нарушение процессов фильтрации, реабсорбции, секреции.
- •Лабораторная оценка реабсорбции Проксимальный каналец
- •Дистальный каналец
- •16. Гомеостатическая функция почек.
- •17. Особенность обмена белков и аминокислот в почках:
- •19. Функции печени. Особенности метаболизма гепатоцитов
- •20. Роль печени в углеводном обмене
- •21. Роль печени в липидном обмене
- •22.Роль печени в азотистом обмене.
- •24. Роль печени в регуляции кос, гормон гомеостаза и уровня бав.
- •I фаза метаболизма ксенобиотиков
- •Восстановление нитросоединений
- •II фаза метаболизма ксенобиотиков
- •25. Струк-функц и метабол характеристика мышечных волокон
- •26. Характеристика белков мышечной ткани
- •27. Роль мышечной ткани в межорганном обмене субстратами
- •28. Особенности метаболизма миокарда
- •30. Общая характеристика метаболизма нервной системы.
- •31. Нейромедиаторы, их характеристика и метаболизм
- •33. Биохим механизмы действ на мозг алк, нарк и токс соед.
- •34. Характеристика волокнистых структур ст.
- •35.Схема биосинтеза гликозамингликанов, их функциональная роль.
- •36.Костная и хрящевая ткань, хим сост и особ метаболизма.
- •37. Изменение ст при старении, коллагенозах, заживлении ран.
- •38.Механизмы канцерогенеза.
- •39. Биохимия легочной ткани. Причины и биохимические механизмы развития эмфиземы легких.
27. Роль мышечной ткани в межорганном обмене субстратами
Цикл Кори — совокупность биохимических ферментативных процессов транспорта лактата из мышц в печень, и дальнейшего синтеза глюкозы из лактата, катализируемое ферментами глюконеогенеза.
При интенсивной мышечной работе глюкоза вступает на путь анаэробного гликолиза с образованием лактата.
Лактат не может далее окисляться, он накапливается (при его накоплении в мышцах раздражаются чувствительные нервные окончания, что вызывает характерную ломоту в мышцах). С током крови лактат поступает в печень. Печень является основным местом скопления ферментов глюконеогенеза (синтез глюкозы из неуглеводных соеднений), и лактат идет на синтез глюкозы.
Креатин подвергается фосфорилированию с образованием креатин-фосфата, который после дефосфорилирования (необратимая реакция) превращается в креатинин, выделяющийся с мочой.

Синтез креатина в тканях человека протекает в две стадии. На первой стадии в почках образуется гуанидинацетат:

На второй стадии в печени происходит реакция трансметилирования:

Синтезированный в печени креатин поступает в кровь и доставляется в мышцы. Там он взаимодействует с АТФ, в результате чего образуется макроэргическое соединение креатинфосфат. Эта реакция легко обратима.

В состоянии покоя мышцы накапливают креатинфосфат (его содержание в неработающей мышце в 3-8 раз выше, чем содержание АТФ). При переходе к мышечной работе изменяется направление реакции и образуется АТФ, необходимый для мышечного сокращения.
Образование АТФ при участии креатинфосфата – наиболее быстрый путь генерации АТФ. Запас креатинфосфата обеспечивает интенсивную работу мышц в течение 2 – 5 секунд. За это время человек успевает пробежать 15 – 50 метров. Тем временем включаются другие механизмы образования АТФ: мобилизация мышечного гликогена, окисление субстратов, поступающих из печени и жировой ткани.
Концентрация креатина в крови здоровых взрослых людей составляет приблизительно 50 мкмоль/л; в моче он практически отсутствует. Появление креатина в моче не всегда является симптомом заболевания. Так, у маленьких детей и подростков моча всегда содержит креатин (физиологическая креатинурия). При заболеваниях мышц, когда нарушается образование креатинфосфата, увеличивается содержание креатина в крови и возрастает его экскреция с мочой.
В результате неферментативного дефосфорилирования креатинфосфата образуется креатинин – ангидрид креатина.

Креатинин – один из конечных продуктов азотистого обмена в организме, он выводится с мочой. Суточное выделение креатинина у здорового человека пропорционально его мышечной массе. Креатинин не реабсорбируется в почечных канальцах, поэтому его суточная экскреция является показателем фильтрационной функции почек. Содержание креатинина в крови снижается при заболеваниях мышц и увеличивается при нарушении функции почек. Выделение креатинина с мочой снижается в обоих случаях.
28. Особенности метаболизма миокарда
по структуре и свойствам похож на красные скелетные мышцы;
строго аэробный характер обмена и очень чувствителен к недостатку и О2, и энергии; основные источники энергии (топливо):
-
70% – ЖК и КТ;
-
30% – углеводы и продукты их распада.
Механизм развития сердечной недостаточности.
Нарушение энергетического метаболизма.
Дефицит O2 (ишемия, гипоксия, аноксия)
Несоответствие нагрузкифункциональной возможности миокарда
Дефицит субстратов (Гл, ЖК, КТ, лактат, ПВК и др.)
В саркоплазме накапливается Ca2+
Митохондрии аккумулируют значительную часть Ca2+
Разобщение дыхания и фосфорилирования:
Поступление кальция в митохондрии снижает мембранный потенциал, что приводит к дефициту энергии. Образуется гидроксиапатит, плохо растворимое соединение, уменьшается резерв фосфата.
В миокарде формируется кислородный голод.
Последовательность развития сердечной недостаточности (СН):
Слабая мышечная стенка растягивается (дилатация).
Повышается синтез коллагена рубцевание миокарда препятствует дилатации снижается эластичность.
Ca2+ ↑ анаэробный гликолиз ↑образование волокон белого типа гипертрофия миокарда усиление биосинтеза мышечных белков.
Ca2+ активирует процессы перекисного окисления (↑ NADH).
Биохимические основы коррекции сердечной недостаточности.
1. Аэрация миокарда - нормализация кровообращения;
2. Нормализация ионного и энергетического баланс:
а) Препараты K+ (печеный картофель, изюм, урюк и т.п.);
б) Инъекции препаратов глюкозы, инсулина и K+.
3. Сердечные гликозиды (СГ) (наперстянки, ландыша, строфанта Комбе) – дигитоксин, дигоксин, дигонин, конваллятоксин, строфантин K, коргликон.
4. Высокоспецифичные ингибиторы Na+/K+-АТФазы.
5. Применение ингибиторов кальциевых каналов и антагонистов Ca2+
- способствуют снижению концентрации ионов кальция.
6. Препараты, увеличивающие уровень АТФ в миокарде: Рибоксин, аспаркам, панангин, L-Карнитин.
7. Антиоксиданты (комплекс витаминов C, A, E)
8. Бетаин:
Синтез
холина в печени – нормализация
липопротеидного обмена.
29. Ограничение двигательной активности (гипокинезия). Гипокинезия – существенное ограничение двигательной активности.
Последствия гипокинезии сказываются практически на всех органах – гипокинетический синдром (ГКС).
Схема развития гипокинетического синдрома:
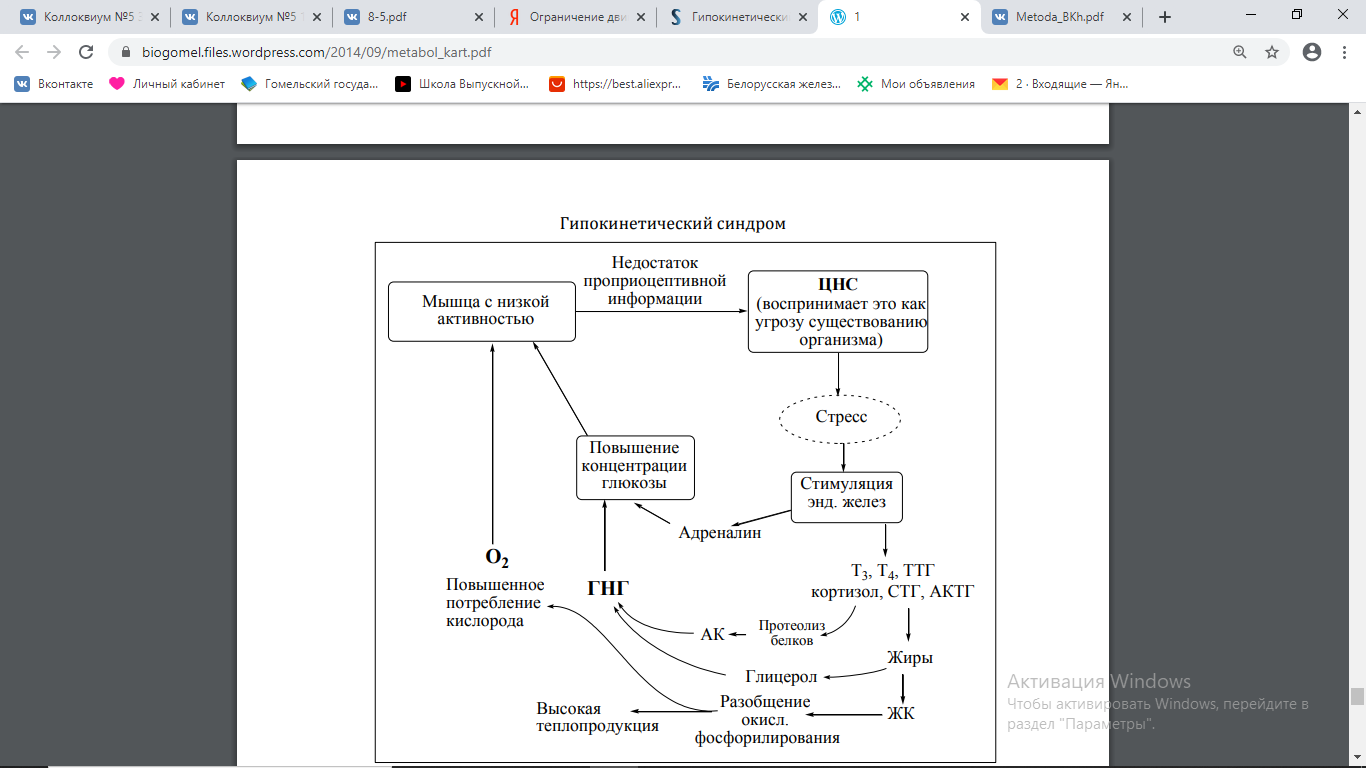
Патогенез ГКС (1-й этап):
-
Дефицит проприоцептивной информации
-
Стресс (как реакция организма на недостаток проприоцептивной информации)
-
Эффекты континсулярных гормонов: катехоламинов, T3, T4, глюкокортикоидов и др.
-
Активация протеолиза, липолиза, ГНГ
-
Увеличение концентрации ЖК в крови
-
Разобщение окисления и фосфорилирования
-
Усиление катаболических процессов в организме
-
Увеличение теплопродукции
Патогенез ГКС (2-й этап):
-
Увеличение потребления кислорода (гипокинетический парадокс)
-
Снижение массы мышечной ткани
-
протеолиз
-
Резорбция костной ткани, остеопороз, ухудшение минерального обмена.
-
снижение физ. нагрузки
-
Потеря с мочой электролитов Na+, K+,Ca2+
-
Как следствие уменьшения количества клеток
-
Увеличение частоты спонтанных мутаций
Гипокинетический синдром– диссипативный процесс, вызывающий распад структуры и превращающий ее в тепло, рассеивающееся в окружающей среде. У человека он ассоциирован с развитием 35 групп заболеваний (ожирение, сахарный диабет, атеросклероз, гипертензия и т.д.).
