
- •1. Кровь, её функции. Основные физико-химические константы крови в норме и при патологии.
- •2. Белки плазмы крови, классификация, методы разделения.
- •3.Основные небелковые компоненты крови. Остаточный азот, его состав.
- •4.Принципы организации и механизмы регуляции кос.
- •5. Виды, причины и механизм развития алкалоза и ацидоза.
- •6. Эритроциты. Общая характеристика, строение, особенности метаболизма.
- •8. Биосинтез гема. Реакции, ферменты, локализация, регуляция и биологическая роль. Порфирии
- •9. Распад Hb в клетках рэс.
- •10. Метаболизм Fe
- •11. Особенности метаболизма лейкоцитов.
- •12. Особ метаболизма тромбоцитов, роль в гемостазе.
- •13. Механизм и стадии образования мочи.
- •Петля Генле обеспечивает реабсорбцию воды и солей
- •Реабсорбция кальция происходит в дистальном отделе
- •Конечный отдел нефрона определяет объем мочи
- •14. Органические и неорганические компоненты мочи норме/пат.
- •Калий Нормальные величины
- •Нормальные величины
- •Клинико диагностическое значение
- •Хлориды
- •Нормальные величины
- •Клинико диагностическое значение
- •Бикарбонаты
- •Нормальные величины
- •Клинико диагностическое значение
- •Фосфаты
- •Нормальные величины
- •Клинико диагностическое значение
- •Органические компоненты мочи Мочевина
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Креатинин
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Креатин
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Мочевая кислота
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Гиппуровая кислота
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Органические кислоты
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Пигменты
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Нормальные величины
- •Клинико‑диагностическое значение
- •Глюкоза
- •Нормальные величины
- •Клинико‑диагностическое значение
- •15. Нарушение процессов фильтрации, реабсорбции, секреции.
- •Лабораторная оценка реабсорбции Проксимальный каналец
- •Дистальный каналец
- •16. Гомеостатическая функция почек.
- •17. Особенность обмена белков и аминокислот в почках:
- •19. Функции печени. Особенности метаболизма гепатоцитов
- •20. Роль печени в углеводном обмене
- •21. Роль печени в липидном обмене
- •22.Роль печени в азотистом обмене.
- •24. Роль печени в регуляции кос, гормон гомеостаза и уровня бав.
- •I фаза метаболизма ксенобиотиков
- •Восстановление нитросоединений
- •II фаза метаболизма ксенобиотиков
- •25. Струк-функц и метабол характеристика мышечных волокон
- •26. Характеристика белков мышечной ткани
- •27. Роль мышечной ткани в межорганном обмене субстратами
- •28. Особенности метаболизма миокарда
- •30. Общая характеристика метаболизма нервной системы.
- •31. Нейромедиаторы, их характеристика и метаболизм
- •33. Биохим механизмы действ на мозг алк, нарк и токс соед.
- •34. Характеристика волокнистых структур ст.
- •35.Схема биосинтеза гликозамингликанов, их функциональная роль.
- •36.Костная и хрящевая ткань, хим сост и особ метаболизма.
- •37. Изменение ст при старении, коллагенозах, заживлении ран.
- •38.Механизмы канцерогенеза.
- •39. Биохимия легочной ткани. Причины и биохимические механизмы развития эмфиземы легких.
-
Восстановление нитросоединений

б) восстановление азосоединений

II фаза метаболизма ксенобиотиков
Реакции II фазы (синтетические реакции) — конъюгации. В результате реакций II фазы происходит присоединение к веществу или его метаболитам химических группировок или молекул эндогенных соединений, при этом образуются полярные, хорошо растворимые в воде конъюгаты, легко выводимые через почки или с жёлчью.
Основные виды коньюгации: глюкуронирование, ацетилирование, метилирование, сульфатирование и водная конъюгация (гидратация). Все ферменты, функционирующие во II фазе обезвреживания ксенобиотиков, относят к классу трансфераз. Они характеризуются широкой субстратной специфичностью.
Глюкуронированию подвергаются природные соединения (билирубин, стероидные гормоны) и ксенобиотики (токоферолы, спирты, морфин, парацетамол). В реакции вступают субстраты, содержащие гидроксильные, карбоксильные, карбамоильные, тиоловые, карбонильные и нитрогруппы. Ферменты УДФ-глюкуронилтрансферазы, локализованы в эндоплазматической сети клеток печени, в меньшей степени в почках, пищеварительном тракте, коже.
Ацетильная коньюгация происходит в печени, слизистой кишечника и в ретикулоэндотелиальных клетках селезенки и легких. Субстраты ацетилирования — JIC и метаболиты, содержащие амино или нитрогруппу (серотонин, гистамин, изониазид, сульфаниламиды).
Сульфатной коньюгации подвергаются эндогенные токсические продукты гниения белков в кишечнике (индол, скатол, фенол), а также стеройды, токоферолы, нафтохиноны и ксенобиотики (тербуталин, пероральные контрацептивы). Как правило, это циклические соединения, имеющие свободные гидроксильные или аминные группы. Происходит в основном в печени.
Метильная коньюгация. Процесс наиболее интенсивен в печени. Метильной коньюгации подвергаются фенолы, амины, тиолоыве соединения (пиридин, никотинат, унитиол, кокаин).
Коньюгации с глутатионом подвергаются алифатические и ароматические соединения. Протекает в печени и почках. Глутатионтрансферазы представляют собой большое семейство как растворимых, так и мембранносвязанных белков и являются основными обезвреживающими ферментами печени. Взаимодействуют с глутатионом метаболиты парацетамола, хлороформа, алкены, эпоксиды.
В большинстве случаев в результате реакций II фазы ксенобиотики полностью утрачивают биологическую активность. Однако иногда отмечают образование активных метаболитов (морфин-6-глюкуронид) и даже канцерогенов (N-ацетилбензидин глюкуронид) в процессе реакций конъюгации.
Конъюгация может быть единственным путем превращения веществ, либо она следует за предшествующей ей метаболической трансформацией.
25. Струк-функц и метабол характеристика мышечных волокон
Типы мышечных волокон
|
красные мышцы |
белые мышцы |
|
аэробные |
анаэробные |
|
медленные |
быстрые |
|
много миоглобина и мтх |
мало миоглобина и мтх |
|
мало миофибриллярных белков |
много миофибриллярных белков |
Мышечная ткань использует разные субстраты метаболизма: глюкозу, жирные кислоты, кетоновые тела.
Скелетные мышцы различаются по энергозатратам в зависимости от активности.
В покоящейся мышце главным энергетическим субстратом являются жирные кислоты, при физической активности главным субстратом становится глюкоза, для этого необходим запас гликогена в мышцах.
В скелетных мышцах хранится около 75% всего гликогена организма, в печени – 25%. Глюкоза не может выйти из мышц, так там отсутствует фермент Г6Ф-аза.
При физической нагрузке скорость анаэробного гликолиза в мышце выше, чем ЦТК, поэтому лактат накапливается и выходит из клеток.
Другой продукт метаболизма – Ала – образуется при переаминировании ПВК.
Лактат и Ала транспортируются с кровотоком в печень, где снова превращаются в глюкозу (ГНГ).
Мышечные белки тоже могут использоваться для энергообеспечения, однако этот процесс не выгоден энергетически и опасен для здоровья. По этой причине катаболизм мышечных белков в норме минимален и усиливается при длительном голодании.
Дополнительный энергетический резерв – креатинфосфат, он быстро расходуется в начальном периоде физической нагрузки и должен восполняться в период покоя.
Энергетический метаболизм мышц
При интенсивной мышечной работе: АТФ4- → АДФ3- + Фн2- + H+
актомиозин проявляет свойства АТФ-азы;
Закислению препятствуют буферные дипептиды ансерин и карнозин, содержащие гистидин.
Скорость гидролиза АТФ превышает скорость его синтеза.
АДФ накапливается, но не используется ни в каких реакциях, кроме аденилаткиназной:
2 АДФ ↔ АТФ + АМФ (миоаденилаткиназа)
В ходе аденилаткиназной реакции накапливается АМФ. Снижает его концентрацию фермент АМФ-дезаминаза:
АМФ → ИМФ + NH3
Дополнительный энергетический резерв – креатинфосфат, он быстро расходуется в начальном периоде физической нагрузки и должен восполняться в период покоя.
ЦИКЛ ПУРИНОВЫХ НУКЛЕОТИДОВ
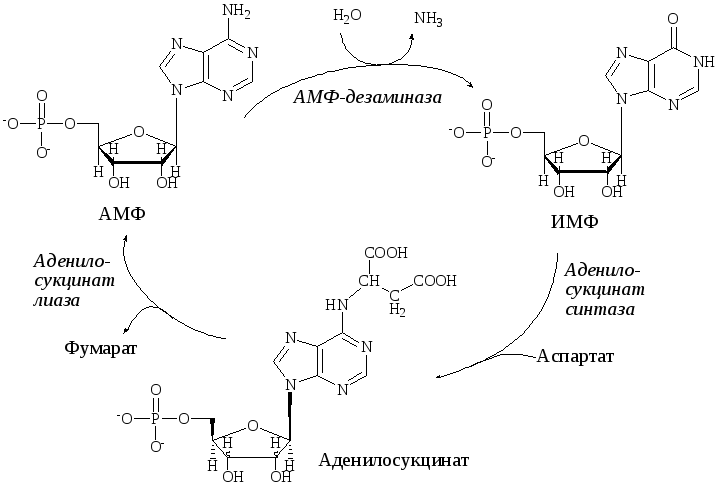
1. Самым важным резервом энергии в мышцах является гликоген. Расщепление гликогена в мышцах находитс под гормональным влиянием. Адреналин активирует расщепление гликолиза через АЦ-механизм. Увеличение концентрации кальция во время мышечного сокращения также приводит к активации гликогенфосфорилазы.
Глюкоза, которая освобождается из гликогена, фосфорилируется и расходуется на синтез АТФ. Это обеспечивает процессы гликолиза и окислительного фосфорилирования.
2. При первых нескольких секундах мышечной работы запускается самый быстрый процесс получения АТФ – расщепление креатинфосфата с помощью креатинкиназы.
3. Непродолжительным периодом поддержания АТФ является аденилаткиназа (миокиназа). Фермента катализирует образование АТФ и АМФ из 2ух молекул АДФ.
4. Среди всех процессов самым эффективным является оксилительное фосфорилирование. Именно оно и обеспечивает потребность сердечной мышцы в АТФ для постоянной работы. Но здесь требуется очень много кислорода. И в мышцах, зависимых от кислорода, присутствует миоглобин.
В мышцах, где потребности в АТФ покрываются и гликолизом, миоглобина НЕТ. Это белые мышечные волокна. В них очень много гликогена.
