
- •Федеральное агентство по образованию
- •Пищевые добавки и ароматизаторы Физико-химические и функционально-технологические свойства
- •Введение
- •1. Функциональные классы пищевых добавок
- •2. Терминология пищевых добавок и ароматизаторов, принятая в рф
- •3. Правовое регулирование производства и обращения пищевых добавок и ароматизаторов
- •Директивы, принятые ес по пищевым добавкам
- •Директивы, принятые по критериям чистоты пищевых добавок
- •Законодательство ес по ароматизаторам
- •Законодательство ес в области безопасности консервантов
- •Законодательство ес в области безопасности антиоксидантов
- •Документы, регламентирующие применение пищевых добавок в рф
- •4. Система подтверждения безопасности пищевых добавок и ингредиентов
- •Пищевые добавки, запрещенные в рф к применению при производстве пищевых продуктов
- •5. Методы оценки органолептических характеристик пищевых добавок и ароматизаторов
- •5.1. Различительные методы
- •5.2. Методы с использованием шкал и категорий
- •5.3. Описательные методы
- •6. Пищевые добавки, влияющие на вкус и аромат пищевого продукта
- •6.1. Пищевые ароматизаторы
- •6.1.1. Сырье для получения ароматизаторов
- •6.1.2. Компонентный состав и технология ароматизаторов
- •Физико-химические показатели растворителей
- •Рецептуры фруктовых ароматизаторов ( е.В. Смирнов, 2006 г.)
- •6.1.3. Применение и дозировки ароматизаторов
- •6.2. Подсластители и сахарозаменители
- •Относительная сладость подсластителей
- •6.2.1. Интенсивные подсластители
- •6.2.2. Объемные сахарозаменители
- •6.2.3. Смесевые подсластители
- •6.2.4. Особенности применения заменителей сахара в производстве пищевых продуктов
- •Максимальные концентрации подсластителей, используемых в некоторых пищевых продуктах, мг/кг (а.П. Нечаев и др., 2002 г.; л.А. Сарафанова, 1997 г.)
- •Генотоксичность подсластителей (а.Д. Дурнев, 2007 г.)
- •6.3. Пищевые кислоты и регуляторы кислотности пищевых систем
- •6.3.1. Пищевые органические кислоты
- •Наличие органических кислот в различных фруктах и ягодах
- •Основные свойства пищевых кислот
- •Сравнительная оценка бактерицидного действия уксусной, молочной и лимонной кислот при 20 ºС в течение 15 мин
- •Характеристики пищевых кислот, используемых в кондитерском производстве
- •Свойства винных кислот
- •Растворимость виннокаменной кислоты в воде в зависимости от температуры
- •Константы диссоциации и пороговые концентрации чувствительности пищевых кислот
- •6.3.2. Соли пищевых кислот
- •Содержание цитратов в пищевых продуктах
- •Кислотность водных растворов фосфатов
- •6.4. Усилители вкуса и аромата пищевой продукции
- •Усилители вкуса и аромата, разрешенные к применению в рф
- •7. Пищевые добавки, улучшающие внешний вид пищевых продуктов
- •7.1. Пищевые красители
- •Пищевые красители, разрешенные к применению в рф в производстве пищевых продуктов (по данным СанПин 2.3.2.2364–08)
- •7.1.1. Натуральные красители
- •Стойкость основных натуральных красителей (по л.А. Сарафановой, 2004 г.)
- •7.1.2. Синтетические красители
- •Цветовая гамма синтетических красителей, разрешенных к применению в рф в производстве пищевых продуктов
- •Свойства синтетических красителей
- •Свойства азокрасителей
- •Гигиенические регламенты применения синтетических красителей (СанПиН 22.3.2.1293–03)
- •7.1.3. Минеральные (неорганические) красители
- •Минеральные (неорганические) красители, разрешенные к применению в рф в производстве пищевых продуктов
- •7.2. Применение пищевых красителей в производстве пищевых продуктов
- •Рецептуры смесевых красителей (л.А. Сарафанова, 2008 г.)
- •8. Пищевые добавки, увеличивающие срок годности пищевой продукции
- •8.1. Консерванты для пищевой промышленности
- •Список консервантов, разрешенных в рф для применения в пищевых продуктах
- •Эффективность некоторых консервантов по отношению к микроорганизмам (э. Люк, м. Ягер, 2003 г.)
- •8.1.1. Индивидуальные консерванты
- •Растворимость сорбиновой кислоты и сорбата калия в зависимости от вкусовых веществ
- •Действие сорбиновой кислоты на микроорганизмы (э. Люк, м. Ягер, 2003 г.)
- •Действие бензойной кислоты на микроорганизмы (э. Люк, м. Ягер, 2003 г.)
- •Действие парабенов на микроорганизмы (э. Люк, м. Ягер, 2003 г.)
- •Действие муравьиной кислоты на микроорганизмы (э. Люк, м. Ягер, 2003 г.)
- •Характеристики сернистого газа и его производных
- •Действие сернистой кислоты на микроорганизмы (э. Люк, м. Ягер, 2003 г.)
- •Действие нитрита на бактерии (э. Люк, м. Ягер, 2003 г.)
- •8.1.2. Смесевые консерванты и эффект синергизма
- •8.1.3. Факторы, влияющие на эффективность действия консервантов
- •Доля недиссоциированных молекул для консервантов (кислот) при различных значениях рН (э. Люк, м. Ягер, 2003 г.)
- •Пороговые значения активности воды для некоторых микроорганизмов, встречающихся в пищевых продуктах
- •8.2. Антиокислители и их синергисты
- •Антиокислители, разрешенные к применению в рф
- •Содержание токоферола в некоторых жирах, маслах и жиросодержащих продуктах
- •8.3. Пищевые добавки, способствующие повышению сроков годности пищевых продуктов
- •Список литературы
- •Содержание
Свойства винных кислот
|
Наименование кислоты
|
tпл, ºС |
Растворимость в воде при 20 ºС, г/100 г |
Константы кислотности |
|
|
рК1 |
рК2 |
|||
|
D-винная |
170 |
139,4 |
2,93 |
4,23 |
|
L-винная |
170 |
139,4 |
2,93 |
4,23 |
|
Мезовинная |
140 |
125 |
3,11 |
4,80 |
|
Виноградная |
206 |
20,6 |
2,96 |
4,24 |
Нагревание безводной L(+)-винной кислоты до температуры выше 180 С приводит сначала к отщеплению от двух молекул кис-лоты одной молекулы воды и образованию двувинной-метавинной кислоты (Е 353). При отщеплении еще одной молекулы воды образуется ангидрид винной кислоты.
L-винная кислота хорошо растворима в воде (табл. 6.13) и водно-спиртовых растворах. Ее растворимость увеличивается с повышением температуры. Она кристаллизуется из водных растворов в виде бесцветных прозрачных косых ромбических или моноклиноэдрических призм с притупленными передними углами, не содержащих крис-таллизационной воды.
Таблица 6.13
Растворимость виннокаменной кислоты в воде в зависимости от температуры
|
Темпе- ратура, С
|
В 100 г воды растворяется винно- каменной кислоты, г |
Темпе- ратура, С
|
В 100 г воды растворяется винно- каменной кислоты, г |
Темпе- ратура, С
|
В 100 г воды растворяется винно- каменной кислоты, г |
|
0 |
115 |
35 |
165 |
70 |
244 |
|
5 |
120 |
40 |
176 |
75 |
258 |
|
10 |
126,7 |
45 |
185 |
80 |
273 |
|
15 |
133 |
50 |
195 |
85 |
290 |
|
20 |
139,4 |
55 |
206 |
90 |
307 |
|
25 |
148 |
60 |
218 |
95 |
325 |
|
30 |
156,2 |
65 |
230 |
100 |
343 |
Винная кислота и ее соли проявляют стойкость при хранении, только если они хорошо высушены. Во влажном состоянии и в раст-воре они разрушаются микроорганизмами.
Промышленное производство винной кислоты складывается из следующих основных процессов:
1) переработки всех видов сырья в винно-кислую известь, которую получают из отходов на заводах первичного виноделия: из дрожжевых осадков после сбраживания виноградного сока и выжи-мок после прессования мезги; винного камня, образующегося на стенках и днищах бочек, цистерн во время брожения сусла и выдержки вин, а также при упаривании виноградного сока в вакуум-аппаратах;
2) выделения из винно-кислой извести винной кислоты путем расщепления серной кислотой, отфильтровывания осадка, упаривания фильтрата, кристаллизации и центрифугирования неочищенных крис-таллов;
3) адсорбционной и химической очистки растворов винной кис-лоты;
4) упаривания очищенного раствора, кристаллизации, центрифугирования, сушки и упаковки готовой виннокаменной кислоты.
Все показатели качества винной кислоты регламентирует ГОСТ 21205–83.
В качестве подкислителя и регулятора кислотности винную кис-лоту применяют в производстве джемов, цитрусовых мармеладов, варенья, консервированных фруктов и овощей, томата-пасты, безалкогольных напитков, вин, фруктово-ягодного мороженого.
Особенность винной кислоты – очень малая гигроскопичность – обусловливает ее предпочтительность в производстве шипучих таблеток и быстрорастворимых порошкообразных напитков.
Для пищевой винной кислоты (Е 334) установлено допустимое суточное поступление на уровне 30 мг/кг массы тела в день.
Пищевая добавка Е 353 (метавинная кислота) также разрешена в России, но сфера ее применения весьма ограничена. В основном ее используют для снижения или исключения выпадения винного камня и помутнения вин (не более 100 мг/дм3 вина).
Яблочная кислота известна в двух оптически деятельных и одной рацемической формах. В природе распространена L(–)-яблочная кислота. Присутствие в натуральных соках D-яблочной кислоты рассматривается как его фальсификация.
Яблочная кислота может быть получена различными методами: синтетическим, методом извлечения из растительного сырья и микробиологическим. В основе химических методов лежат реакции присоединения воды к малеиновой и фумаровой кислотам, восстановления D,L-винной кислоты (виноградной кислоты), замена гидроксилом брома в D,L-бромянтарной кислоте. В этих случаях образуется рацемическая яблочная кислота. Яблочную кислоту и ее соли можно выделить из листьев хлопчатника и отходов хлопкоочистительной промышленности, плодов рябины и барбариса. Микробный синтез яблочной кислоты осуществляют с помощью иммобилизованных на силикагеле клеток микроорганизмов Brevibacterium ammoniag в колонне с фиксирующим слоем.
В промышленном масштабе рацемическую кислоту (пищевую добавку Е 296) получают синтетическим путем из малеиновой кислоты. Она представляет собой белый кристаллический порошок, мало гигроскопичный, с температурой плавления 130–132 С, хорошо растворимый в холодной воде и нерастворимый в жиросодержащих растворителях.
Яблочная кислота относится к разрешенным в России пищевым подкислителям. Допустимое суточное поступление для нее не ограничено.
Как подкислитель яблочная кислота имеет сильный кислый вкус с небольшим оттенком вкуса недозрелых плодов, поэтому в рецептуры пищевых изделий ее вносят в значительно меньших количествах (на 10–20 %), чем лимонную.
Область применения яблочной кислоты: кондитерские изделия, фруктовые консервы, безалкогольные напитки.
Фумаровая кислота яляется ненасыщенной двухосновной кис-лотой. В природе она встречается в сорном растении дымянке и во многих грибах. Промышленный способ получения фумаровой кисло-ты основан на каталитической изомеризации малеиновой кислоты.
Фумаровая кислота – белое кристаллическое вещество, которое, не плавясь, возгоняется при 200 С; в запаянном капилляре имеет температуру плавления 287–288 С. Фумаровая кислота имеет низкие степень растворимости и скорость растворения в воде: 7 г/дм3 при 20 С. Хорошо растворима в спиртах.
Фумаровая кислота как пищевая добавка разрешена к примене-нию в пищевой промышленности России, но ввиду токсичности имеет ограничения. Для нее допустимое суточное поступление установлено на уровне 6 мг/кг массы тела человека. Кроме того, причинами ограничения ее применения в качестве подкислителя являются и технологические факторы: плохие растворимость, смачиваемость и скорость растворения.
Обычно фумаровую кислоту используют в составе комплекс-ных пищевых добавок, предназначенных для производства конди-терских изделий (карамели, мармелада), безалкогольных напитков, а также для подкисления теста, в сухих смесях для гелеобразных продуктов и десертов.
Янтарная кислота также является двухосновной предельной кислотой. Представляет собой белый кристаллический порошок с температурой плавления 182,8 С, хорошо растворимый в горячей воде (1:1), хуже – в холодной и спирте. Имеет незначительный солоновато-горький привкус. В природе янтарная кислота содержится во многих растениях: водорослях, грибах, лишайниках. Может быть выделена из янтаря путем сухой перегонки. В промышленности янтарную кислоту получают гидрированием малеиновой кислоты.
Янтарная кислота является подкислителем, разрешенным к применению в РФ. Допустимое суточное поступление для нее не определено.
Применяют янтарную кислоту в производстве порошкообразных продуктов длительного хранения. В определенной степени янтарная кислота стабилизирует цвет и усиливает вкус рыбы.
Адипиновая кислота является двухосновной предельной кислотой. Представляет собой белое кристаллическое вещество с темпера-турой плавления 153 С. Характеризуется низкой растворимостью в спирте и средней – в воде (15 г/дм3 при 20 С). Адипиновую кислоту получают окислением циклогексана (или циклогексанола, или циклогексанона) азотной кислотой. Производство адипиновой кислоты пищевого назначения незначительно, так же как и потребление. Допустимое суточное поступление – 5 мг/кг массы тела в день в пересчете на адипат-ион.
Сфера применения: производство жевательной резинки, порошкообразных смесей напитков, смесей для выпечки.
Ортофосфорная кислота (синоним – фосфорная кислота) пред-ставляет собой прозрачную вязкую жидкость без запаха с температурой плавления 42,35 С и температурой разложения 150 С, смешивается с водой и этанолом.
Получают ортофосфорную кислоту химическим синтезом из природного сырья – фосфатов (ГОСТ 10678–76Е, марка А, пищевая). Разрешена к применению в РФ, но допустимая суточная доза фосфорной кислоты в составе пищевых продуктов ограничена – не более 15 мг/кг массы тела, так как избыточное количество может привести в организме человека к нарушениям баланса фосфора и кальция.
В качестве подкислителя фосфорная кислота в основном используется в производстве безалкогольных напитков и плавленых сыров.
Пищевые кислоты обладают одной общей вкусовой характеристикой – кислым вкусом, но различаются по его интенсивности и вкусовым характеристикам во времени (рис. 6.6).
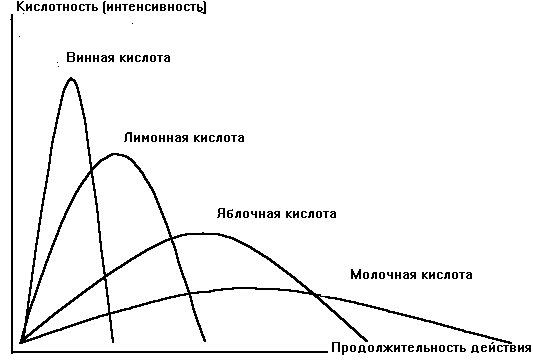
Рис. 6.6. Интенсивность и продолжительность действия кислого вкуса пищевых кислот (Х. Хамелийинк, 1999 г.)
Кислый вкус пропорционален концентрации ионов Н+. Однако на ощущение кислого вкуса органических кислот влияет и анион, за счет чего возникают различные вкусовые ощущения. Если сравнивать вкусовые характеристики наиболее часто используемых пищевых кислот, то вкусовая характеристика молочной кислоты описывается как мягкая и длительная. Лимонная и винная кислоты дают быстрый кисловатый начальный импульс. Яблочная кислота по вкусовым характеристикам занимает промежуточное положение между молочной и лимонной кислотами. Вкус яблочной кислоты сохраняется дольше, чем лимонной, давая замедленную кислую ноту. Она обладает приятным кислым привкусом, который дополняет фруктовый аромат.
Интенсивность восприятия человеком кислого вкуса органиче-ских кислот зависит не только от титруемой кислотности, она также связана со степенью диссоциации пищевых кислот. В связи с этим различен порог ощущения пищевых кислот. В табл. 6.14 приведены данные константы диссоциации и порога чувствительности пищевых кислот.
Таблица 6.14
