
- •Сборник методических указаний к лабораторным работам
- •«Аналитическая химия»
- •Атомно-эмиссионная фотометрия пламени
- •Цель и задачи работы
- •Оборудование и реактивы
- •Программа работы
- •Определение калия по методу градуировочного графика
- •Приготовление стандартных растворов:
- •Подготовка прибора к работе:
- •Построение градуировочного графика
- •1. Цель и задачи работы.
- •Определение содержания натрия в анализируемом растворе.
- •1. Цель и задачи работы.
- •Определения содержания кальция в анализируемом растворе.
- •1. Цель и задачи работы.
- •Вопросы для самоконтроля
- •Сущность и основы метода ик-спектроскопии
- •Фурье спектрометр фсм 1201
- •Фотометрический анализ
- •Цель и задачи работы
- •Оборудование и реактивы
- •Определение концентрации ионов меди(II) в водных растворах дифференциальным методом и методом градуировочного графика
- •Приготовление стандартных растворов:
- •Приготовление раствора сравнения.
- •Выбор светофильтра
- •Определение меди(II) по методу градуировочного графика.
- •Определение меди(II) дифференциальным методом.
- •Определение титана (IV) методом градуировочного графика
- •Приготовление стандартных растворов:
- •Приготовление раствора сравнения
- •Определение титана (IV) по методу градуировочного графика
- •Определение фосфора в виде синего фосфорномолибденового комплекса методом градуировочного графика
- •Приготовление стандартных растворов:
- •Приготовление раствора сравнения
- •Выбор светофильтра
- •Определение фосфора по методу градуировочного графика
- •Определение фосфора в виде фосфорномолибденованадиевой гетерополикислоты
- •Приготовление стандартных растворов
- •Приготовление раствора сравнения
- •Выбор светофильтра
- •Определение фосфат-ионов по методу градуировочного графика
- •Определение нитрит-ионов по методу градуировочного графика
- •Оформление лабораторного журнала.
- •Определение меди(II) в водных растворах методом градуировочного графика и дифференциальным методом.
- •1. Цель и задачи работы.
- •Определение железа (III) в водных растворах методом градуировочного графика.
- •1. Цель и задачи работы.
- •3.4. Определение железа (III) в водных растворах методом градуировочного графика.
- •Определение титана (IV) методом градуировочного графика.
- •1. Цель и задачи работы.
- •3.3. Определение титана (IV) методом градуировочного графика.
- •Определение фосфора в виде синего фосфорномолибденового комплекса методом градуировочного графика
- •1. Цель и задачи работы.
- •3.4. Определение фосфора в водных растворах методом градуировочного графика.
- •Определение фосфора в виде фосфорномолибденованадиевой гетерополикислоты
- •1. Цель и задачи работы.
- •Определение нитрит-ионов методом градуировочного графика.
- •1. Цель и задачи работы.
- •3.5. Определение нитрит-ионов методом градуировочного графика.
- •Вопросы для самоконтроля
- •Фототурбидиметрия.
- •Цель и задачи работы
- •Оборудование и реактивы
- •Определение сульфатов в растворе
- •Приготовление стандартных растворов и раствора сравнения:
- •1. Цель и задачи работы.
- •Вопросы для самоконтроля
- •Рефрактометрия
- •Цель и задачи работы
- •Оборудование и реактивы
- •Программа работы
- •Рефрактометрическое определение сахара в молоке.
- •Подготовка пробы к анализу:
- •Порядок работы на рефрактометре:
- •Контрольная задача. Определение содержания сахара в анализируемом образце
- •Определение содержания хлорида натрия в водном растворе. Приборы и реактивы.
- •Приготовление стандартных растворов:
- •Построение градуировочного графика.
- •Контрольная задача. Определение содержания хлорида натрия в анализируемом растворе
- •Оформление лабораторного журнала
- •1.2. Оборудование и реактивы
- •1.3. Рефрактометрическое определение сахара в молоке
- •Вопросы для самоподготовки
- •Определение содержания глюкозы в анализируемом растворе по методу градуировочного графика.
- •Поляриметрическое определение сорбита в смеси.
- •Оформление лабораторного журнала
- •Определение глюкозы
- •Цель и задачи работы
- •Определение сорбита
- •1. Иономер-кондуктометр; 2. Магнитная мешалка; 3. Кондуктометрический датчик; 4. Ячейка; 5. Бюретка
- •Определение солесодержания вод скважин методом прямой кондуктометрии.
- •Определение качества очистки дистиллированной и бидистиллированной воды методом прямой кондуктометрии
- •Определение качества очистки дисстилированной воды.
- •Опредление качества очистки бидистиллированной воды
- •Определение слабой кислоты и соли слабого основания в их смеси методом кондуктометрического титрования
- •Определение слабой кислоты и соли слабого основания в их смеси.
- •Стандартизация раствора (вторичного стандарта) по первичном стандарту hCl
- •Контрольная задача. Определение содержания борной кислоты и солянокислого гидроксиламина в испытуемой смеси
- •Определение ионов и в их смеси методом кондуктометрического титрования
- •Определение сульфат-ионов методом кондуктометрического титрования
- •Оформление лабораторного журнала
- •Определение солесодержания вод скважин методом прямой кондуктометрии
- •1. Цель и задачи работы.
- •Определение качества очистки дистиллированной и бидистиллированной воды методом прямой кондуктометрии
- •1. Цель и задачи работы.
- •Определение слабой кислоты и соли слабого основания в их смеси методом кондуктометрического титрования
- •1. Цель и задачи работы
- •Определение ионов и в их смеси методом кондуктометрического титрования
- •Определение сульфат ионов методом кондуктометрического титрования
- •Вопросы для самоконтроля.
- •Потенциометрия
- •Цель и задачи работы
- •Оборудование и реактивы
- •1. Иономер универсальный Анион-4100. 2. Стеклянный электрод. 3. Хлорсеребряный электрод. 4.Ячейка. 5. Бюретка. 6. Магнитная мешалка.
- •Определение нитрат-ионов методом прямой потенциометрии методом градуировочного графика и методом добавок
- •Определение нитрат-ионов по методу градуировочного графика
- •Определение нитрат-ионов методом добавок
- •Определение хлороводородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования
- •Стандартизация раствора (вторичного стандарта) по первичном стандарту hCl
- •Контрольная задача. Определение содержания хлороводородной и уксусной кислот в анализируемом образце.
- •Определение фосфорной кислоты и дигидрофосфата натрия в растворе при их совместном присутствии методом потенциометрического титрования
- •Стандартизация раствора (вторичного стандарта) по первичном стандарту hCl
- •Контрольная задача. Определение содержания фосфорной кислоты и дигидрофосфата натрия в анализируемом образце.
- •Определение железа (II) в присутствии железа (III) методом потенциометрического титрования.
- •Приготовление модельного раствора
- •Определение содержания железа (II) в анализируемом растворе
- •Определение свинца (II) в растворе.
- •Контрольная задача. Определение свинца (II) в растворе.
- •Определение железа (III) в растворе
- •Определение железа (III) в растворе (рабочий электрод – платиновый)
- •Определение железа (III) в растворе (рабочий электрод – стеклянный)
- •Оформление лабораторного журнала
- •Определение нитрат-ионов методом прямой потенциометрии методом градуировочного графика и методом добавок
- •1. Цель и задачи работы.
- •Определение хлороводородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования
- •1. Цель и задачи работы
- •Определение фосфорной кислоты и дигидрофосфата натрия в растворе при их совместном присутствии методом потенциометрического титрования
- •1. Цель и задачи работы
- •Определение железа (II) в присутствии железа (III) методом потенциометрического титровании.
- •Определение железа (III) в растворе
- •Определение железа (III) в растворе ( рабочий электрод - платиновый)
- •Определение железа (III) в растворе (рабочий электрод - стеклянный)
- •Вопросы для самоподготовки.
- •Контрольная задача. Определение содержания тиосульфата натрия в анализируемом образце
- •Определение хлороводородной кислоты методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности
- •Оформление лабораторного журнала
- •Опредление тиосульфата натрия методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности
- •Определение хлороводородной кислоты методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности.
- •Вопросы для самоподготовки
-
Вопросы для самоподготовки
-
На чём основан рефрактометрический метод анализа?
-
Что называется относительным показателем преломления?
-
Что называется абсолютным показателем преломления?
-
От каких факторов зависит показатель преломления?
-
Что называется дисперсией света и как она влияет на показатель преломления?
-
Какой луч называется предельным?
-
На чём основано устройство рефрактометра?
-
Какое явление называется полным внутренним отражением и как оно используется в рефрактометре?
-
Какова оптическая схема рефрактометра?
-
Каковы пределы измерения показателя преломления на рефрактометрах?
-
Какова погрешность измерений (%) на рефрактометре?
-
Поляриметрия
-
Цель и задачи работы
-
Изучение работы поляриметра, овладение навыками практического применения поляриметрического метода анализа.
-
Оборудование и реактивы
-
Поляриметр СМ-3;
-
Рабочий раствор глюкозы ω(C6H12O6) = 20%;
-
Мерная пробирка вместимостью 10 см3 – 6 шт.
-
Рабочий раствор сорбита ω(C6H14O6) = 20%;
-
Молибдат аммония (NH4)6Mo7O24·4H2O криталлический, ч.д.а.;
-
Серная кислота, раствор С(1/2 H2SO4) = 0,5 моль/дм3.
-
Аналитические весы;
-
Мерные колбы вместимостью 100,0 см3 – 2 шт.;
-
Пипетка Мора 10,0 см3.
-
Поляриметрическое определение глюкозы
Поляриметрический метод анализа основан на зависимости угла вращения плоскости поляризации плоскополяризованного света от концентрации оптически активного вещества в растворе.
Для поляриметрических определений используют прозрачные растворы.
Ход работы:
-
Приготовление стандартных растворов глюкозы:
-
Разбавлением рабочего раствора глюкозы готовят серию стандартных растворов с содержанием глюкозы 3; 6; 9; 12 (%).
-
Необходимые объемы исходного раствора и воды находят графическим методом (креста). Например, для приготовления первого раствора:

т.е. на 3 весовых частей исходного раствора необходимо взять 17 весовых частей воды. Переходя к объемам и учитывая, что воды = 1 г/см3, находят объем исходного раствора (необходимый для приготовления 25 см3 первого стандартного раствора) из соотношения:


где
 - плотность исходного раствора (
- плотность исходного раствора ( ).
).
-
Определение содержания глюкозы в анализируемом растворе по методу градуировочного графика.
-
Построение градировочного графика
Каждый раствор вносят в кювету и измеряют угол вращения с помощью поляриметра 5-7 раз.
Результаты измерений вносят в таблицу 5.1.
Строят градуировочный график в координатах
 .
.
2. Контрольная задача
Анализируемую пробу довести до метки дистиллированной водой.
Контрольный раствор вносят в кювету и измеряют угол вращения с помощью поляриметра 5-7 раз.
Результаты измерений вносят в таблицу 5.1.
По графику находят
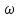 .
.
-
Поляриметрическое определение сорбита в смеси.
Методика основана на измерении оптической
активности сорбита с добавлением
молибдата аммония и без него. Удельное
вращение
 сорбита мало (-2,01°); в присутствии
молибдата аммония образуется комплексное
соединение, удельное вращение которого
+105,6°.
сорбита мало (-2,01°); в присутствии
молибдата аммония образуется комплексное
соединение, удельное вращение которого
+105,6°.
Ход работы:
2.2.1. Определение сорбита в контрольной пробе.
В мерную колбу вместимостью 100,0 см3 вносят с помощью пипетки по 10,0 см3 анализируемый раствор, объем раствора доводят до метки дистиллированной водой, перемешивают и измеряют угол вращения с помощью поляриметра 5-7 раз.
В другую мерную колбу вместимостью 100,0 см3 с помощью пипетки по 10,0 см3 вносят анализируемый раствор, прибавляют 1,000 г молибдата аммония и с помощью цилиндра по 25,0 см3 вносят раствор серной кислоты. После полного растворения молибдата аммония объем раствора доводят до метки дистиллированной водой и измеряют угол вращения с помощью поляриметра 5-7 раз.
