
- •Сборник методических указаний к лабораторным работам
- •«Аналитическая химия»
- •Атомно-эмиссионная фотометрия пламени
- •Цель и задачи работы
- •Оборудование и реактивы
- •Программа работы
- •Определение калия по методу градуировочного графика
- •Приготовление стандартных растворов:
- •Подготовка прибора к работе:
- •Построение градуировочного графика
- •1. Цель и задачи работы.
- •Определение содержания натрия в анализируемом растворе.
- •1. Цель и задачи работы.
- •Определения содержания кальция в анализируемом растворе.
- •1. Цель и задачи работы.
- •Вопросы для самоконтроля
- •Сущность и основы метода ик-спектроскопии
- •Фурье спектрометр фсм 1201
- •Фотометрический анализ
- •Цель и задачи работы
- •Оборудование и реактивы
- •Определение концентрации ионов меди(II) в водных растворах дифференциальным методом и методом градуировочного графика
- •Приготовление стандартных растворов:
- •Приготовление раствора сравнения.
- •Выбор светофильтра
- •Определение меди(II) по методу градуировочного графика.
- •Определение меди(II) дифференциальным методом.
- •Определение титана (IV) методом градуировочного графика
- •Приготовление стандартных растворов:
- •Приготовление раствора сравнения
- •Определение титана (IV) по методу градуировочного графика
- •Определение фосфора в виде синего фосфорномолибденового комплекса методом градуировочного графика
- •Приготовление стандартных растворов:
- •Приготовление раствора сравнения
- •Выбор светофильтра
- •Определение фосфора по методу градуировочного графика
- •Определение фосфора в виде фосфорномолибденованадиевой гетерополикислоты
- •Приготовление стандартных растворов
- •Приготовление раствора сравнения
- •Выбор светофильтра
- •Определение фосфат-ионов по методу градуировочного графика
- •Определение нитрит-ионов по методу градуировочного графика
- •Оформление лабораторного журнала.
- •Определение меди(II) в водных растворах методом градуировочного графика и дифференциальным методом.
- •1. Цель и задачи работы.
- •Определение железа (III) в водных растворах методом градуировочного графика.
- •1. Цель и задачи работы.
- •3.4. Определение железа (III) в водных растворах методом градуировочного графика.
- •Определение титана (IV) методом градуировочного графика.
- •1. Цель и задачи работы.
- •3.3. Определение титана (IV) методом градуировочного графика.
- •Определение фосфора в виде синего фосфорномолибденового комплекса методом градуировочного графика
- •1. Цель и задачи работы.
- •3.4. Определение фосфора в водных растворах методом градуировочного графика.
- •Определение фосфора в виде фосфорномолибденованадиевой гетерополикислоты
- •1. Цель и задачи работы.
- •Определение нитрит-ионов методом градуировочного графика.
- •1. Цель и задачи работы.
- •3.5. Определение нитрит-ионов методом градуировочного графика.
- •Вопросы для самоконтроля
- •Фототурбидиметрия.
- •Цель и задачи работы
- •Оборудование и реактивы
- •Определение сульфатов в растворе
- •Приготовление стандартных растворов и раствора сравнения:
- •1. Цель и задачи работы.
- •Вопросы для самоконтроля
- •Рефрактометрия
- •Цель и задачи работы
- •Оборудование и реактивы
- •Программа работы
- •Рефрактометрическое определение сахара в молоке.
- •Подготовка пробы к анализу:
- •Порядок работы на рефрактометре:
- •Контрольная задача. Определение содержания сахара в анализируемом образце
- •Определение содержания хлорида натрия в водном растворе. Приборы и реактивы.
- •Приготовление стандартных растворов:
- •Построение градуировочного графика.
- •Контрольная задача. Определение содержания хлорида натрия в анализируемом растворе
- •Оформление лабораторного журнала
- •1.2. Оборудование и реактивы
- •1.3. Рефрактометрическое определение сахара в молоке
- •Вопросы для самоподготовки
- •Определение содержания глюкозы в анализируемом растворе по методу градуировочного графика.
- •Поляриметрическое определение сорбита в смеси.
- •Оформление лабораторного журнала
- •Определение глюкозы
- •Цель и задачи работы
- •Определение сорбита
- •1. Иономер-кондуктометр; 2. Магнитная мешалка; 3. Кондуктометрический датчик; 4. Ячейка; 5. Бюретка
- •Определение солесодержания вод скважин методом прямой кондуктометрии.
- •Определение качества очистки дистиллированной и бидистиллированной воды методом прямой кондуктометрии
- •Определение качества очистки дисстилированной воды.
- •Опредление качества очистки бидистиллированной воды
- •Определение слабой кислоты и соли слабого основания в их смеси методом кондуктометрического титрования
- •Определение слабой кислоты и соли слабого основания в их смеси.
- •Стандартизация раствора (вторичного стандарта) по первичном стандарту hCl
- •Контрольная задача. Определение содержания борной кислоты и солянокислого гидроксиламина в испытуемой смеси
- •Определение ионов и в их смеси методом кондуктометрического титрования
- •Определение сульфат-ионов методом кондуктометрического титрования
- •Оформление лабораторного журнала
- •Определение солесодержания вод скважин методом прямой кондуктометрии
- •1. Цель и задачи работы.
- •Определение качества очистки дистиллированной и бидистиллированной воды методом прямой кондуктометрии
- •1. Цель и задачи работы.
- •Определение слабой кислоты и соли слабого основания в их смеси методом кондуктометрического титрования
- •1. Цель и задачи работы
- •Определение ионов и в их смеси методом кондуктометрического титрования
- •Определение сульфат ионов методом кондуктометрического титрования
- •Вопросы для самоконтроля.
- •Потенциометрия
- •Цель и задачи работы
- •Оборудование и реактивы
- •1. Иономер универсальный Анион-4100. 2. Стеклянный электрод. 3. Хлорсеребряный электрод. 4.Ячейка. 5. Бюретка. 6. Магнитная мешалка.
- •Определение нитрат-ионов методом прямой потенциометрии методом градуировочного графика и методом добавок
- •Определение нитрат-ионов по методу градуировочного графика
- •Определение нитрат-ионов методом добавок
- •Определение хлороводородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования
- •Стандартизация раствора (вторичного стандарта) по первичном стандарту hCl
- •Контрольная задача. Определение содержания хлороводородной и уксусной кислот в анализируемом образце.
- •Определение фосфорной кислоты и дигидрофосфата натрия в растворе при их совместном присутствии методом потенциометрического титрования
- •Стандартизация раствора (вторичного стандарта) по первичном стандарту hCl
- •Контрольная задача. Определение содержания фосфорной кислоты и дигидрофосфата натрия в анализируемом образце.
- •Определение железа (II) в присутствии железа (III) методом потенциометрического титрования.
- •Приготовление модельного раствора
- •Определение содержания железа (II) в анализируемом растворе
- •Определение свинца (II) в растворе.
- •Контрольная задача. Определение свинца (II) в растворе.
- •Определение железа (III) в растворе
- •Определение железа (III) в растворе (рабочий электрод – платиновый)
- •Определение железа (III) в растворе (рабочий электрод – стеклянный)
- •Оформление лабораторного журнала
- •Определение нитрат-ионов методом прямой потенциометрии методом градуировочного графика и методом добавок
- •1. Цель и задачи работы.
- •Определение хлороводородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования
- •1. Цель и задачи работы
- •Определение фосфорной кислоты и дигидрофосфата натрия в растворе при их совместном присутствии методом потенциометрического титрования
- •1. Цель и задачи работы
- •Определение железа (II) в присутствии железа (III) методом потенциометрического титровании.
- •Определение железа (III) в растворе
- •Определение железа (III) в растворе ( рабочий электрод - платиновый)
- •Определение железа (III) в растворе (рабочий электрод - стеклянный)
- •Вопросы для самоподготовки.
- •Контрольная задача. Определение содержания тиосульфата натрия в анализируемом образце
- •Определение хлороводородной кислоты методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности
- •Оформление лабораторного журнала
- •Опредление тиосульфата натрия методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности
- •Определение хлороводородной кислоты методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности.
- •Вопросы для самоподготовки
Министерство образования и науки РФ
Федеральное государственное бюджетное образовательное
учреждение высшего образования
«Тульский государственный университет»
Кафедра химии
Сборник методических указаний к лабораторным работам
по дисциплине
«Аналитическая химия»
Направление подготовки: 020100 «Химия»
Профиль подготовки (специализация): 020100.62.10. «Химия окружающей среды,
химическая экспертиза и экологическая безопасность»
Форма обучения: очная
Тула 2018 г.
1 Атомно-эмиссионная фотометрия пламени 10
1.1 Цель и задачи работы 10
1.2 Оборудование и реактивы 10
1.3 Программа работы 10
1.3.1 Определение калия по методу градуировочного графика 10
1.3.2 Определение натрия по методу градуировочного графика 13
1.3.3 Определение кальция по методу градуировочного графика 13
1.4 Оформление лабораторного журнала. 14
1.4.1 Определение содержания калия в анализируемом растворе. 14
1.4.2 Определение содержания натрия в анализируемом растворе. 15
1.4.3 Определения содержания кальция в анализируемом растворе. 17
1.5 Вопросы для самоконтроля 18
2 ИК-спектроскопия органических веществ 20
3 Фотометрический анализ 27
3.1 Цель и задачи работы 27
3.2 Оборудование и реактивы 27
3.2.1 Определение концентрации ионов меди(II) в водных растворах дифференциальным методом и методом градуировочного графика 29
3.2.2 Определение железа (III) методом градуировочного графика 31
3.2.3 Определение титана (IV) методом градуировочного графика 32
3.2.4 Определение фосфора в виде синего фосфорномолибденового комплекса методом градуировочного графика 34
3.2.5 Определение фосфора в виде фосфорномолибденованадиевой гетерополикислоты 35
3.2.6 Определение нитрит-ионов 37
3.3 Оформление лабораторного журнала. 38
3.3.1 Определение меди(II) в водных растворах методом градуировочного графика и дифференциальным методом. 38
3.3.2 Определение железа (III) в водных растворах методом градуировочного графика. 42
3.3.1 Определение титана (IV) методом градуировочного графика. 44
3.3.2 Определение фосфора в виде синего фосфорномолибденового комплекса методом градуировочного графика 47
3.3.3 Определение фосфора в виде фосфорномолибденованадиевой гетерополикислоты 50
3.3.4 Определение нитрит-ионов методом градуировочного графика. 52
3.4 Вопросы для самоконтроля 55
4 Фототурбидиметрия. 57
4.1 Цель и задачи работы 57
4.2 Оборудование и реактивы 57
4.2.1 Определение сульфатов в растворе 57
4.2.2 Клетки 59
4.3 Оформление лабораторного журнала. 59
4.3.1 Определение сульфатов турбидиметрическим методом. 59
4.3.2 клетки 61
4.4 Вопросы для самоконтроля 61
5 Рефрактометрия 62
5.1 Цель и задачи работы 62
5.2 Оборудование и реактивы 62
5.3 Программа работы 62
5.3.1 Рефрактометрическое определение сахара в молоке. 62
5.3.2 Определение содержания хлорида натрия в водном растворе. 65
5.4 Оформление лабораторного журнала 67
5.5 Вопросы для самоподготовки 69
6 Поляриметрия 71
6.1 Цель и задачи работы 71
6.2 Оборудование и реактивы 71
6.2.1 Поляриметрическое определение глюкозы 71
6.2.2 Поляриметрическое определение сорбита в смеси. 72
6.3 Оформление лабораторного журнала 73
6.3.1 Определение глюкозы 73
6.3.2 Определение сорбита 74
6.4 Вопросы для самоконтроля 74
7 Кондуктометрия. 75
7.1 Цель и задачи работы. 75
7.2 Оборудование и реактивы 75
7.2.1 Определение солесодержания вод скважин методом прямой кондуктометрии. 76
7.2.2 Определение качества очистки дистиллированной и бидистиллированной воды методом прямой кондуктометрии 77
7.2.3 Определение слабой кислоты и соли слабого основания в их смеси методом кондуктометрического титрования 78
7.2.4 Определение слабой кислоты и соли слабого основания в их смеси. 78
7.2.5 Определение
ионов
 и
и
 в их смеси методом кондуктометрического
титрования 80
в их смеси методом кондуктометрического
титрования 80
7.2.6 Определение сульфат-ионов методом кондуктометрического титрования 82
7.3 Оформление лабораторного журнала 83
7.3.1 Определение солесодержания вод скважин методом прямой кондуктометрии 83
7.3.2 Определение качества очистки дистиллированной и бидистиллированной воды методом прямой кондуктометрии 84
7.3.3 Определение слабой кислоты и соли слабого основания в их смеси методом кондуктометрического титрования 84
7.3.4 Определение
ионов
 и
и
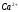 в их смеси методом кондуктометрического
титрования 86
в их смеси методом кондуктометрического
титрования 86
7.3.5 Определение сульфат ионов методом кондуктометрического титрования 88
7.4 Вопросы для самоконтроля. 89
8 Потенциометрия 91
8.1 Цель и задачи работы 91
8.2 Оборудование и реактивы 91
8.2.1 Определение нитрат-ионов методом прямой потенциометрии методом градуировочного графика и методом добавок 93
8.2.2 Определение хлороводородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования 95
8.2.3 Определение фосфорной кислоты и дигидрофосфата натрия в растворе при их совместном присутствии методом потенциометрического титрования 97
8.2.4 Определение железа (II) в присутствии железа (III) методом потенциометрического титрования. 99
8.2.5 Определение свинца (II) в растворе. 100
8.2.6 Определение железа (III) в растворе 101
8.3 Оформление лабораторного журнала 103
8.3.1 Определение нитрат-ионов методом прямой потенциометрии методом градуировочного графика и методом добавок 103
8.3.2 Определение хлороводородной и уксусной кислот в растворе при их совместном присутствии методом потенциометрического титрования 108
8.3.3 Определение фосфорной кислоты и дигидрофосфата натрия в растворе при их совместном присутствии методом потенциометрического титрования 110
8.3.4 Определение железа (II) в присутствии железа (III) методом потенциометрического титровании. 113
8.3.5 Определение железа (III) в растворе 115
8.4 Вопросы для самоподготовки. 117
9 Кулонометрия 119
9.1 Цель и задачи работы 119
9.2 Реактивы и оборудование 119
9.2.1 Опредление тиосульфата натрия методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности 119
9.2.2 Определение хлороводородной кислоты методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности 121
9.3 Оформление лабораторного журнала 122
9.3.1 Опредление тиосульфата натрия методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности 122
9.3.2 Определение хлороводородной кислоты методом кулонометрического титрования с потенциометрической фиксацией точки эквивалентности. 124
9.4 Вопросы для самоподготовки 125
