
- •Глава 1 вода основа жизни на земле
- •1.1.Вода, ее происхождение и количество на земном шаре.
- •Мировые запасы воды
- •Периоды возобновления запасов воды на земле
- •1.2.Круговорот воды на земном шаре.
- •Характеристики круговорота воды для материков земного шара
- •1.3.Физические и химические свойства воды.
- •Глава 2 состав и показатели качества природных и сточных вод
- •2.1.Дисперсные водные системы и их классификация.
- •2.2.Свойства коллоидных растворов, их устойчивость и разрушение.
- •2.3.Состав природных вод.
- •2.4.Показатели качества природных вод.
- •Степень жесткости природных вод
- •2.5.Оценка качества поверхностных вод
- •Общие требования к составу и свойствам воды
- •Критерии оценки загрязненности поверхностных вод
- •Эколого-санитарная классификация качества поверхностных вод
- •Классификация загрязненности воды водных объектов
- •Ориентировочная шкала оценки загрязнения водных систем
- •2.6.Контроль загрязнения поверхностных вод
- •Расположение и категория пунктов наблюдения на водных объектах
- •Состав программ наблюдений за качеством поверхностных вод
- •2.7.Характеристика сточных вод.
- •Состав сточных вод машиностроительного завода
- •Состав сточных вод цехов приборостроительного завода
- •Состав сточных вод металлопокрытий автомобильных заводов
- •Классификация примесей воды по их фазово-дисперсному состоянию и процессы, используемые для их удаления. (по л.А.Кульскому)
- •2.8.Показатели качества сточных вод
- •2.9.Оценка качества сточных вод.
- •Характеристика агрессивности производственных сточных вод
- •Глава 3 Современное производство и загрязнение гидросферы
- •3.1.Понятие о системах водообеспечения и водоотведения промышленных предприятий.
- •Укрупненные нормы водоотведения
- •3.2.Система канализации промышленных предприятий.
- •Методы обезвреживания производственных сточных вод (по с. В. Яковлеву)
- •3.3.Условия выпуска производственных сточных вод в городскую канализацию.
- •3.4.Определение необходимой степени очистки производственных сточных вод
- •3.4.1.Расчет необходимой степени очистки сточных вод по концентрации взвешенных веществ.
- •3.4.2.Расчет допустимого состава сточных вод по концентрации растворенных вредных веществ.
- •3.4.3.Расчет необходимой степени очистки по изменению активной реакции воды.
- •Глава 4 Механические методы очистки сточных вод
- •4.1.Основная схема механической очистки производственных сточных вод.
- •4.2.Решетки для процеживания.
- •Решетка из металлических стержней; 2 - механизм для снятия задержанных решеткой
- •4.3.Песколовки
- •4.4.Усреднители.
- •4.5.Устройства для выделения из сточных вод нерастворимых примесей под действием гравитационных сил.
- •4.5.1.Теоретические основы процессов осаждения твердых частиц в вязкой среде.
- •4.5.2.Первичные отстойники.
- •4.5.3.Прочие устройства для механической очистки воды.
- •4.6. Устройства для выделения из сточных вод нерастворимых примесей под действием центробежных сил
- •4.6.1.Открытые и напорные гидроциклоны.
- •Числовые значения коэффициентов и констант m в формуле
- •Сточная вода
- •4.6.2.Центрифуги.
- •4.7.Фильтрование.
- •4.7.1.Фильтрование через фильтрующие перегородки.
- •4.7.2. Сетчатые барабанные фильтры.
- •4.7.3. Фильтры с зернистой загрузкой.
- •Основные размеры, мм, напорных вертикальных фильтров
- •4.7.4.Магнитные фильтры.
- •4.7.5.. Фильтрование эмульгированных веществ
- •Глава 5 Химические методы очистки сточных вод
- •5.1.Нейтрализация
- •Условия применения способов нейтрализации кислых сточных вод
- •5.1.1.Нейтрализация смешением.
- •5.1.2.Реагентная нейтрализация.
- •Расход реагентов, кг/кг, для нейтрализации 100%-ных кислот и щелочей
- •5.1.3.Нейтрализация кислых сточных вод путем их фильтрования через нейтрализующие материалы.
- •5.1.4.Нейтрализация щелочных сточных вод кислыми газами.
- •5.2.Окислительный метод очистки сточных вод.
- •5.2.1.Окисление реагентами, содержащими активный хлор.
- •Состав цианосодержащих сточных вод гальванических цехов автозаводов России. (по д.Н.Смирнову и в.Е.Генкину).
- •5.2.2.Окисление пероксидом водорода.
- •5.2.3.Окисление кислородом воздуха.
- •5.2.4.Озонирование.
- •Технические характеристики отечественных озонаторов трубчатого типа
- •5.2.5.Окисление перманганатом калия.
- •5.2.6.Радиационное окисление.
- •5.3.Очистка восстановлением.
- •5.4.Реагентные методы выделения загрязняющих веществ в виде малорастворимых и нерастворимых соединений.
- •Значения констант произведения растворимости при комнатной температуре
- •Расход реагентов, кг/кг, требуемых для удаления металлов
- •Величины рН осаждения гидроксидов металлов
- •Растворимость сульфидов некоторых металлов в зависимости от рН раствора при комнатной температуре.
- •Глава 6 Физико-химические методы очистки сточных вод
- •6.1.Коагуляция и флокуляция.
- •6.1.1.Основные характеристики дисперсных систем.
- •Основные типы дисперсных систем
- •6.1.2.Теоретические основы коагуляции коллоидных примесей, содержащихся в сточных водах.
- •6.1.2.1.Понятие о строении двойного электрического слоя.
- •6.1.2.2.Устойчивость дисперсных систем
- •6.1.3. Понятие о гетерокоагуляции и применяемых коагулянтах .
- •Оптимальные величины рН при коагуляционной очистке
- •6.1.4. Флокуляция.
- •6.1.5. Технология коагуляционной и флокуляционной очистки сточных вод и используемое оборудование.
- •Зависимость скорости потока сточной воды в осветлителе от концентрации взвешенных веществ.
- •6.2. Сорбция.
- •Конструктивные и технологические показатели сорбционных фильтров с активированным углем.
- •6.3.Флотация.
- •6.3.1.Флотация с выделением воздуха из раствора.
- •6.3.2.Напорная флотация.
- •6.3.3.Флотация с механическим диспергированием воздуха.
- •6.3.4.Флотация с подачей воздуха через пористые материалы.
- •Скорость подъема пузырьков в воде при 20 оС
- •6.3.5.Очистка методом пенного фракционирования (пенной сепарацией)
- •6.3.6.Понятие о химической, биологической и ионной флотации.
- •6.4. Экстракция.
- •Значения коэффициента распределения kp некоторых загрязняющих веществ между экстрагентами и водой при комнатной температуре.
- •Основные экстрагенты, предназначенные для выделения из сточных вод тяжелых цветных металлов и железа.
- •6.5.Ионный обмен.
- •Характеристика основных марок отечественных катионитов, выпускаемых для нужд водоподготовки (по а.И.Родионову с соавт.).
- •Характеристика основных марок отечественных анионитов, выпускаемых для нужд водоподготовки (по а.И.Родионову с соавт.)
- •6.5.1. Понятие об ионообменном равновесии.
- •6.5.2.Понятие о регенерации ионитов.
- •6.5.3. Технологические схемы ионообменной очистки сточных вод и установки для их реализации.
- •VIII - обезвоженный осадок на полигон.
- •6.6.Электрохимическая очистка сточных вод.
- •6.6.1. Классификация методов электрохимической очистки сточных вод.
- •6.6.2. Теоретические основы электрохимических процессов.
- •6.6.2.1.Электродные потенциалы.
- •6.6.2.2.Понятие об окислительно-восстановительном равновесии
- •6.6.2.3. Массоперенос вещества и скорость электрохимической реакции.
- •6.6.2.4. Поляризационные явления в электрохимических реакциях.
- •6.6.2.5.Кинетические закономерности основных электродных процессов, протекающих при очистке сточных вод.
- •6.6.2.6.Понятие о редокси -процессах (электрохимическом восстановлении и окислении).
- •6.6.3. Применение электрохимических методов при очистке сточных вод.
- •6.6.3.1. Анодное окисление и катодное восстановление.
- •6.6.3.2. Электрокоагуляция.
- •6.6.3.3.Электрофлотация.
- •6.6.3.4.Электродиализ.
- •Основные свойства ионитовых мембран.
- •6.6.3.5.Гальванокоагуляционная очистка сточных вод.
- •Результаты опытно-промышленных испытаний по гальванокоагуляционной очистке сточных вод
- •6.7. Применение методов обратного осмоса и ультрафильтрации для очистки сточных вод.
- •6.7.1.Понятие о мембранных процессах.
- •6.7.2.Классификация полупроницаемых мембран.
- •6.7.3.Использования установки обратного осмоса для очистки хромсодержащих сточных вод.
- •6.8.Термическая обработка сточных вод.
- •6.8.1.Очистка сточных вод с выделением растворенных веществ (концентрирование сточных вод).
- •6.8.2.Выделение растворенных веществ из концентрированных растворов.
- •6.8.3.Термоокислительные методы обезвреживания сточных вод.
- •Глава 7 Биологическая очистка сточных вод
- •7.1.Общие положения.
- •7.2.Влияние различных технологических факторов на эффективность процессов биологической очистки
- •7.3.Естественные и искусственные методы биологической очистки.
- •7.3.1.Сооружения почвенной очистки и биологические пруды.
- •Продолжительность очистки сточных вод в биологических прудах
- •7.3.2.Биофильтры.
- •7.3.3.Аэротенки.
- •7.3.4.Окситенки.
- •7.4.Использование биологических методов очистки сточных вод от тяжелых металлов.
- •7.5.Понятие о глубокой очистке (доочистке) производственных сточных вод
- •Глава 8 Обработка осадков производственных сточных вод
- •8.1.Состав и свойства осадков.
- •Химический состав минеральной части осадков
- •Удельное сопротивление осадков сточных вод
- •Зависимость удельного сопротивления сырых осадков первичных источников от характерных особенностей сточных вод
- •8.2.Основные процессы, применяемые для обработки осадков производственных сточных вод
- •8.3.Уплотнение осадков.
- •8.3.1.Гравитационное уплотнение осадков.
- •8.3.2.Флотационное уплотнение осадков.
- •8.3.3.Центробежное уплотнение осадков.
- •Техническая характеристика серийных центрифуг
- •Оптимальный режим работы центрифуги огш 502 к-4
- •Значения критериев гидродинамического подобия при разделении активного ила
- •8.4. Анаэробное (метановое) сбраживание осадков
- •8.4.1. Понятие об анаэробном сбраживании.
- •8.4.2. Технологические схемы анаэробного сбраживания осадков.
- •1 Ступени, 6 - метатенк п ступени, 7 - выгрузка сброженного осадка.
- •Требуемые объемы и число метатенков для станций аэрации различной производительности
- •8.4.3.Основы расчета метатенков.
- •8.5.Аэробная стабилизация осадков.
- •8.6.Кондиционирование осадков.
- •8.6.1.Реагентная обработка .
- •8.6.3. Жидкофазное окисление (метод Циммермана).
- •8.6.4. Замораживание и оттаивание.
- •8.7. Обезвоживание осадков.
- •8.7.1. Сушка осадков на иловых площадках.
- •8.7.2. Фильтрование.
- •Технические характеристики отечественных барабанных вакуум-фильтров
- •Показатели работы барабанных вакуум-фильтров
- •Показатели работы фильтр-прессов
- •8.7.3. Центрифугирование и сепарирование.
- •Технологические параметры работы осадительной центрифуги
- •8.8. Термическая сушка осадков.
- •8.8.1. Основные понятия.
- •8.8.2. Оборудование для сушки осадков.
- •8.9. Термические методы обезвреживания осадков.
- •8.9.1. Основные положения.
- •8.9.2. Основное оборудование для термического обезвреживания осадков.
- •Сравнительная характеристика показателей работы печей при термическом обезвреживании осадков (по с.В.Яковлеву).
- •Глава 9 Очистка сточных вод от радиоактивных загрязнений
- •Пдк и содержание отдельных компонентов в шахтных водах
- •Пдк и содержание компонентов жидкой фазы отвальной рудной пульпы, г/л.
- •Нормированные количества жидких радиоактивных отходов.
- •Ориентировочная характеристика отходов аэс.
- •Классификация жидких радиоактивных отходов.
- •Количество твердых отходов низкой и средней активности, образующихся в год при эксплуатации аэс мощностью 100 мВт.
- •Реакции образования радионуклидов - продуктов коррозии.
- •Количества радиоактивных отходов, образующихся на аэс
6.1.2.Теоретические основы коагуляции коллоидных примесей, содержащихся в сточных водах.
Коагуляция - это процесс укрупнения дисперсных частиц за счет их взаимодействия и объединения в агрегаты. Мелкие (первичные) частицы в таких агрегатах соединены силами межмолекулярного взаимодействия. Слипание однородных частиц называется гомокоагуляцией, а разнородных - гетерокоагуляцией. Вещества, способные вызвать коагуляцию частиц называют в общем случае коагуляторами, а в водоподготовке - коагулянтами или гидролизующимися коагулянтами. Последние не только вызывают коагуляцию частиц загрязнений, но и образуют, гидролизуясь, малорастворимые продукты, способные объединяться в крупные хлопья.
Дискретная фаза (твердая или жидкая) в производственных сточных водах представлена коллоидными частицами размером 0,001-0,1мкм, мелкодисперсными частицами размером 0,1-10 мкм, а также частицами, размер которых превышает 10 мкм. В процессах механической обработки сточных вод наиболее эффективно удаляются последние из вышеперечисленных частиц. Коллоидные и мелкодисперсные частицы при механической обработке практически не удаляются, поэтому для очистки сточных вод от этих загрязнений используют различные коагулянты (чаще всего - соли аммония и железа), которые увеличивают их скорость осаждения.
Для лиофобных золей и суспензий характерно образование на поверхности двойного электрического слоя (ДЭС) ионов и скачки потенциала на границе раздела фаз.
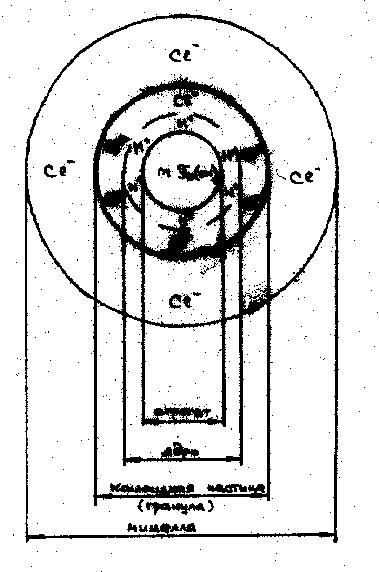
Рис. 6.30 Схема строения мицеллы гидроксида железа.
Рассмотрим в качестве примера строение золя гидроксида железа (Рис.5.1). Согласно существующей мицеллярной теории золь состоит из двух частей: мицелл и интермицеллярной жидкости. Мицелла - это структурная коллоидная частица, т.е. частицы дисперсной фазы, окруженная двойным электрическим слоем. Интермицеллярной жидкостью называют дисперсионную среду, разделяющую мицеллы, в которой растворены электролиты, не электролиты и поверхностно-активные вещества, являющиеся стабилизаторами коллоидной системы. Основу коллоидной частицы составляют микрокристаллы труднорастворимого , называемые агрегатами. В результате избирательной адсорбции на поверхности агрегата образуется положительно зараженный слой, состоящий из ионов водорода (потенциалообразующие ионы, сокращенно РОИ). Агрегаты вместе с потенциалообразующими ионами образует ядро. Под действием электростатических сил притяжения у ядра формируются слой ионов противоположного знака - противоионов, компенсирующих частично заряд ядра. В рассмотренном примере их роль выполняют ионы Сl-. Частицу с окружающим ее плотным слоем ионов называют гранулой.
Гранула характеризуется двойным электрическим слоем, который образуется из потенциалообразующих ионов и противоионов.
Следует указать, что часть противоионов (n-х) наиболее близко расположенных к ядру, находится в слое жидкости, смачивающем поверхность твердого ядра и испытывают действие не только электростатических, но и ван-дер-ваальсовых сил ядра, поэтому прочно удерживаются около него и образуют так называемый адсорбционный слой противоионов (плотный слой). Остальные х противоионов, слабее связаны с ядром (только электростатически) и под влиянием теплового движения располагаются в жидкой фазе диффузно и называются диффузионным слоем. Такова схема строения мицеллы. Мицеллы золей электронейтральны.
Структуру мицеллы Fe(OH)3 можно представить следующими формулами:
{[Fe(OH)3]mnH+(n-x)Cl-}+xCl- ( 6.0)
или {[Fe(OH)3]mnFeOCl+,+FeO+(n-x)Cl-}+xCl- ( 6.0)
Укажем также, что граница между коллоидной частицей и диффузионным слоем носит название границы или поверхности скольжения. Границы скольжения обозначают ту геометрическую поверхность, по которой происходит разделение ("разрыв") мицеллы на коллоидную часть и диффузный слой в случае ее перемещения относительно дисперсионной среды.
Для мицеллы гидрооксида алюминия, образованного при гидролизе, можно по аналогии записать:
{[Al(OH)3]m nH+1/2(n-x)SO 42-}+1/2xSO42- ( 6.0)
Если предположить, что потенциалообразующим ионов является Al3+, то:
{[Al(OH) 3] m nAl3+ 3/2(n-x)SO 2-4}+3/2xSO42- ( 6.0)
В ряде публикаций также отмечается, что потенциалообразующим слоем в мицелле Al(OH)3 может быть катион Al6(OH)153+.
