
- •Термодинамика
- •Глава 1 Основные понятия и определения термодинамики…………… 11
- •Глава 8 Термохимия…………………………………………………….. 60
- •Глава 9 Термодинамические свойства индивидуальных веществ. Стандартное состояние вещества……………………………… 69
- •Глава 10 Отдельная химическая реакция………………………………… 83
- •Глава 11 Методы расчета термодинамических свойств химически реагирующих систем…………………………………………… 104
- •Глава 12 Термодинамические политропные процессы с идеальными газами……………………………………………………………. 156
- •Глава 13 Тепловые машины и компрессоры……………………………. 171
- •Глава 14 Термодинамика потоков жидкости и газа………………………197
- •Глава 15 Водяные пары……………………………………………………..223
- •Глава 16 Основы эксергетического метода термодинамического анализа………………………………………………………… 241
- •Глава 1. Основные понятия и определения термодинамики
- •Глава 2 уравнения состояния вещества
- •2.1. Термические и калорические уравнения состояния
- •2.2. Термические уравнения состояния для идеального газа
- •2.3. Термические уравнения состояния для реальных газов
- •Глава 3. Смеси веществ
- •3.1. Способы задания состава смеси. Закон Амага.
- •3.2. Соотношения для смесей идеальных газов. Закон Дальтона
- •Глава 4. Теплоемкость
- •4.1. Виды теплоемкости
- •4.2. Уравнение Майера
- •4.3. Теплоемкость химически реагирующей термодинамической системы
- •Глава 5. Первый закон термодинамики
- •5.1. Уравнение первого закона термодинамики для сложной открытой системы в общем виде.
- •5.2. Уравнение 1-го закона термодинамики для проточной термодинамической системы
- •Глава 6. Второй закон термодинамики
- •6.1. Сущность второго закона термодинамики. Равновесные и неравновесные состояния, обратимые и необратимые процессы
- •6.2. Математическое выражение 2-го закона термодинамики. Три составляющие изменения энтропии термодинамической системы
- •6.3. Энтропия изолированной термодинамической системы
- •Глава 7. Объединенные выражения первого и второго законов термодинамики
- •7.1. Различные формы записи объединенных выражений
- •7.2. Характеристические функции и дифференциальные соотношения взаимности термодинамики
- •7.3. Максимальная и минимальная работы процесса. Термодинамические потенциалы
- •7.4. Условия равновесия термодинамической системы. Термодинамическое сродство
- •7.5. Связь между изобарной и изохорной теплоемкостями в общем виде
- •7.6.Расчетные выражения для скорости звука в общем виде
- •7.7. Максимальная и минимальная теплоты процесса
- •Глава 8. Термохимия
- •8.1. Формы записи уравнений химических реакций в общем виде
- •8.2. Понятие пробега химической реакции
- •8.3. Изохорный и изобарный тепловые эффекты химических реакций и связь между ними
- •8.4. Зависимости тепловых эффектов хр от температуры. Формула Кирхгофа.
Глава 6. Второй закон термодинамики
6.1. Сущность второго закона термодинамики. Равновесные и неравновесные состояния, обратимые и необратимые процессы
Второй закон термодинамики устанавливает существование у всякой равновесной термодинамической системы однозначной функции состояния – энтропии S.
Понятие энтропии вводится в
феноменологической термодинамике с
помощью выражения dS=![]() ,
в соответствии с которым при подводе к
ТС порции теплоты
,
в соответствии с которым при подводе к
ТС порции теплоты![]() энтропия системы возрастает. Температура
Т в этом выражении есть температура на
границе ТС в точке, где подводится порция
теплоты
энтропия системы возрастает. Температура
Т в этом выражении есть температура на
границе ТС в точке, где подводится порция
теплоты![]() .
С помощью этой специальной функции
состояния можно математически описать
2-ой закон термодинамики.
.
С помощью этой специальной функции
состояния можно математически описать
2-ой закон термодинамики.
ТС находится в состоянии равновесия, если после ее изоляции от окружающей среды в ней не наблюдается никаких изменений, и в неравновесном состоянии, если после ее изоляции в ней обнаруживаются какие-либо изменения. Эти изменения в изолированной системе протекают самопроизвольно, и со временем система приходит в равновесное состояние. Процесс является неравновесным, если при его совершении ТС хотя бы в одной точке процесса находится в неравновесном состоянии. Неравновесные состояния ТС могут быть связаны либо с локальной неравновесностью в точке, либо с объемной неравновесностью из-за различия температур, давлений и других параметров в различных элементах объема ТС. При объемной неравновесности ТС для проведения термодинамических расчетов объем ТС можно разбить на малые объемы, в пределах которых перепады параметров (р, Ти др.) малы и состояния в пределах каждого из объемов можно считать локально равновесным.
Энтропия изолированной ТС не изменяется только при равновесных процессах в ней и всегда возрастает при неравновесных процессах. Таким образом, 2-ой закон термодинамики – закон об энтропии и состоит из принципа существования энтропии и принципа возрастания энтропии.
Все равновесные процессы – обратимые, а неравновесные – необратимые процессы. Процесс называется необратимым, если суммарный запас энергии направленного, упорядоченного движения частиц ТС (работы) уменьшается, и обратимым, если этот запас энергии сохраняется. В необратимых процессах происходит диссипация (рассеяние) энергии упорядоченного движения материи в энергию теплового, неупорядоченного движения, которую нельзя превратить ни в какой другой вид энергии в обратном направлении. Обратимый (равновесный) процесс возможен только при бесконечно малых перепадах параметров на границе ТС и окружающей среды в любой момент процесса.
Второй закон термодинамики является обобщением опытных данных, указывает на особый характер протекания тепловых процессов и устанавливает пределы возможных превращений теплоты в работу. Этот закон позволяет определить направление и условия протекания любого термодинамического процесса. Дело в том, что тепловые процессы, удовлетворяющие первому закону термодинамики, подразделяются на самопроизвольные, протекающие без внешнего воздействия в данных условиях и на процессы, которые не могут происходить в данных условиях без внешнего воздействия.
В изолированной ТС самопроизвольные
процессы протекают в направлении
достижения равновесия системы. При этом
работа преобразуется в теплоту (![]() ),
а теплота переходит лишь от тела с более
высокой температурой к телу с более
низкой температурой. Процессы с
превращением теплоты в работу (
),
а теплота переходит лишь от тела с более
высокой температурой к телу с более
низкой температурой. Процессы с
превращением теплоты в работу (![]() )
в изолированной системе самопроизвольно
идти не могут. Открытие 2-го закона
термодинамики было связано с анализом
работы тепловых машин (Сади Карно).
)
в изолированной системе самопроизвольно
идти не могут. Открытие 2-го закона
термодинамики было связано с анализом
работы тепловых машин (Сади Карно).
Для осуществления процессов с превращением
теплоты в работу надо создать из двух
тел с различной температурой (Т1>Т2)
неравновесную ТС, обладающую запасом
энергии направленного упорядоченного
движения частиц, а также осуществить с
помощью термодинамического рабочего
тела (ТРТ) обратимый цикл и передать
результирующую работу циклаlцтретьему телу – аккумулятору работы.
При этом всю подведенную теплотуq1нельзя превратить в работуlц.
Часть теплоты необходимо отвести в
холодильник![]() .
.
Схему превращения теплоты в работу
можно представить в виде
![]() :
:
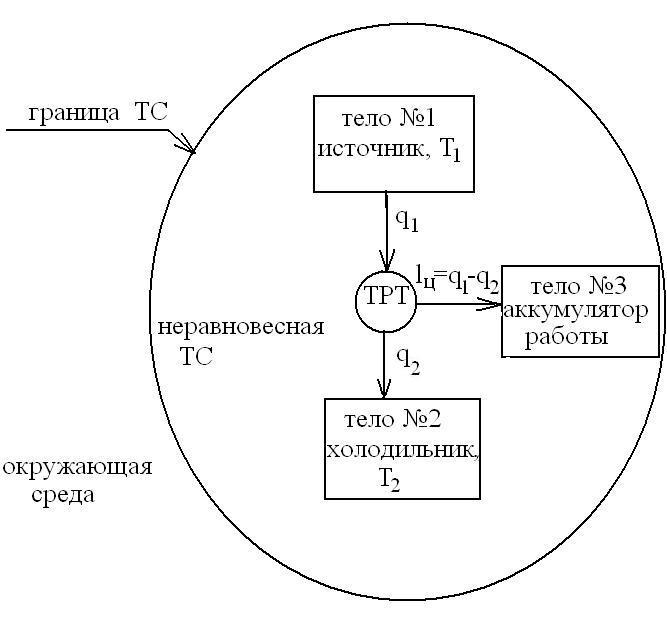
Неравноценность превращений работы в теплоту и теплоты в работу объясняется тем, что энергию направленного движения частиц (работу) можно превратить в тепловую энергию неупорядоченного, хаотического движения частиц, а обратный процесс возможен только при наличии соответствующей компенсации.
Наиболее краткой формулировкой 2-го закона термодинамики является формулировка Томсона-Кельвина: «Теплота, содержащаяся в окружающей среде, не может быть превращена в работу теплового двигателя, если температура всех окружающих тел будет одинаковой, т.е. вечный двигатель II рода неосуществим». Вечный двигательIIрода – это двигатель, который производил бы механическую работу исключительно за счет теплоты окружающей среды с одинаковой температурой во всех ее точках.
