
- •Термодинамика
- •Глава 1 Основные понятия и определения термодинамики…………… 11
- •Глава 8 Термохимия…………………………………………………….. 60
- •Глава 9 Термодинамические свойства индивидуальных веществ. Стандартное состояние вещества……………………………… 69
- •Глава 10 Отдельная химическая реакция………………………………… 83
- •Глава 11 Методы расчета термодинамических свойств химически реагирующих систем…………………………………………… 104
- •Глава 12 Термодинамические политропные процессы с идеальными газами……………………………………………………………. 156
- •Глава 13 Тепловые машины и компрессоры……………………………. 171
- •Глава 14 Термодинамика потоков жидкости и газа………………………197
- •Глава 15 Водяные пары……………………………………………………..223
- •Глава 16 Основы эксергетического метода термодинамического анализа………………………………………………………… 241
- •Глава 1. Основные понятия и определения термодинамики
- •Глава 2 уравнения состояния вещества
- •2.1. Термические и калорические уравнения состояния
- •2.2. Термические уравнения состояния для идеального газа
- •2.3. Термические уравнения состояния для реальных газов
- •Глава 3. Смеси веществ
- •3.1. Способы задания состава смеси. Закон Амага.
- •3.2. Соотношения для смесей идеальных газов. Закон Дальтона
- •Глава 4. Теплоемкость
- •4.1. Виды теплоемкости
- •4.2. Уравнение Майера
- •4.3. Теплоемкость химически реагирующей термодинамической системы
- •Глава 5. Первый закон термодинамики
- •5.1. Уравнение первого закона термодинамики для сложной открытой системы в общем виде.
- •5.2. Уравнение 1-го закона термодинамики для проточной термодинамической системы
- •Глава 6. Второй закон термодинамики
- •6.1. Сущность второго закона термодинамики. Равновесные и неравновесные состояния, обратимые и необратимые процессы
- •6.2. Математическое выражение 2-го закона термодинамики. Три составляющие изменения энтропии термодинамической системы
- •6.3. Энтропия изолированной термодинамической системы
- •Глава 7. Объединенные выражения первого и второго законов термодинамики
- •7.1. Различные формы записи объединенных выражений
- •7.2. Характеристические функции и дифференциальные соотношения взаимности термодинамики
- •7.3. Максимальная и минимальная работы процесса. Термодинамические потенциалы
- •7.4. Условия равновесия термодинамической системы. Термодинамическое сродство
- •7.5. Связь между изобарной и изохорной теплоемкостями в общем виде
- •7.6.Расчетные выражения для скорости звука в общем виде
- •7.7. Максимальная и минимальная теплоты процесса
- •Глава 8. Термохимия
- •8.1. Формы записи уравнений химических реакций в общем виде
- •8.2. Понятие пробега химической реакции
- •8.3. Изохорный и изобарный тепловые эффекты химических реакций и связь между ними
- •8.4. Зависимости тепловых эффектов хр от температуры. Формула Кирхгофа.
7.2. Характеристические функции и дифференциальные соотношения взаимности термодинамики
Характеристической функцией называется функция состояния ТС, позволяющая при соответствующем выборе независимых переменных (при определенных условиях сопряжения ТС с окружающей средой) выражать через свои производные наиболее просто и в явном виде термодинамические параметры, характеризующие свойства термодинамической системы. Построение термодинамического анализа на этих свойствах характеристических функций составляет основу метода характеристических функций.
Рассмотрим простую (![]() ℒ=0),
закрытую (
ℒ=0),
закрытую (![]() )
термодинамическую систему. Тогда для
обратимых процессов объединенные
выражения 1-го и 2-го законов термодинамики
будут иметь вид:
)
термодинамическую систему. Тогда для
обратимых процессов объединенные
выражения 1-го и 2-го законов термодинамики
будут иметь вид:
![]() , (5)
, (5)
![]() (6)
(6)
![]() (7)
(7)
![]() . (8)
. (8)
Каждое из уравнений (5)-(8) связывает пять
переменных величин, которые зависят
лишь от состояния ТС и не зависят от
пути процесса. Функции U,
H, F,
Gявляются
характеристическими только при
определенном выборе независимых
переменных:![]() .
Полные дифференциалы функцийU,
H, F,
Gимеют вид:
.
Полные дифференциалы функцийU,
H, F,
Gимеют вид:
![]() (9)
(9)
![]() (10)
(10)
![]() , (11)
, (11)
![]() . (12)
. (12)
Линейным дифференциальным соотношениям (9)-(12) тождественны объединенные выражения 1-го и 2-го законов термодинамики (5)-(8). Сопоставляя уравнения (5) и (9) можно наиболее просто выразить неизвестные параметры – температуру Ти давлениер с помощью частных производных внутренней энергии по энтропииSи по объемуV:
![]() ,
,![]() . (13)
. (13)
По аналогии выразим неизвестные параметры в выражениях (6)-(8) с помощью частных производных (10)-(12) для функций H, FиG:
![]() ,
,![]() , (14)
, (14)
![]() ,
,![]() , (15)
, (15)
![]() ,
,![]() . (16)
. (16)
Согласно свойству полного дифференциала вторая смешанная производная от функции Uне зависит от порядка дифференцирования, т.е.:
 ,
или (17)
,
или (17)
![]() .
.
По аналогии для функций H, F,Gполучим:
![]() ,
дляН, (18)
,
дляН, (18)
![]() ,
дляF, (19)
,
дляF, (19)
![]() ,
дляG. (20)
,
дляG. (20)
Уравнения (17)-(20) называются дифференциальными
соотношениями взаимности или уравнениями
Максвелла. Они в такой же степени
достоверны, как и законы термодинамики,
следствием которых они являются.
Уравнения (17)-(20) широко используются
при термодинамическом анализе. При
анализе также широко используется
уравнение связи, которое выводится
следующим образом. Если функция
![]() - функция состояния, то ее полный
дифференциал равен:
- функция состояния, то ее полный
дифференциал равен:
![]() .
.
Для
![]() =const
=const![]() .
Тогда получим:
.
Тогда получим:
![]() .
.
После деления на
![]() имеем:
имеем:
![]()
![]() . (21)
. (21)
Связи частных производных одного термодинамического параметра по другому (21) справедливы при определенных условиях сопряжения ТС с окружающей средой.
Схема чередования термодинамических параметров в уравнении связи (21) имеет вид:
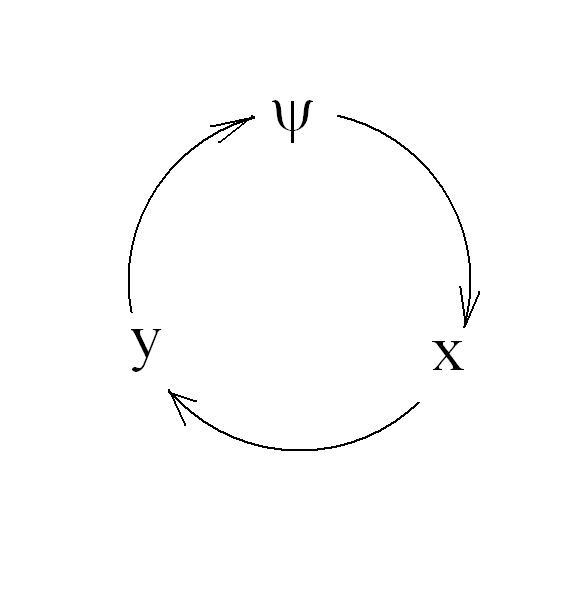
т.е. функция → аргумент → фиксированный
параметр: (![]() ),
(
),
(![]() ),
(
),
(![]() ).
).
7.3. Максимальная и минимальная работы процесса. Термодинамические потенциалы
По изменению характеристических функций можно определить максимальную работу немеханического характера при соответствующих условиях сопряжения ТС с окружающей средой, т.е. при двух фиксированных независимых параметрах. Так, для сложной закрытой ТС, в которой протекают процессы с двумя фиксированными параметрами, находящимися под знаками дифференцирования в правых частях объединенных выражений 1-го и 2-го законов термодинамики (1)-(4) получим следующие соотношения:
при S,
V=const ![]() ℒs,V
, (22)
ℒs,V
, (22)
при S,
p=const ![]() ℒs,p
, (23)
ℒs,p
, (23)
при T,
V=const ![]() ℒT,V, (24)
ℒT,V, (24)
при T,
p=const ![]() ℒT,p, (25)
ℒT,p, (25)
где
![]() ℒ=
ℒ=![]() - сумма работ немеханического
характера. Для конечного процесса 1-2
эти выражения запишем в виде, умножив
левые и правые части уравнений (22)-(25) на
минус единицу (-1). Тогда:
- сумма работ немеханического
характера. Для конечного процесса 1-2
эти выражения запишем в виде, умножив
левые и правые части уравнений (22)-(25) на
минус единицу (-1). Тогда:
![]() ℒs,V, (26)
ℒs,V, (26)
![]() ℒs,p, (27)
ℒs,p, (27)
![]() ℒT,V, (28)
ℒT,V, (28)
![]() ℒT,p, (29)
ℒT,p, (29)
При протекании обратимых процессов работа немеханического характера ℒ максимальна и равна уменьшению соответствующей характеристической функции, т.е.:
![]() ℒs,V
max,
ℒs,V
max,
![]() ℒs,p
max,
ℒs,p
max,
(30)
![]() ℒT,V
max,
ℒT,V
max,
![]() ℒT,p
max.
ℒT,p
max.
При протекании необратимых процессов с максимальными потерями работоспособности ТС работа немеханического характера равна нулю, т.е.
ℒmin=0. (31)
В общем случае при необратимых процессах часть энергии упорядоченного движения материи диссипирует (рассеивается) в энергию теплового неупорядоченного движения и работа немеханического характера ТС ℒ будет меньше максимальной работы в обратимых процессах.
В термодинамике характеристические функции: U, H, F, G, дифференциалы которых с обратным знаком равны элементарной работе немеханического характера, называют термодинамическими потенциалами:
U– изохорно-изоэнтропийный потенциал,
H– изобарно-изоэнтропийный потенциал,
F– изохорно-изотермический потенциал,
G – изобарно-изотермический потенциал.
Уменьшение термодинамических потенциалов при фиксации двух параметров в обратимых процессах равно максимальной работе ТС.
Таким образом, сумма работ немеханического характера может быть определена через изменения характеристических функций при фиксации двух независимых параметров.
