
- •Термодинамика
- •Глава 1 Основные понятия и определения термодинамики…………… 11
- •Глава 8 Термохимия…………………………………………………….. 60
- •Глава 9 Термодинамические свойства индивидуальных веществ. Стандартное состояние вещества……………………………… 69
- •Глава 10 Отдельная химическая реакция………………………………… 83
- •Глава 11 Методы расчета термодинамических свойств химически реагирующих систем…………………………………………… 104
- •Глава 12 Термодинамические политропные процессы с идеальными газами……………………………………………………………. 156
- •Глава 13 Тепловые машины и компрессоры……………………………. 171
- •Глава 14 Термодинамика потоков жидкости и газа………………………197
- •Глава 15 Водяные пары……………………………………………………..223
- •Глава 16 Основы эксергетического метода термодинамического анализа………………………………………………………… 241
- •Глава 1. Основные понятия и определения термодинамики
- •Глава 2 уравнения состояния вещества
- •2.1. Термические и калорические уравнения состояния
- •2.2. Термические уравнения состояния для идеального газа
- •2.3. Термические уравнения состояния для реальных газов
- •Глава 3. Смеси веществ
- •3.1. Способы задания состава смеси. Закон Амага.
- •3.2. Соотношения для смесей идеальных газов. Закон Дальтона
- •Глава 4. Теплоемкость
- •4.1. Виды теплоемкости
- •4.2. Уравнение Майера
- •4.3. Теплоемкость химически реагирующей термодинамической системы
- •Глава 5. Первый закон термодинамики
- •5.1. Уравнение первого закона термодинамики для сложной открытой системы в общем виде.
- •5.2. Уравнение 1-го закона термодинамики для проточной термодинамической системы
- •Глава 6. Второй закон термодинамики
- •6.1. Сущность второго закона термодинамики. Равновесные и неравновесные состояния, обратимые и необратимые процессы
- •6.2. Математическое выражение 2-го закона термодинамики. Три составляющие изменения энтропии термодинамической системы
- •6.3. Энтропия изолированной термодинамической системы
- •Глава 7. Объединенные выражения первого и второго законов термодинамики
- •7.1. Различные формы записи объединенных выражений
- •7.2. Характеристические функции и дифференциальные соотношения взаимности термодинамики
- •7.3. Максимальная и минимальная работы процесса. Термодинамические потенциалы
- •7.4. Условия равновесия термодинамической системы. Термодинамическое сродство
- •7.5. Связь между изобарной и изохорной теплоемкостями в общем виде
- •7.6.Расчетные выражения для скорости звука в общем виде
- •7.7. Максимальная и минимальная теплоты процесса
- •Глава 8. Термохимия
- •8.1. Формы записи уравнений химических реакций в общем виде
- •8.2. Понятие пробега химической реакции
- •8.3. Изохорный и изобарный тепловые эффекты химических реакций и связь между ними
- •8.4. Зависимости тепловых эффектов хр от температуры. Формула Кирхгофа.
8.3. Изохорный и изобарный тепловые эффекты химических реакций и связь между ними
Тепловой эффект химической реакции
(ТЭХР) рассматривается только для
закрытых ТС
![]() при отсутствии работ
при отсутствии работ![]() и при фиксации двух параметров:T,V=constиT,p=const.
При этих условиях мы фактически задаем
состояние ТС, если система является
равновесной.
и при фиксации двух параметров:T,V=constиT,p=const.
При этих условиях мы фактически задаем
состояние ТС, если система является
равновесной.
Для простой, закрытой ТС уравнение 1-го закона термодинамики имеет вид:
![]() ,
приТ,V=const:
,
приТ,V=const:
![]() , (1)
, (1)
![]() ,
приТ,р=const:
,
приТ,р=const:
![]() . (2)
. (2)
Тепловой эффект ХР – это максимальная теплота процесса, выделяемая или поглощаемая ТС при T,V=constиТ,р=constи отнесенная к пробегу ХР, т.е.:
![]() ,
[Дж/моль], (3)
,
[Дж/моль], (3)
![]() ,
[Дж/моль], (4)
,
[Дж/моль], (4)
где QV– изохорный тепловой эффект ХР;Qp- изобарный тепловой эффект ХР;![]() - пробег ХР.QVиQp
– функции состояния, т.е. они
характеризуют термодинамическое
состояние химически реагирующей ТС.
- пробег ХР.QVиQp
– функции состояния, т.е. они
характеризуют термодинамическое
состояние химически реагирующей ТС.
Таким образом, изохорный QVи изобарныйQpТЭХР выражаются через изменение внутренней энергии и энтальпии соответственно и определяются только начальными и конечными состояниями ТС.
Тепловые эффекты ХР не зависят от промежуточных химических состояний, через которые проходит ТС (закон Гесса, 1840г.).
В соответствии с законом Гесса сумма тепловых эффектов промежуточных ХР есть величина постоянная, равная тепловому эффекту сложной реакции независимо от последовательности протекания реакций. Закон Гесса позволяет косвенным путем аналитически вычислить тепловые эффекты ХР, в том числе и таких, которые не поддаются эксперименту.
Для ТС, где протекает одна химическая реакция, внутренняя энергия и энтальпия определяются выражениями:
![]() , (5)
, (5)
![]() , (6)
, (6)
где
![]() ,
Дж/моль, молярные величины внутренней
энергии и энтальпииi-го
вещества при стандартном состоянии
(р0=1 физ.атм);
,
Дж/моль, молярные величины внутренней
энергии и энтальпииi-го
вещества при стандартном состоянии
(р0=1 физ.атм);![]() ,
моль, количествоi-го
вещества.
,
моль, количествоi-го
вещества.
Соотношения (5) и (6) справедливы как для
идеальных, так и для реальных газов и
растворов. Для идеальных термодинамических
систем величины
![]() являются функциями только температуры.
Тогда получим связи:
являются функциями только температуры.
Тогда получим связи:
![]() , (7)
, (7)
![]() . (8)
. (8)
После подстановки выражений (7) и (8) в
формулы (3) и (4) и дифференцирования по
пробегу ХР![]() получим формулы для расчета изохорного
и изобарного ТЭХР:
получим формулы для расчета изохорного
и изобарного ТЭХР:
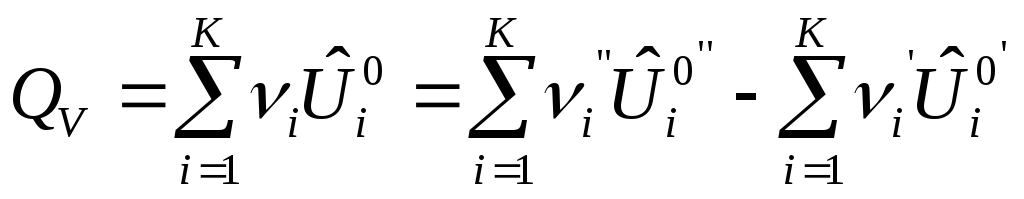 ,
Дж/моль, (9)
,
Дж/моль, (9)
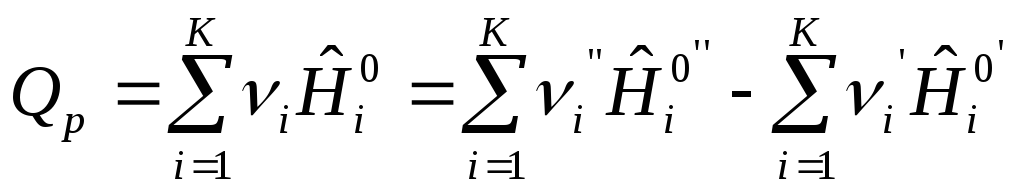 ,
Дж/моль (10)
,
Дж/моль (10)
По формулам (9) и (10) определяется тепловой эффект образования вещества. Тепловой эффект сгорания (теплота сгорания) равен теплоте образования с обратным знаком:
![]() , (11)
, (11)
![]() . (12)
. (12)
Рассмотрим пример: для ХР: 2Н2О-2Н2-О2=0.
Изобарный ТЭХР равен:![]() ,
Дж/моль, т.е. из двух молекул Н2и
одной молекулы О2образуется две
молекулы воды. Если число элементарных
реакций равноNA=6,022·1023,
то суммарная теплота этих реакций
является тепловым эффектом. Таким
образом, моль – это набор из пяти частиц
(2Н2, О2, 2Н2О) умноженный
на число Авагадро.
,
Дж/моль, т.е. из двух молекул Н2и
одной молекулы О2образуется две
молекулы воды. Если число элементарных
реакций равноNA=6,022·1023,
то суммарная теплота этих реакций
является тепловым эффектом. Таким
образом, моль – это набор из пяти частиц
(2Н2, О2, 2Н2О) умноженный
на число Авагадро.
Если
![]() зависят и от температуры и от состава
ТС, то получим выражения:
зависят и от температуры и от состава
ТС, то получим выражения:
![]() , (13)
, (13)
![]() . (14)
. (14)
Связь между изобарным и изохорным ТЭХР получим следующим образом. Запишем для 1 моля идеального газа выражение для энтальпии:
![]() .
.
Тогда для смеси идеальных газов имеем:
![]() , (15)
, (15)
где
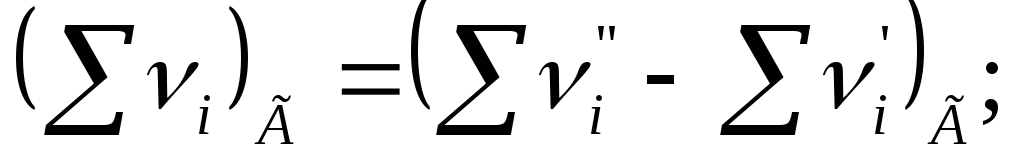
![]() ;
;![]() .
.
После подстановки QpиQVв выражение (15) имеем:
![]() . (16)
. (16)
Эта связь между QpиQV для смеси идеальных газов получена, пренебрегая объемами жидких и твердых реагентов.
Зависимость
![]() определяется видом ХР:
определяется видом ХР:
- если
![]() тоQp>QV
тоQp>QV
- если
![]() тоQp=QV
тоQp=QV
- если
![]() тоQp<QV.
тоQp<QV.
Для конденсированных веществ (растворов)
![]() .
.
