
- •Термодинамика
- •Глава 1 Основные понятия и определения термодинамики…………… 11
- •Глава 8 Термохимия…………………………………………………….. 60
- •Глава 9 Термодинамические свойства индивидуальных веществ. Стандартное состояние вещества……………………………… 69
- •Глава 10 Отдельная химическая реакция………………………………… 83
- •Глава 11 Методы расчета термодинамических свойств химически реагирующих систем…………………………………………… 104
- •Глава 12 Термодинамические политропные процессы с идеальными газами……………………………………………………………. 156
- •Глава 13 Тепловые машины и компрессоры……………………………. 171
- •Глава 14 Термодинамика потоков жидкости и газа………………………197
- •Глава 15 Водяные пары……………………………………………………..223
- •Глава 16 Основы эксергетического метода термодинамического анализа………………………………………………………… 241
- •Глава 1. Основные понятия и определения термодинамики
- •Глава 2 уравнения состояния вещества
- •2.1. Термические и калорические уравнения состояния
- •2.2. Термические уравнения состояния для идеального газа
- •2.3. Термические уравнения состояния для реальных газов
- •Глава 3. Смеси веществ
- •3.1. Способы задания состава смеси. Закон Амага.
- •3.2. Соотношения для смесей идеальных газов. Закон Дальтона
- •Глава 4. Теплоемкость
- •4.1. Виды теплоемкости
- •4.2. Уравнение Майера
- •4.3. Теплоемкость химически реагирующей термодинамической системы
- •Глава 5. Первый закон термодинамики
- •5.1. Уравнение первого закона термодинамики для сложной открытой системы в общем виде.
- •5.2. Уравнение 1-го закона термодинамики для проточной термодинамической системы
- •Глава 6. Второй закон термодинамики
- •6.1. Сущность второго закона термодинамики. Равновесные и неравновесные состояния, обратимые и необратимые процессы
- •6.2. Математическое выражение 2-го закона термодинамики. Три составляющие изменения энтропии термодинамической системы
- •6.3. Энтропия изолированной термодинамической системы
- •Глава 7. Объединенные выражения первого и второго законов термодинамики
- •7.1. Различные формы записи объединенных выражений
- •7.2. Характеристические функции и дифференциальные соотношения взаимности термодинамики
- •7.3. Максимальная и минимальная работы процесса. Термодинамические потенциалы
- •7.4. Условия равновесия термодинамической системы. Термодинамическое сродство
- •7.5. Связь между изобарной и изохорной теплоемкостями в общем виде
- •7.6.Расчетные выражения для скорости звука в общем виде
- •7.7. Максимальная и минимальная теплоты процесса
- •Глава 8. Термохимия
- •8.1. Формы записи уравнений химических реакций в общем виде
- •8.2. Понятие пробега химической реакции
- •8.3. Изохорный и изобарный тепловые эффекты химических реакций и связь между ними
- •8.4. Зависимости тепловых эффектов хр от температуры. Формула Кирхгофа.
Глава 8. Термохимия
Термохимия изучает изменение состояния ТС с неоднородными рабочими телами и химическими реакциями в них, которые сопровождаются изменением состава системы и тепловыми эффектами. Термохимия изучает тепловые эффекты химических реакций (ТЭХР).
8.1. Формы записи уравнений химических реакций в общем виде
В качестве примеров химических реакций (ХР) можно привести следующие ХР:
![]() - ХР сгорания водорода;
- ХР сгорания водорода;
![]() - ХР сгорания углерода;
- ХР сгорания углерода;
![]() -
ХР диссоциации кислорода;
-
ХР диссоциации кислорода;
![]() -
- ХР ионизации водорода;
-
- ХР ионизации водорода;
![]() -
ХР рекомбинации кислорода;
-
ХР рекомбинации кислорода;
![]() -
ХР сублимации углерода;
-
ХР сублимации углерода;
![]() -
ХР испарения воды;
-
ХР испарения воды;
![]() -
ХР конденсации водяного пара,
-
ХР конденсации водяного пара,
где (Т) – твердое вещество; (ж) – жидкое вещество; (Г) – газообразное вещество. Обозначение (Г) обычно отпускается, т.к. большинство рассматриваемых реагентов является газообразными веществами.
При химических реакциях вещества
реагируют друг с другом в строго
определенных отношениях, характеризуемых
стехиометрическими коэффициентами
компонентов реакции -
![]() ,
гдеi=1, 2, 3,… и т.д.
,
гдеi=1, 2, 3,… и т.д.
Первая форма записи уравнения произвольной ХР:
![]()
или
![]() ,
,
где
![]() - стехиометрический коэффициентi-го
исходного вещества;
- стехиометрический коэффициентi-го
исходного вещества; - стехиометрический коэффициентi-го
продукта реакции;
- стехиометрический коэффициентi-го
продукта реакции;![]() - символi-го исходного
вещества;
- символi-го исходного
вещества; - символi-го продукта
реакции.
- символi-го продукта
реакции.
Вторая форма записи уравнения произвольной ХР может быть получена если все слагаемые уравнения ХР перенести в сторону продуктов ХР:
![]() ,
,
где
![]() и
и![]() ,
т.е. стехиометрические коэффициенты
левой части уравнения ХР считаются
отрицательными, т.к. они убывают в ходе
прямой ХР, а коэффициенты правой части
уравнения ХР считаются положительными.
В этой форме записи уравнение ХР может
быть представлена в виде:
,
т.е. стехиометрические коэффициенты
левой части уравнения ХР считаются
отрицательными, т.к. они убывают в ходе
прямой ХР, а коэффициенты правой части
уравнения ХР считаются положительными.
В этой форме записи уравнение ХР может
быть представлена в виде:
![]()
Например, для ХР сгорания водорода:
2Н2+ О2=2Н2О,
имеем для первой формы записи уравнения ХР:
![]()
и для второй формы записи уравнения ХР:
2Н2О – 2Н2– О2=0
имеем:
![]()
При подсчете чисел молей принято не принимать во внимание жидкие и твердые тела.
Например, для ХР:
![]() ,
имеем
,
имеем![]() .
.
8.2. Понятие пробега химической реакции
При химических реакциях изменения количеств реагирующих компонентов пропорциональны их стехиометрическим коэффициентам:
![]() ,
,
где ni– текущее значение количества веществаi-го компонента при
протекании ХР;![]() - количество веществаi-го
реагента в начальный момент ХР;
- количество веществаi-го
реагента в начальный момент ХР;![]() - пробег химической реакции.
- пробег химической реакции.
Величина пробега ХР
![]() характеризует степень изменения состава
термодинамической системы при химической
реакции и показывает на сколько сдвинулась
химическая реакция по отношению к
начальному состоянию системы.
характеризует степень изменения состава
термодинамической системы при химической
реакции и показывает на сколько сдвинулась
химическая реакция по отношению к
начальному состоянию системы.
В начальный момент химической реакции
принимается, что
![]() =0.
=0.
Рассмотрим термодинамическую систему, в которой протекает лишь одна ХР. В реакции могут участвовать не все вещества, входящие в рабочее тело. Однако присутствие веществ, не участвующих в химической реакции, влияет на ход ее протекания.
Текущее число молей i-го
вещества равно![]() ,
гдеi=1, 2, …КС – число
веществ в системе. Для веществ левой
части уравнения ХР:
,
гдеi=1, 2, …КС – число
веществ в системе. Для веществ левой
части уравнения ХР:![]() ,
и для веществ правой части уравнения
ХР:
,
и для веществ правой части уравнения
ХР:![]() .
.
Стехиометрический коэффициент i-го
компонентаviпоказывает, на сколько должно измениться
число молей этого компонента при ХР.
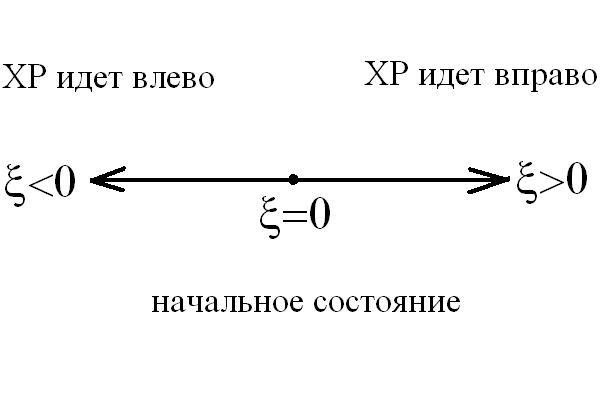
Если ХР идет вправо, т.е. пробег ХР![]() >0,
то исходные вещества убывают, а продукты
реакции увеличиваются. Если ХР идет
влево, т.е. пробег ХР
>0,
то исходные вещества убывают, а продукты
реакции увеличиваются. Если ХР идет
влево, т.е. пробег ХР![]() <0,
то продукты реакции убывают, а количество
исходных веществ увеличивается, как
это показано на схеме:
<0,
то продукты реакции убывают, а количество
исходных веществ увеличивается, как
это показано на схеме:
Стехиометрические коэффициенты
![]() - безразмерные величины. Пробег химической
реакции
- безразмерные величины. Пробег химической
реакции![]() имеет размерность – [моль].
имеет размерность – [моль].
С физической точки зрения пробег
химической реакции – это число
элементарных реакций, измеряемое числами
молей. Если химическая реакция прошла
путь от
![]() =0
до
=0
до![]() =1
, то это означает, что произошло число
элементарных реакций, равное числу
АвагадроNA=6,022·1023.
В общем случае число элементарных
реакций равно произведению числа
Авагадро на пробег ХР, т.е. произведениюNA·
=1
, то это означает, что произошло число
элементарных реакций, равное числу
АвагадроNA=6,022·1023.
В общем случае число элементарных
реакций равно произведению числа
Авагадро на пробег ХР, т.е. произведениюNA·![]() .
.
Изменение количеств реагирующих веществ
в процессе ХР при пути ХР от
![]() =0
до
=0
до![]() =1
можно проиллюстрировать следующей
таблицей:
=1
можно проиллюстрировать следующей
таблицей:
|
|
Исходные вещества |
Продукты реакции |
|
|
Начальный момент ХР |
|
|
0 |
|
Конечный момент ХР |
|
|
1 |

