
- •Передмова
- •Мета і завдання дисципліни, її місце у навчальному процесі
- •Загальні вказівки до вивчення дисципліни
- •Вказівки до самостійної роботи
- •Вказівки щодо розв'язування задач
- •Вимоги до оформлення контрольних робіт
- •Спектральні закономірності водню
- •Модель воднеподібного атома по Бору
- •Потенціали збудження та іонізації
- •Хвильові властивості речовини
- •Рівняння Шредінгера
- •Атом водню у квантовій механіці
- •Хвилі де Бройля
- •Співвідношення невизначеностей
- •Квантування орбітального моменту імпульсу електрона
- •Квантування орбітального магнітного моменту електрона
- •Спін електрона. Заповнення електронних оболонок і шарів.
- •Частинка у потенціальній ямі
- •Закономірності радіоактивних процесів
- •Поняття про ядерні реакції
- •Тинок,вони перетворювались на ядра ізотопу фосфору із викидом нейтронів:
- •Будова ядра
- •Дефект маси і енергія звязку ядра
- •Явище радіоактивного розпаду
- •Ядерні реакції
- •Енергетичний вихід ядерних реакцій
- •Рекомендована література
- •Тестові завдання з розділу “ядерна фізика”.........................................49 Будова ядра............................................………………………………………...49
- •Енергетичний вихід ядерних реакцій................................................................66
Спектральні закономірності водню
Яка спектральна лінія у спектрі водню описується формулою:
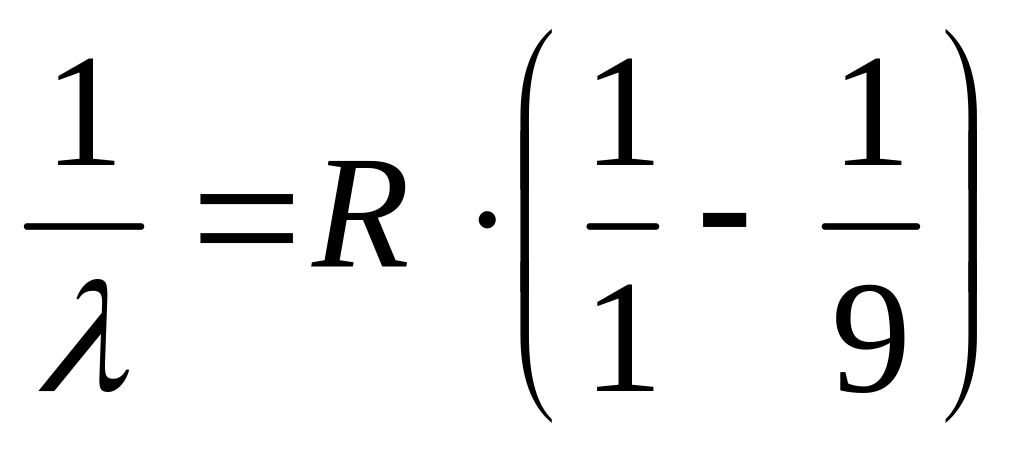 ?
?
А) Перша лінія серії Лаймана. Б) Друга лінія серії Бальмера. В) Третя лінія серії Пашена.
Г) Четверта лінія серії Бальмера. Д) Друга лінія серії Лаймана.
Яка спектральна лінія у спектрі водню описується формулою:
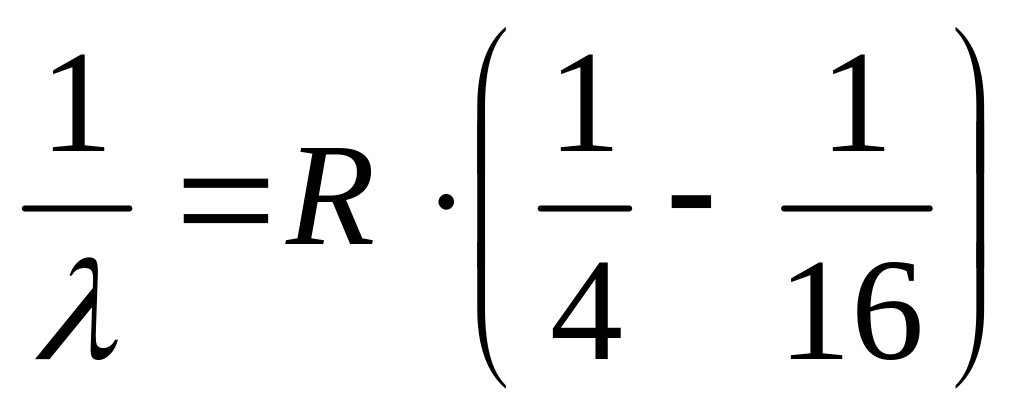 ?
?
А) Перша лінія серії Лаймана. Б) Друга лінія серії Бальмера. В) Третя лінія серії Пашена.
Г) Четверта лінія серії Бальмера. Д) Друга лінія серії Лаймана.
Яка спектральна лінія у спектрі водню описується формулою:
 ?
?
А) Перша лінія серії Пашена. Б) Друга лінія серії Лаймана. В) Третя лінія серії Пашена.
Г) Четверта лінія серії Бальмера. Д) Друга лінія серії Лаймана.
Яка спектральна лінія у спектрі водню описується формулою:
 ?
?
А) Перша лінія серії Пашена. Б) Друга лінія серії Лаймана. В) Третя лінія серії Пашена.
Г) Четверта лінія серії Бальмера. Д) Друга лінія серії Брекета.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа n відповідає лінії поглинання у серії Лаймана спектра водню ?
А) 2 та 4. Б) 3 та 1. В) 3 та 5. Г) 1 та 5. Д) 6 та 2.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа n відповідає другій лінії випромінювання у серії Лаймана спектра водню ?
А) 4 та 1. Б) 5 та 2. В) 3 та 1. Г) 4 та 3. Д) 1 та 2.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа n відповідає лінії поглинання у серії Бальмера спектра водню ?
А) 3 та 2. Б) 2 та 4. В) 1 та 3. Г) 5 та 2. Д) 4 та 1.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа n відповідає лінії випромінювання у серії Бальмера спектра водню ?
А) 2 та 4. Б) 3 та 1. В) 3 та 5. Г) 1 та 5. Д) 6 та 2.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа n відповідає лінії поглинання у серії Пашена спектра водню ?
А) 2 та 4. Б) 3 та 1. В) 3 та 5. Г) 1 та 5. Д) 6 та 3.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа n відповідає лінії випромінювання у серії Пашена спектра водню ?
А) 6 та 3. Б) 3 та 1. В) 3 та 5. Г) 5 та 1. Д) 4 та 2.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа n відповідає лінії поглинання у серії Брекета спектра водню ?
А) 4 та 2. Б) 6 та 4. В) 5 та 3. Г) 4 та 5. Д) 3 та 1.
Перехід між якими енергетичними рівнями із відповідними значеннями головного квантового числа відповідає лінії випромінювання у серії Брекета спектра водню ?
А) 2 та 4. Б) 6 та 4. В) 3 та 5. Г) 4 та 5. Д) 4 та 2.
Визначте мінімальну довжину хвилі min, що відповідає межі серії Бальмера у спектрі атома водню. (Стала Ридберга R=1,097107 м-1).
А) 464 нм. Б) 687 нм. В) 365 нм. Г) 584 нм. Д) 712 нм.
Визначте найбільшу довжину хвилі max серії Бальмера у видимій частині спектру атомарного водню.
А) 692 нм. Б) 429 нм. В) 538 нм. Г) 723 нм. Д) 656 нм.
Визначте мінімальну довжину хвилі min, що відповідає межі серії Пашена у інфрачервоній частині спектру атома водню. (Стала Ридберга R=1,097107 м-1).
А) 890 нм. Б) 1040 нм. В) 960 нм. Г) 820 нм. Д) 780 нм.
Визначте найбільшу довжину хвилі max серії Пашена у спектрі атомарного водню.
А) 4,32 мкм. Б) 1,88 мкм. В) 3,67 мкм. Г) 0,96 мкм. Д) 2,54 мкм.
Визначте мінімальну довжину хвилі min, що відповідає межі серії Брекета у інфрачервоній частині спектру атома водню. (Стала Ридберга R=1,097107 м-1).
А) 1,93 мкм. Б) 0,98 мкм. В) 1,24 мкм. Г) 2,82 мкм. Д) 1,46 мкм.
Визначте найбільшу довжину хвилі max серії Брекета у спектрі атомарного водню.
А) 6,14 мкм. Б) 2,86 мкм. В) 1,32 нм. Г) 4,05 нм. Д) 8,67 нм.
Визначте довжину хвилі у спектрі іонізованого гелію, що відповідає переходу електрона із третього енергетичного рівня на другий. (z=2).
А) 126,2 нм. Б) 164,0 нм. В) 182,8 нм. Г) 202,4 нм. Д) 328,6 нм.
Визначте довжину хвилі у спектрі двічі іонізованого літію що відповідає переходу електрона із четвертого енергетичного рівня на другий. (z=3).
А) 108 нм. Б) 36 нм. В) 54 нм. Г) 148 нм. Д) 72 нм.
Визначте довжину хвилі у спектрі тричі іонізованого берилію, що відповідає переходу електрона із третього енергетичного рівня на перший. (z=4).
А) 18,2 нм. Б) 12,8 нм. В) 32,6 нм. Г) 25,6 нм. Д) 6,4 нм.
Визначте довжину хвилі у спектрі двічі іонізованого бору, що відповідає переходу електрона із четвертого енергетичного рівня на другий. (z=5).
А) 21,3 нм. Б) 64,6 нм. В) 42,1 нм. Г) 16,8 нм. Д) 32,4 нм.
