
- •Неорганическая химия способы выражения состава растворов
- •Задачи для самостоятельного решения
- •1 Следствие
- •2 Следствие
- •Задачи для самостоятельного решения
- •Растворы сильных электролитов
- •Задачи для самостоятельного решения
- •Растворы слабых электролитов
- •Задачи для самостоятельного решения
- •Буферные растворы
- •Кривые титрования
- •Произведение растворимости
- •Задачи для самостоятельного решения
- •Окислительно-восстановительные реакции
- •Окислители и восстановители
- •Окислители.
- •Окислительно-восстановительные свойства сложных веществ
- •Влияние среды реакции.
- •Влияние среды на состав продуктов реакции
- •Влияние концентрации на состав продуктов реакции
- •Водород в реакциях с азотной кислотой практически не выделяется! Реакции серной кислоты
- •Реакции самоокисления-самовосстановления
- •Химическая связь.
- •Ковалентная связь
- •Метод валентных связей
- •Валентность
- •Гибридизация атомных орбиталей и геометрия молекул
- •Метод молекулярных орбиталей
- •Энергия связи
- •При переходе от одинарной связи двойной и тройной (между одними и теми же атомами) энергия связи возрастает, однако связь укрепляется непропорцианально увеличению её кратности.
- •Б)что длина связи уменьшается с возрастанием порядка или кратности связи, а прочность увеличивается с уменьшением длины связи.
- •Окислительно-восстановительные процессы.
- •Комплексные соединения
- •Задачи для самостоятельного решения
- •Вопросы и задачи для самостоятельного решения
- •4. Изобразите геометрическую форму ионов: ClO-, ClO3-, ClO4-.
Задачи для самостоятельного решения
1. Дайте определения понятиям «:идеальный» и «реальный» растворы, «активность», «ионная сила», «коэффициент активности иона».
2. Рассчитайте [Н3О +], [ОН -], а(Н3О+) , а(ОН-) и рН:
а) 0,01 М. раствора НС1,
б) раствора Н2SО4 с концентрацией С[0,5Н2SO4 ]= 0,01 моль/л;
в) 0,2 М раствора КОН;
г) раствора Ва(ОН)2. с концентрацией С[0,5 Ва(ОН)2]= 1 • 10-3 моль/л.
3. Рассчитайте молярную концентрацию:
а) раствора HBr, если рН раствора равно 1,65.
б) раствора NaOH, если рН раствора равно11,26.
Вычислите с учётом коэффициентов активности ионов рН водного раствора, содержащего
гидроксид натрия [w(NaOH)= 0,05%] и хлорид натрия [w(NaCl)= 0,2%],.
если плотность раствора равна 1,02 г/мл.
5. Рассчитайте рН раствора, содержащего в 2,5л одновременно 0,0032 моль HNO3 и
0,0083 моль H2SO4.
6. Вычислите рН конечного водного раствора, полученного при смешении 20 мл 0,1 М НС1 и
20 мл О,2М KOH с последующим разбавлением водой до объёма 1л.
Растворы слабых электролитов
Слабые электролиты – это электролиты, которые в растворе неполностью диссоциируют на ионы.
Свойства растворов слабых электролитов в значительной степени обусловлены существующими в них равновесиями между непродиссоциировавшими молекулами и ионами, которые образуются в результате частичной диссоциации молекул. Реакции диссоциации слабых электролитов описываются законом действующих масс и характеризуются константой и степенью диссоциации.
Согласно теории электролитической диссоциации Аррениуса, например, в водном растворе уксусная кислота распадается на ацетат ионы и ионы водорода:
CH3COOH(p) = CH3COO-(p) + H+(p)
Выражение закона действующих масс для реакции диссоциации уксусной кислоты:
![]()
К – константа равновесия, которую для реакций диссоциаций называют константой диссоциации или константой ионизации; [CH3COO-],[H+] и [CH3COOH] — равновесные концентрации ацетат- ионов, ионов водорода и молекул уксусной кислоты.
Но теория Аррениуса не учитывает влияние растворителя и нельзя, в частности, представить существование катиона Н+ в растворе, так как протон лишён электронной оболочки, меньше других ионов и очень подвижен.
Многие растворители обладают способностью переносить протоны к соответствующим акцепторам или присоединять протоны к молекуле растворителя.
Это учитывает протолитическая теория Н.Бренстеда и Т. Лоури.
Согласно этой теории вещества, способные отдавать протон, называются кислотами, а вещества , принимающие протон – основаниями.
Кислотами и основаниями могут быть как нейтральные молекулы, так и ионы.
Пример кислот: HCl, H3PO4, HCOOH, H2O, PCl5, Cl2,H3O+, [Al(H2O)6]3+,HCO3- ,NH4+.
Пример оснований: NH3, H2O, CH3NH2, C2H5OH, СаО,Cl-, CH3COO-, OH-, [Al(H2O)5OH]2+.
Некоторые вещества способны быть и донором и акцептором протонов. Такие вещества называются амфолитами. Например, H2О,HCO3-, [Al(H2O)5OH]2+.
Обратимые реакции с переносом протона от кислоты НА к основанию В называются кислотно-основными полуреакциями. Реакция между кислотой и основанием — борьба за протон между двумя основаниями:
НА + HL = LН2+ + А-
кислота 1 основание 2 кислота 2 основание 1
Кислота и получившееся при отдаче протона основание составляют сопряжённую пару.
В этом уравнении это НА и А- , LН2+ и LH.
Примеры протолитических равновесий:
HCl + H2O = H3O+ + Cl- (1)
кислота1 основание2 кислота2 основание 1
HCl + OH- = H2O + Cl- (2)
кислота 1 основание 2 кислота 2 основание 1
H2O + NH3 = NH4+ + OH- (3)
кислота 1 основание 2 кислота 2 основание 1
NH4+ + H2O = H3O+ + NH3 (4)
кислота 1 основание 2 кислота 2 основание1
Растворитель является одним из участников протолитической реакции.
Вода как амфолит обладает как кислотными , так и основными свойствами.
Такие растворители являются амфипротными. Важнейшая особенность амфипротных растворителей – способность к передаче протона от одной молекулы растворителя к другой.
H2O + H2O = H3O+ + OH-
Такие процессы, в которых одна молекула растворителя проявляет свойства кислоты, а другая – основания, называется автопротолизом.
Ион Н3О+ называется гидроксоний.
Константа автопротолиза воды Кw или Кн2о называется ионным произведением воды:
Кw = a(Н3О+)a(ОН-) = 1,0 ∙ 10-14(25оС).
Ионное произведение воды независимо от изменения концентраций ионов при неизменной температуре остаётся постоянным.
В нейтральном растворе а(Н3О+)=а(ОН-) = 10-7 моль/л
В кислой среде а(Н3О+)>а(ОН-).В щелочной среде а(Н3О+)<а(ОН-).
Кислотность среды принято оценивать по водородному показателю рН, который равен отрицательному десятичному логарифму от активности иона Н3О+ (или Н+)
рН = - lg а(Н3О+) или рН = - lg а(Н+).
При малой ионной силе, когда активность иона практически равна его концентрации
рН = -lg[H3O+] .
Аналогично гидроксильный показатель pOH = - lg a(OH-).
Или рОН = - lg[OH-]
Таким образом, в нейтральной среде рН = рОН = 7.
В кислой среде: рН < 7 , рОН >7. В щелочной среде: рН > 7, рОН < 7.
рН + рОН = 14
При взаимодействии с амфипротными растворителями, например, водой растворённые вещества могут проявлять как кислотные свойства( ур-е 4) , так и основными свойствами (ур-е 3).
Сила кислоты и основания характеризуется константами равновесий, которые называются соответственно константой кислотности Ка и константой основности Кb.
НА + НL = LН2+ + А-
кислота 1 основание 2 кислота 2 основание 1

Эта константа показывает относительную кислотность кислоты НА по отношению основанию В, т.е. является константой кислотности Ка кислоты НА.
Протолитическое равновесие в водном растворе уксусной кислоты:
СН3СООН + Н2О = СН3СОО- + Н3О+
Константа кислотности уксусной кислоты Ка показывает, что уксусная кислота является более сильной кислотой, чем вода:
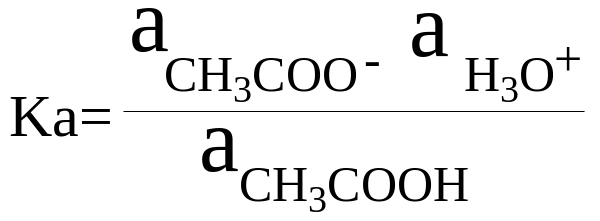
В уравнение не входит активность воды, которая принята равной единице.
Протолитическое равновесие в водном растворе соли уксусной кислоты:
СН3СОО- + Н2О = СН3СООН + ОН-
Константа этого протолитического равновесия, которая является константой основности ацетат иона:

Константа основности ацетат иона показывает, что ацетат ион является более сильным основанием, чем вода.
Константы кислотности и основности сопряжённой пары связаны между собой.
Перемножив Ка (СН3СООН) и Кb(СН3СОО-), получим:
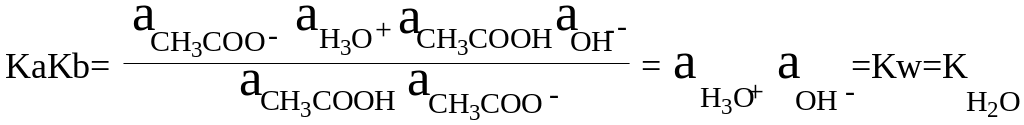
Или в общем виде:
HA + HL = LH2+ + A-
![]()
A- + HL = HA + L-
![]()
Произведение констант кислотности и основности KaKb сопряжённой пары НА и А-
равно:

Активность растворителя HL принята равной единице.
При малой ионной силе константы кислотности и основности можно выразить через концентрации:

Константы химического равновесия ,в том числе константы кислотности и основности, тоже принято выражать в логарифмической форме;
pKa = - lg Ka ,а pKb = - lg Kb
Для сопряжённых кислот и оснований pKa + pKb = 14 ( 298К)
Степень протолиза α слабого электролита представляет собой отношение концентрации одного из продуктов протолиза к равновесной концентрации протолита.
Например, степень протолиза уксусной кислоты α = [H3O+] / [CH3COOH]исх:
Математическая зависимость константы кислотности (или основности) и степень протолиза связаны законом разбавления Оствальда:
НА + Н2О = Н3О+ + А-
Если α ‹ <5% то можно считать, что Сисх = [НА]равн. и если пренебречь автопротолизом воды
Ка = [H3O+] [A-] / [HA] = [H3O+]2 / Cисх.
_______
[H3O+] = √Ka Cисх.
Если α > 5% , то [HA]равн ≠ Сисх. и тогда [НА]равн. = Сисх – [Н3О+]
Ка = [Н3О+] [А-] / [НА] = [H3O+]2 / ( Сисх - [Н3О+] )
[H3O+]2 + Ka [H3O+] - Ka Cисх. = 0 ________________
Решая квадратное уравнение, получим: [H3O+] = 0,5 ( -Ka + √Ka2 + 4Ka Cисх. )
Например, для 0,01M молочной кислоты:
______________________
[H3O+] = 0,5 ( -1,4∙10-4 + √ 1,96∙10-8 + 4∙1,4∙0-4∙10-2 ) = 1,12∙10-4 pH = 2,95
Степень протолиза α слабого электролита представляет собой отношение концентрации одного из продуктов протолиза к равновесной концентрации протолита.
Например, степень протолиза уксусной кислоты α = [H3O+] / [CH3COOH]исх. :
Математическая зависимость константы кислотности (или основности) и степень протолиза связаны законом разбавления Оствальда:
К = α2 Сисх. / (1 – α). Так как 1 – α ≈ 1 для малой величины α, то упрощённая формула имеет вид
К = α2 Сисх.
где К – константа кислотности или основности в зависимости от вида протолиза.
Пример 1 Рассчитайте степень диссоциации, рН, с(Н3О +) и с(ОН-) в водном растворе уксусной кислоты с концентрацией 0,1моль/л. рКа(СН3СООН) = 4,76.
Решение:
Протолитическое равновесие: CH3COOH +H2O = CH3COO- + H3O+
Сопряжённые пары: кислота СН3СООН и сопряжённое с ней основание СН3СОО-,
Основание Н2О и сопряжённая с ним кислота Н3О+.
Константа протолитического равновесия- константа кислотности уксусной кислоты
Ка =
![]()
Для слабых электролитов ионная сила
мала и коэффициент активности можно
принять равным 1. Тогда: Ка =
![]()
Поскольку с(СН3СОО-) =с(Н3О+) предыдущее выражение можно представить в виде:
Ка =![]() ;
Ка·с(CH3COOH)
= c(H3O+)2
. Прологорифмировав левую и правую
часть, получим: рКа – lgc(CH3COOH)
= 2pH
;
Ка·с(CH3COOH)
= c(H3O+)2
. Прологорифмировав левую и правую
часть, получим: рКа – lgc(CH3COOH)
= 2pH
Равновесная концентрация уксусной кислоты равна исходной за вычетом концентрации, подвергнутой протолизу, т.е. сисх.- с(Н3О+)[или с(СН3СОО-), поскольку они равны]
Для слабых электролитов, в растворах которых концентрация ионов очень мала можно принять
сисх – с(Н3О+)![]() сисх.
сисх.
Тогда: 4,76 – lg0,1 = 2pH. pH = 2,88. pOH = 14 – 2,88 = 11,12.
c(H3O+) =1,32·10-3 . c(OH-) = 7,59·10-12
Степень
диссоциации(протолиза)
![]()
Пример 2. Рассчитайте [HCO3-] и [CO32-] в 0,01М растворе угольной кислоты, если рН этого раствора равен 4,5. Ка1 = 4,45∙10-7 Ка2 =4,69∙10-11 .
Решение:
Протолитические равновесия:
1 ступень: H2CO3 + H2O = HCO3- + H3O+
2 ступень: HCO3- + H2O = CO32- + H3O+
pH = 4,5. Отсюда [H3O+] = 3,16∙10-5 моль/л
Константа протолиза (константа кислотности) по первой ступени:

Отсюда [HCO3-] = 4,45∙ 10-7 ∙ 10-2 / 3,16∙10-5 = 1,41∙10-4 моль/л.

Отсюда [CO32-] = 4,69∙10-11 ∙ 1,41∙10-4 / 3,16∙10-5 = 2,09∙10-10 моль/л.
Пример 3. Вычислите концентрационную константу кислотности уксусной кислоты в водном растворе Mg(NO3)2 с концентрацией соли 0,05 моль/л, если рКо = 4,75.
Решение:
Термодинамическая константа кислотности уксусной кислоты:

Концентрационная константа кислотности уксусной кислоты:
![]()
аCH3COO- = fCH3COO- ∙[CH3COO-]; aH3O+ = fH3O+ [H3O+] ; aСH3COOH = fCH3COOH∙[CH3COOH]
Отсюда: Kо = Kc fCH3COO- fH3O+ / fCH3COOH∙, но поскольку для уксусной кислоты коэффициент активности практически равен 1, то Kc = Kо / fCH3COO- fH3O+
Ионная сила раствора в основном определяется сильным электролитом-солью:
I = 0,5( 0,05∙ 22 + 0,1∙1) = 0,15.
В соответствии с таблицей: fCH3COO- = 0,79, а fH3O+ = 0,85.
Если рКо = 4,75, то Ко = 1,78∙10-5
Тогда Кс = 1,78∙10-5 / 0,79∙0,85 = 2,65∙10-5
Пример 4. Рассчитайте рН 0,01М раствора молочной кислоты. Ка = 1,4 ∙ 10-4
Решение:
Протолитическое равновесие:
CH3CH(OH)COOH + H2O = CH3CH(OH)COO- + H3O+
Для слабых электролитов, у которых степень протолиза > 5%,
уже нельзя считать концентрацию молекул, не подвергнутых протолизу, равной исходной концентрации электролита. Поэтому для молочной кислоты:
[CH3CH(OH)COOH] = [CH3CH(OH)COOH] исх. - [H3O+]
Тогда: Ka = [H3O+] [CH3CH(OH)COOH] / [CH3CH(OH)COOH] =
[H3O+]2 / [CH3CH(OH)COOH] исх. – [H3O+]
[H3O+]2 + Ka[H3O+] - Ka[CH3CH(OH)COOH] исх. = 0
________________________________
[ H3O+]
= 0,5 ( -Ka + √ Ka2
+ 4Ka[CH3CH(OH)COOH]
исх.;
H3O+]
= 0,5 ( -Ka + √ Ka2
+ 4Ka[CH3CH(OH)COOH]
исх.;
_____________________________
[ H3O+]
= 0,5 ( -1,4 ∙10-4
+ √ (1,4 ∙ 10-4)2
+ 4 ∙ 1,4 ∙10-4
∙ 10-2
) = 1,12∙ 10-3
моль/л..
H3O+]
= 0,5 ( -1,4 ∙10-4
+ √ (1,4 ∙ 10-4)2
+ 4 ∙ 1,4 ∙10-4
∙ 10-2
) = 1,12∙ 10-3
моль/л..
pH = 2,9
Пример 5. Рассчитайте рН раствора HCN с концентрацией 10-6 моль/л . Ка = 6,2 ∙10-10
Решение:
Для слабых электролитов с концентрацией < 10-4 моль/л, у которых константа протолиза < 10-8
необходимо учитывать автопротолиз воды.
Протолитическое равновесие:
HCN + H2O = CN- + H3O+
Уравнение электронейтральности: [H3O+] = [CN-] + [OH-];
[OH-] = Kw/ [H3O+] ;
Ka = [H3O+] [CN-] / [HCN]; [CN-] = Ka [HCN] / [H3O+];
Так как очень слабая, можно считать: [HCN] = [HCN] исх.
Тогда: [H3O+] = Ka [HCN]исх. / [H3O+] + Kw/[H3O+];
[H3O+]2 = Ka [HCN]исх. + Kw;

 ___________________
__________________
___________________
__________________
[H3O+] = √ Ka [HCN]исх. + Kw = √ 6,2 ∙ 10-10 ∙ 10-6 + 10-14 = 1,03 ∙ 10-7 моь/л .
pH = 6,99.
Пример 6. Рассчитайте рН раствора ацетата натрия с концентрацией 0,1 моль/л, а также степень протолиза(гидролиза) этой соли. Ка(СН3СООН) = 1,75 ∙10-5.
Решение:
Протолитическое равновесие: CH3COO- + H2O = CH3COOH + OH-
Константа протолиза(константа основности иона ацетата):
Kb = [CH3COOH] [OH-] / [CH3COO-]
[CH3COOH] = [OH-]
а) Для приближенных расчетов можно считать, что [CH3COO-] = [CH3COO-] исх.
б) Для точных расчетов: [CH3COO-] = [CH3COO-] исх. - [OH-]
Kb = Kw/ Ka = 10-14 / 1,75 ·10-5 = 5,75 ·10-10
а) Kw/Ka = [OH-]2 / [CH3COO-]; [OH-]2 = Kw/Ka [CH3COO-];
2pOH = -lgKw + lgKa - lg[CH3COO-] = -lg10-14 + lg1,75 ∙10-5 - lg 0,1 = 10,24.
pOH = 5,12. pH = 14 - 5,12 = 8,88.
б) Kw/Ka = [OH-]2 / ([CH3COO-] исх. – [OH-]);
[OH-]2 = Kw/Ka ([CH3COO-] исх. – [OH-]);
[OH-]2 = 5,75 · 10-10 ( 0,1 – [OH-]); Пусть [OH-] = x.
x2 + 5,75·10-10 x - 5,75 ·10-10 · 0,1 = 0;
x = 7,6 ·10-6; [OH-] = 7,6 ·10-6 моль/л; рОН = 5,12. pH = 8,88.
Степень гидролиза соли: h = [OH-] / [CH3COO-] исх. = 7,6 ·10-6 / 10-1 = 7,6 ·10-5 = 0,0076%.
