
- •Неорганическая химия способы выражения состава растворов
- •Задачи для самостоятельного решения
- •1 Следствие
- •2 Следствие
- •Задачи для самостоятельного решения
- •Растворы сильных электролитов
- •Задачи для самостоятельного решения
- •Растворы слабых электролитов
- •Задачи для самостоятельного решения
- •Буферные растворы
- •Кривые титрования
- •Произведение растворимости
- •Задачи для самостоятельного решения
- •Окислительно-восстановительные реакции
- •Окислители и восстановители
- •Окислители.
- •Окислительно-восстановительные свойства сложных веществ
- •Влияние среды реакции.
- •Влияние среды на состав продуктов реакции
- •Влияние концентрации на состав продуктов реакции
- •Водород в реакциях с азотной кислотой практически не выделяется! Реакции серной кислоты
- •Реакции самоокисления-самовосстановления
- •Химическая связь.
- •Ковалентная связь
- •Метод валентных связей
- •Валентность
- •Гибридизация атомных орбиталей и геометрия молекул
- •Метод молекулярных орбиталей
- •Энергия связи
- •При переходе от одинарной связи двойной и тройной (между одними и теми же атомами) энергия связи возрастает, однако связь укрепляется непропорцианально увеличению её кратности.
- •Б)что длина связи уменьшается с возрастанием порядка или кратности связи, а прочность увеличивается с уменьшением длины связи.
- •Окислительно-восстановительные процессы.
- •Комплексные соединения
- •Задачи для самостоятельного решения
- •Вопросы и задачи для самостоятельного решения
- •4. Изобразите геометрическую форму ионов: ClO-, ClO3-, ClO4-.
Метод молекулярных орбиталей
Метод ВС широко используется химиками. В рамках этого метода большая и сложная молекула рассматривается как состоящая из отдельных двухцентровых и двухэлектронных связей. Принимается, что электроны, обусловливающие химическую связь, локализованы (расположены) между двумя атомами. К большинству молекул метод ВС может быть применен с успехом. Однако имеется ряд молекул, к которым этот метод неприменим или его выводы находятся в противоречии с опытом.
Установлено,
что в ряде случаев определяющую роль в
образовании химической связи играют
не электронные пары, а отдельные
электроны. На возможность химической
связи при помощи одного электрона
указывает существование иона H2+.
При образовании этого иона из атома
водорода и иона водорода выделяется
энергия в 255 кДж . Таким образом, химическая
связь в ионе H2+![]() довольно
прочная.
довольно
прочная.
Если попробовать описать химическую связь в молекуле кислорода по методу ВС, то придем к заключению, что, во-первых, она должна быть двойной (σ- и p-связи), во-вторых, в молекуле кислорода все электроны должны быть спарены, т.е. молекула О2 должна быть диамагнитна (у диамагнитных веществ атомы не обладают постоянным магнитным моментом и вещество выталкивается из магнитного поля). Парамагнитным веществом называется то, атомы которого или молекулы обладают магнитным моментом, и оно обладает свойством втягиваться в магнитное поле. Экспериментальные данные показывают, что по энергии связь в молекуле кислорода действительно двойная, но молекула является не диамагнитной, а парамагнитной. В ней имеется два неспаренных электрона. Метод ВС бессилен объяснить это факт.
Метод молекулярных орбиталей (МО) наиболее нагляден в его графической модели линейной комбинации атомных орбиталей (ЛКАО). Метод МО ЛКАО основан на следующих правилах.
1) При сближении атомов до расстояний химических связей из атомных орбиталей (АО) образуются молекулярные.
2) Число полученных молекулярных орбиталей равно числу исходных атомных.
3) Перекрываются атомные орбитали, близкие по энергии. В результате перекрывания двух атомных орбиталей образуются две молекулярные. Одна из них имеет меньшую энергию по сравнению с исходными атомными и называется связывающей, а вторая молекулярная орбиталь обладает большей энергией, чем исходные атомные орбитали, и называется разрыхляющей.
4) При перекрывании атомных орбиталей возможно образование и σ-связи (перекрывание по оси химической связи), и π-связи (перекрывание по обе стороны от оси химической связи).
5) Молекулярная орбиталь, не участвующая в образовании химической связи, носит название несвязывающей. Ее энергия равна энергии исходной АО.
6)На одной молекулярной орбитали (как, впрочем, и атомной) возможно нахождение не более двух электронов.
7)Электроны занимают молекулярную орбиталь с наименьшей энергией (принцип наименьшей энергии).
8)Заполнение вырожденных (с одинаковой энергией) орбиталей происходит последовательно по одному электрону на каждую из них.
Применим метод МО ЛКАО и разберем строение молекулы водорода.
Мысленно перекроем две атомные орбитали, образовав две молекулярные, одна из которых (связывающая) обладает меньшей энергией (расположена ниже), а вторая (разрыхляющая) – большей энергией (расположена выше)

Рис. 8 Энергетическая диаграмма образования молекулы Н2
Метод МО ЛКАО
позволяет наглядно объяснить образование
ионов Н2+, что вызывает
трудности в методе валентных связей.
На σ-связывающую молекулярную орбиталь
катиона Н2+переходит один
электрон атома H с выигрышем энергии.
Образуется устойчивое соединение с
энергией связи 255кДж/моль. Кратность
связи равна ½. Молекулярный ион
парамагнитен. Молекула обычного водорода
содержит уже два электрона с противоположными
спинами на σcв1s-орбитали: Энергия
связи в Н2 больше, чем в H2+![]() -
435 кДж/моль. В молекуле Н2 имеется
одинарная связь, молекула диамагнитна.
-
435 кДж/моль. В молекуле Н2 имеется
одинарная связь, молекула диамагнитна.

Рис. 9 Энергетическая диаграмма образования иона Н2+
Используя метод МО ЛКАО, рассмотрим возможность образования молекулы He2
В этом случае
два электрона займут связывающую
молекулярную орбиталь, а два других –
разрыхляющую. Выигрыша в энергии такое
заселение двух орбиталей электронами
не принесет. Следовательно, молекулы
He2 не существует.

Рис. 10 Энергетическая диаграмма, иллюстрирующая невозможность образования химической
связи между атомами He
Заполнение молекулярных орбиталей происходит при соблюдении принципа Паули и правила Хунда по мере увеличения их энергии в такой последовательности:
σ1s < σ*1s < σ2s < σ*2s < σ2pz < π2px = π2py < π*2px =π*2py < σ*2pz
Значения энергии σ2p и π2p близки и для некоторых молекул(В2,С2,N2) соотношение обратное приведённому: сначала π2p потом σ2p
Таблица 1 Энергия и порядок связи в молекулах элементов 1 периода
Молекулы и молекулярные ионы |
Электронная конфигурация |
Энергия связи кДж/моль |
Порядок связи |
Н2+ |
(σs)1 |
256 |
0,5 |
Н2 |
(σs)2(σs*)1 |
431 |
1 |
Н2- |
(σs)2(σs*)1 |
- |
0,5 |
НеН |
(σs)2(σs*)1 |
- |
0,5 |
Не2+ |
(σs)2(σs*)1 |
243 |
0,5 |
Не2 |
(σs)2(σs*)2 |
- |
0 |
Согласно методу МО порядок связи в молекуле определяется разностью между числом связывающих и разрыхляющих орбиталей, деленный на два. Порядок связи может быть равен нулю (молекула не существует), целому или дробному положительному числу. При нулевой кратности связи,как в случае Не2,молекула не образуется.
На рисунке 11 изображена энергетическая схема образования молекулярных орбиталей из атомных для двухатомных гомоядерных (одного и того же элемента) молекул элементов второго периода. Число связывающих и разрыхляющих электронов зависит от их числа в атомах исходных элементов.

Рис.11 Энергетическая диаграмма образования двухатомных молекул
элементов 2 периода
Образование молекул из атомов элементов II периода может быть записано следующим образом
(К – внутренние электронные слои):
Li 2 [KK(σs)2]
Be2 [KK(σs)2(σs*)2] молекула не обнаружена, как и молекула Не2
B2 [KK(σs)2(σs*)2 (πx)1(πy)1] молекула парамагнитна
C2 [KK(σs)2(σs*)2(πx)2(πy)2]
N2 [KK(σs)2(σs*)2(πx)2(πy)2(σz)2 ]
O2 [KK(σs)2(σs*)2(σz)2(πx)2(πy)2(πx)1(πy)1 ] молекула парамагнитна
F2 [KK(σs)2(σs*)2(σz)2(πx)2(πy)2(πx)2(πy)2 ]
Ne2 [KK(σs)2(σs*)2(σz)2 (πx)2(πy)2(πx)2(πy)2(σz*)2 ] молекула не обнаружена
Методом МО ЛКАО легко продемонстрировать парамагнитные свойства молекулы кислорода. С тем чтобы не загромождать рисунок, не будем рассматривать перекрывание 1s-орбиталей атомов кислорода первого (внутреннего) электронного слоя. Учтем, что p-орбитали второго (внешнего) электронного слоя могут перекрываться двумя способами. Одна из них перекроется с аналогичной с образованием σ-связи.
|
Рис.12 Перекрывание p-АО, направленных вдоль оси x σ-связи |
Две других p-АО перекроются по обе стороны от оси x с образованием двух π-связей.
|
Рис.13 Перекрывание p-АО, направленных вдоль оси y (z), с образованием π-связи |
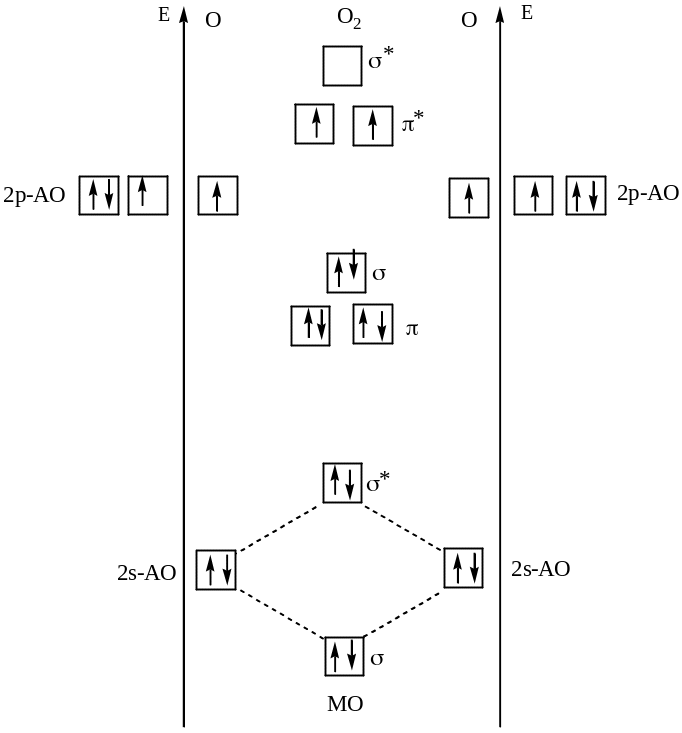
Рис. 14 Энергетическая диаграмма,иллюстрирующая с помощью метода МО ЛКАО парамагнитные свойства молекулы O2
Энергии молекулярных орбиталей могут быть определены по данным спектров поглощения веществ в ультрафиолетовой области. Так, среди молекулярных орбиталей молекулы кислорода, образовавшихся в результате перекрывания p-АО, две π-связывающие вырожденные (с одинаковой энергией) орбитали обладают меньшей энергией, чем σ-связывающая, впрочем, как и π*-разрыхляющие орбитали обладают меньшей энергией в сравнении с σ*-разрыхляющей орбиталью .
В молекуле O2 два электрона с параллельными спинами оказались на двух вырожденных
(с одинаковой энергией) π*-разрыхляющих молекулярных орбиталях. Именно наличием неспаренных электронов и обусловлены парамагнитные свойства молекулы кислорода, которые станут заметными, если охладить кислород до жидкого состояния. Так, электронная конфигурация молекул О2 описывается следующим образом:
О2 [КК(σs)2(σs*)2(σz)2(πx)2(πy)2(πx*)1(πy*)1]
Буквами КК показано, что четыре 1 s-электрона (два связывающих и два разрыхляющих) практически не оказывают влияния на химическую связь.
Поскольку три атома водорода имеют только три 1s-орбитали, то суммарное число образованных молекулярных орбиталей будет равно шести (три связывающих и три разрыхляющих). Два электрона атома азота окажутся на несвязывающей молекулярной орбитали (неподеленная электронная пара).
Наилучшим способом квантовомеханической трактовки химической связи в настоящее время считается метод молекулярных орбиталей (МО). Однако он гораздо сложнее метода ВС и не столь нагляден, как последний.
Существование связывающих и разрыхляющих МО подтверждается физическими свойствами молекул. Метод МО позволяет предвидеть, что если при образовании молекулы из атомов электроны в молекуле попадают на связывающие орбитали, то потенциалы ионизации молекул должны быть больше, чем потенциалы ионизации атомов, а если электроны попадают на разрыхляющие орбитали, то наоборот. Так, потенциалы ионизации молекул водорода и азота (связывающие орбитали) – 1485 и 1500 кДж/моль соответственно – больше, чем потенциалы ионизации атомов водорода и азота – 1310 и 1390 кДж/моль, а потенциалы ионизации молекул кислорода и фтора (разрыхляющие орбитали) – 1170 и 1523 кДж/моль – меньше, чем у соответствующих атомов – 1310 и 1670 кДж/моль. При ионизации молекул прочность связи уменьшается, если электрон удаляется со связывающей орбитали (H2 и N2), и увеличивается, если электрон удаляется с разрыхляющей орбитали(О2 и F2).
Полярность связи
Между разными атомами чистая ковалентная связь может проявляться, если электроотрицательность (ЭО) атомов одинакова. Такие молекулы электросимметричны, т.е. «центры тяжести» положительных зарядов ядер и отрицательных зарядов электронов совпадают в одной точке, поэтому их называют неполярными.
Если соединяющиеся атомы обладают различной ЭО, то электронное облако, находящееся между ними, смещается из симметричного положения ближе к атому с большей ЭО:
Смещение электронного облака называется поляризацией. В результате односторонней поляризации центры тяжести положительных и отрицательных зарядов в молекуле не совпадают в одной точке, между ними возникает некоторое расстояние (l). Такие молекулы называются полярными или диполями, а связь между атомами в них называется полярной. Например, в молекуле HCl связующее электронное облако смещено в сторону более электроотрицательного атома хлора. Таким образом, атом водорода в хлороводороде поляризован положительно, а атом хлора отрицательно.
На атоме водорода возникает положительный заряд δ= +0,18, а атоме хлора - отрицательный δ=-018. следовательно связь в молекуле хлороводорода имеет на 18% ионный характер.
Полярная связь – разновидность ковалентной связи, претерпевшей незначительную одностороннюю поляризацию. Расстояние между «центрами тяжести» положительных и отрицательных зарядов в молекуле называется длиной диполя. Естественно, что чем больше поляризация, тем больше длина диполя и больше полярность молекул. Для оценки полярности молекул обычно пользуются постоянным дипольным моментом µ, представляющим собой произведение величины элементарного электрического заряда q на длину диполя (l), т.е. µ = q∙l . Дипольные моменты измеряют в кулонометрах.
Таблица 2 Электрический момент диполя µ некоторых молекул
Молекула |
µ∙1029 Кл∙м |
Молекула |
µ∙1029 Кл∙м |
H2 |
0 |
HF |
0,640 |
N2 |
0 |
HCl |
0,347 |
CO |
0,033 |
HBr |
0,263 |
NO |
0,023 |
HI |
0,127 |
Суммарный дипольный момент сложной молекулы можно считать равным векторной сумме дипольных моментов отдельных связей. Дипольный момент обычно принято считать направленным от положительного конца диполя к отрицательному. Результат сложеиия зависит от структуры молекулы. Дипольный моиент высокосимметричных молекул BeCl2, BF3, CCl4 равен нулю, хотя связи Be - Cl, B - F, C-Cl имеют сильно полярный характер. В угловой молекуле Н2О полярные связи О-Н расположены под углом 104,5о. Поэтому молекула оказывается полярной
(µ = 0,61∙10-29 Кл∙м)
При очень большой разности электроотрицательности у атомов имеет место явная односторонняя поляризация: электронное облако связи максимально смещается в сторону атома с наибольшей электроотрицательностью, атомы переходят в противоположно заряженные ионы и возникает ионная молекула. Ковалентная связь становится ионной. Электроасимметрия молекул возрастает, длина диполя увеличивается, дипольный момент возрастает.
Предсказать полярность связи можно с помощью относительной ЭО атомов. Чем больше разность относительных ЭО атомов, тем сильнее выражена полярность. Правильнее говорить о степени ионности связи, поскольку связи не бывают ионными на 100%. Даже в соединении CsF связь ионная только на 89%.
Если рассматривать соединения элементов какого-либо периода с одним и тем же элементом, то по мере передвижения от начала к концу периода преимущественно ионный характер связи сменяется на ковалентный. Например, у фторидов 2-го периода LiF, BeF2, CF4, NF3, OF2, F2 степень ионности связи от фторида лития постепенно ослабевает и заменяется типично ковалентной связью в молекуле фтора.
Электроотрицательность серы значительно меньше, чем ЭО кислорода. Поэтому полярность связи H –S в H2S меньше полярности связи Н–О в Н2О, а длина связи H–S (0,133 нм) больше, чем Н–О (0,56 нм) и угол между связями приближается к прямому. Для H2S он составляет 92о, а для H2Se – 91o.
По этим же причинам молекула аммиака имеет пирамидальное строение и угол между валентными связями H–N–H больше прямого (107,3о). При переходе от NH3 к PH3, AsH3 и SbH3 углы между связями составляют соответственно 93,3о; 91,8о и 91,3о.
Ионная связь
Ионные молекулы существуют только в парах над нагретыми солями. Энергия разрыва ионной связи не определяется энергией притяжения ионов.
Е ионизации Cs = 3,86 эВ > Е сродства к электрону Cl = 3,83 эВ
Таким образом, даже такая «предельно ионная» молекула CsCl фактически не является ионной на 100%.
Отклонения от чисто ионной связи можно рассматривать как результат электростатического воздействия ионов друг на друга, считая их деформируемыми системами, при этом не учитывающих изменение кинетической энергии электронов и их волновые свойства.
В электрическом поле ион или молекула деформируются, т.е. в них происходит относительное смещение ядер и электронов. Такая деформируемость ионов и молекул называется поляризуемостью. Поскольку наименее прочно в атоме связаны электроны внешнего слоя, то они испытывают смещение в первую очередь.
В первом приближении поляризация иона обусловлена только деформацией внешней электронной оболочки. При одинаковых зарядах и близких радиусах поляризация минимальна у ионов с конфигурацией благородного газа и максимальна – у ионов с 18 внешними электронами.
Значительная поляризуемость ионов d-элементов объясняется большим числом внешних электронов у них. Наибольшее поляризующее действие оказывают те ионы, которые слабо поляризуются. Если катион легко деформируется, то возникший в нём диполь усиливает его поляризующее действие на анион; анион, в свою очередь, оказывает дополнительное воздействие на катион – возникает дополнительный поляризационный эффект. Дополнительный поляризационный эффект и тем самым суммарное поляризующее действие особенно велики для 18- электронных катионов(Zn2+,Cd2+,Hg 2+ и др.). Увеличение стягивания ионов в результате их поляризации приводит к тому, что длина диполя оказывается меньше межъядерного расстояния. Например, в молекуле KCl длина диполя составляет 167пм, а межъядерное расстояние – 267пм. Особенно велики различия у водородсодержащих соединений. Расстояние между ядрами водорода и галогена меньше радиуса иона галогена. Так, r(Cl-)= 181пм, в то время как расстояние между ядрами элементов равно127пм. В отличие от других катионов проникает внутрь электронной оболочки аниона. Проникновение протона внутрь аниона приводит к уменьшению длины диполя и деформируемости аниона.
С увеличением деформируемости аниона может произойти полный переход электронов от него к катиону, т.е. образуется ковалентная связь. Наоборот, чем меньше поляризация иона, тем ближе соединение к ионному типу.
Хлорид серебра растворяется в воде хуже хлорида натрия. Радиус Ag+ соизмерим с радиусом Na+, но поляризуемость больше и поэтому в AgCl межъядерное расстояние меньше, а энергия разрыва связи на ионы больше, чем в хлориде натрия.
Кислоты Н2СО3 и H2SO3 менее стабильны, чем их соли. Причины:
а) очень сильное поляризующее действие Н+ ;б) протон, внедряясь в кислородный анион, снижает его заряд и уменьшает деформируемость; поэтому HCO3- и HSO3- менее устойчивы, чем CO32- и SO32-в) второй протон делает частицу ещё менее устойчивой, поэтому H2CO3 и H2SO3легко теряют воду.
Это также является одной из причин, почему кислородсодержащие кислоты – более сильные окислители, чем их соли.
Деформируемость электронной оболочки влияет и на оптические свойства соединений Поглощение лучей связано с возбуждением внешних электронов. Электронные переходы отвечают тем меньшим энергиям, чем более поляризуема частица. Если частица малополяризуема, то возбуждение требует больших энергий, им отвечаеют ультрафиолетовые лучи. Если частица легко поляризуется, то возбуждение требует квантов небольшой энергии, им отвечает видимая часть спектра. В этом случае вещество окрашено. Так PbI2 имеет жёлтую окраску а CaI2 –бесцветен. Среди сульфидов металлов встречается гораздо больше окрашенных соединений, чем среди оксидов. В ряду PbCl2 - PbBr2- PbI2 окраска соли углубляется.
При образовании ионной связи электрическое поле иона обладает сферической симметрией и поэтому ионная связь не обладает направленностью и насыщаемостью.
Водородная связь
Водородная связь является особым видом химической связи. Известно, что соединения водорода с сильно электроотрицательными неметаллами, такими как F, О, N, имеют аномально высокие температуры кипения. Если в ряду Н2Тe – H2Se – H2S температура кипения закономерно уменьшается, то при переходе от H2S к Н2О наблюдается резкий скачок к увеличению этой температуры. Такая же картина наблюдается и в ряду галогеноводородных кислот. Это свидетельствует о наличии специфического взаимодействия между молекулами Н2О, молекулами HF. Такое взаимодействие должно затруднять отрыв молекул друг от друга, т.е. уменьшать их летучесть, а, следовательно, повышать температуру кипения соответствующих веществ. Вследствие большой разницы в ЭО химические связи H–F, H–O, H–N сильно поляризованы. Поэтому атом водорода имеет положительный эффективный заряд (δ+), а на атомах F, O и N находится избыток электронной плотности, и они заряжены отрицательно (δ-). Вследствие кулоновского притяжения происходит взаимодействие положительно заряженного атома водорода одной молекулы с электроотрицательным атомом другой молекулы. Из-за очень малого размера положительно поляризованного атома водорода и его способности глубоко внедряться в оболочку соседнего (ковалентно с ним не связанного отрицательно поляризованного атома) образуется водородная связь. Благодаря этому молекулы притягиваются друг к другу (жирными точками обозначены водородные связи). Водородная связь весьма распространена и играет важную роль в процессах растворения кристаллизации электролитической диссоциации и других физико-химических процессах.
Молекулы фторида водорода HF в твёрдом жидком и даже в газовом состоянии ассоциированы в зигзаобразные
цепочки (рис.15 ).


Рис. 15 Водородные связи в HF Рис. 16 Водородные связи в Н2О
Молекула воды может образовывать четыре водородные связи так как имеет два атома водорода и две несвязывающие электронные пары(рис.16 ).
Энергия водородной связи (21–29 кДж/моль или 5–7 ккал/моль) приблизительно в 10 раз меньше энергии обычной химической связи. И тем не менее, водородная связь обусловливает существование в парах димерных молекул (Н2О)2, (HF)2 и муравьиной кислоты. В ряду сочетаний атомов НF, HO, HN, HCl, HS энергия водородной связи падает. Она также уменьшается с повышением температуры, поэтому вещества в парообразном состоянии проявляют водородную связь лишь в незначительной степени; она характерна для веществ в жидком и твердом состояниях. Такие вещества как вода, лед, жидкий аммиак, органические кислоты, спирты и фенолы, ассоциированы в димеры, тримеры и полимеры. В жидком состоянии наиболее устойчивы димеры.
Водородные связи приблизительно в 20 раз менее прочные, чем ковалентные, но именно они заставляют воду быть жидкостью или льдом (а не газом) в обычных условиях. Водородные связи разрушаются только тогда, когда жидкая вода переходит в пар. При температурах выше 0 °С (но ниже температуры кипения) вода уже не имеет такую упорядоченную межмолекулярную структуру. Поэтому в жидкой воде молекулы связаны между собой лишь в отдельные агрегаты из нескольких молекул. Эти агрегаты могут свободно двигаться рядом друг с другом, образуя подвижную жидкость. Но при понижении температуры упорядоченность становится все больше и больше, а агрегаты – все крупнее. Наконец, образуется лед, который имеет именно такую упорядоченную структуру. В кристалле льда между молекулами остаются пустоты. Объем этих пустот больше, чем размер отдельной молекулы Н2О. Поэтому лед имеет меньшую плотность, чем жидкая вода и плавает на поверхности воды. Большинство же других веществ при замерзании увеличивает свою плотность.


