
- •Графік залежності х(t) для рівномірного
- •Одиниця прискорення руху тіла в сі
- •Як рухається тіло, якщо напрямок його
- •Формула для розрахунку проекції переміщення в разі вільного падіння тіла.
- •Динаміка №1
- •Динаміка №2
- •Вага тіла, що перебуває в стані спокою або рівномірного прямолінійного руху (в стані рівноваги)
- •Вага тіла, що рухається з прискоренням , напрямленим вертикально вгору
- •Вага тіла, що рухається з прискоренням , напрямленим вертикально вниз
- •Закони збереження в механіці
- •Розрахунок швидкості ракети за умови миттєвого згоряння палива
- •Робота сили тяжіння
- •Потенціальна енергія тіла піднятого над поверхнею Землі .
- •Потенціальна енергія пружно деформованого тіла
- •Робота сили пружності
- •Механічні коливання і хвилі.
- •Основні характеристики коливальної системи здатної здійснювати вільні коливання:
- •Г еометрична модель коливального руху.
- •Рівняння гармонічних коливань (залежність зміщення тіла від часу)
- •Чому під час коливань тіло не зупиняється в положенні рівноваги?
- •Рівняння коливань пружинного маятника
- •Опишіть коливання математичного маятника
- •Рівняння коливань математичного маятника
- •Перетворення енергії під час коливань пружинного маятника
- •Перетворення енергії під час коливань математичного маятника
- •Чим визначається частота вимушених коливань?
- •Від чого залежить амплітуда вимушених коливань?
- •Від чого залежить амплітуда коливань під час резонансу
- •Основні елементи автоколивальної системи
- •Чим відрізняються і чим подібні вільні коливання і автоколивання?
- •Чим відрізняються і чим подібні вимушені коливання і автоколивання?
- •У творення пружних хвиль
- •Основні особливості хвильового руху
- •В яких середовищах поширюються поздовжні хвилі?
- •В яких середовищах поширюються поперечні хвилі?
- •Що означає вираз: «Хвиля є періодичною у просторі і часі»
- •Основи молекулярно – кінетичної теорії
- •Експериментальні факти, що підтверджують взаємодію між молекулами:
- •Твердий стан речовини
- •Рідкий стан речовини
- •Газоподібний стан речовини
- •Зв’язок між середньою кінетичною енергії руху атомів і молекул речовини та її температурою :
- •Зв’язок між тиском і температурою ідеального газу
- •Співвідношення, що визначають зв’язок між температурним шкалами Цельсія і Кельвіна
- •Універсальна газова стала
- •Графіки ізотермічного процесу – ізотерми.
- •Графіки ізобарного процесу – ізобари
- •Графіки ізохорного процесу – ізохори
- •Властивості пари, рідини і твердих тіл
- •Чинники, що впливають на швидкість випаровування:
- •Прилади для вимірювання відносної вологості:
- •Способи збільшення відносної вологості повітря:
- •Чинники, що впливають на значення поверхневого натягу рідини:
- •Методи визначення поверхневого натягу
- •Висота підняття рідини по капіляру :
- •Властивості полімерів:
- •Основи термодинаміки
- •Розрахунок кількості теплоти , яку необхідно передати тілу при його нагріванні або яка виділяється при його охолодженні
- •Максимальний ккд теплової машини:
Розрахунок кількості теплоти , яку необхідно передати тілу при його нагріванні або яка виділяється при його охолодженні
![]()
![]() -
питома теплоємність речовини,
-
маса речовини,
-
питома теплоємність речовини,
-
маса речовини,
![]() - кінцева і початкова
- кінцева і початкова
температури
речовини ,
![]() -
зміна температури речовини.
-
зміна температури речовини.
Питома теплоємність речовини – це фізична величина, що показує, яку кількість теплоти треба передати 1кг речовини для зміни її температури на 10С.

Теплоємність тіла
 -
це
фізична величина, що показує, яку
кількість теплоти треба надати даному
тілу для зміни його температури на 10С.
-
це
фізична величина, що показує, яку
кількість теплоти треба надати даному
тілу для зміни його температури на 10С.

Зв’язок між питомою теплоємністю речовини і теплоємністю тіла
![]()
Розрахунок кількості теплоти , яка необхідна для плавлення тіла або яка виділяється під час тверднення
![]()
- маса речовини, - питома теплота плавлення.
Питома теплота плавлення - фізична величина, що показує, яку кількість теплоти треба надати 1 кг речовини, взятої при температурі плавлення, для повного переходу її в рідкий стан.
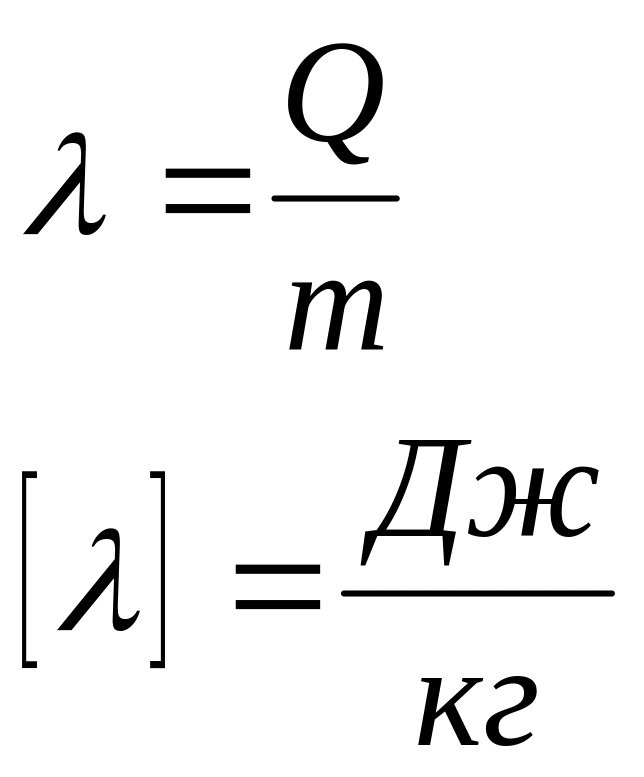
Розрахунок кількості теплоти , яка необхідна для пароутворення або яка виділяється під час конденсації
![]()
- маса речовини, - питома теплота пароутворення.
Питома теплота пароутворення - фізична величина, що показує, яку кількість теплоти треба надати 1 кг речовини, взятої при температурі кипіння, для повного переходу її в газоподібний стан.

Розрахунок кількості теплоти , яка виділяється під час згоряння палива
![]()
-
маса
речовини,
![]() -
питома теплота згоряння палива.
-
питома теплота згоряння палива.
Питома теплота згоряння палива - фізична величина, що показує, яка кількість теплоти виділяється внаслідок повного згоряння 1 кг палива.

Робота газу при ізобарному процесі
![]()
-
тиск
газу,
![]() -
початкове і кінцеве значення об’єму
газу відповідно.
-
початкове і кінцеве значення об’єму
газу відповідно.
Якщо врахувати рівняння Менделєєва – Клапейрона, то формулу для роботи газу
можна записати наступним чином
![]()
-
маса газу,
-
молярна маса,
![]() -
початкове і кінцеве значення термодинамічної
-
початкове і кінцеве значення термодинамічної
температури газу, - універсальна газова стала.
Робота газу при його розширення і стисканні: у випадку , коли газ розширюється, то напрямок дії сили тиску газу співпадає з напрямком переміщення поршня (тіла), тобто вектори сили і переміщення паралельні і кут між ними
 ,
тоді
,
тоді
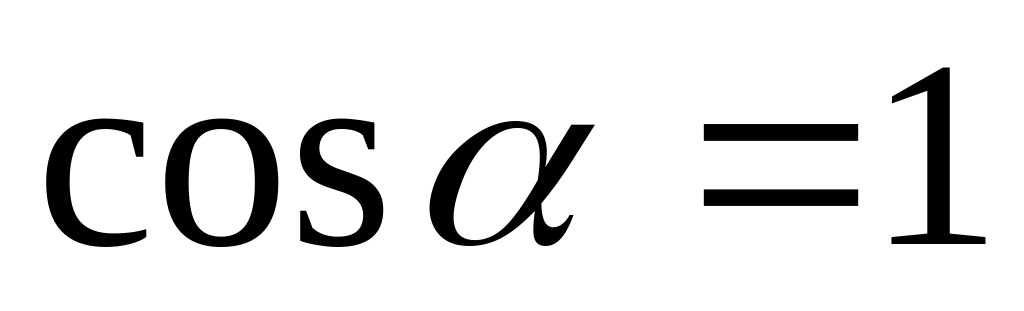 ,
а робота газу є додатною
,
а робота газу є додатною
 ;
у випадку , коли газ стискається, то
напрямок дії сили тиску газу протилежний
до напрямку переміщення поршня (тіла),
тобто вектори сили і переміщення
протилежні і кут між ними
;
у випадку , коли газ стискається, то
напрямок дії сили тиску газу протилежний
до напрямку переміщення поршня (тіла),
тобто вектори сили і переміщення
протилежні і кут між ними
 ,
тоді
,
тоді
 ,
а робота газу є від’ємною
,
а робота газу є від’ємною
 ;
;
Г
 еометричний
зміст роботи: роботу
газу при будь-якому р
еометричний
зміст роботи: роботу
газу при будь-якому р
процесі можна знайти як площу фігури під графіком р( ),
яка обмежена двома асимптотами що проходять через
початкове та кінцеве значення об’єму газу (наприклад, на А
наведеному графіку робота газу визначається як площа
прямокутної
трапеції )
![]()
![]()
Макроскопічні параметри, якими визначається робота газу: основний параметр, який характеризує виконання роботи газу є його об’єм: якщо об’єм газу зменшується, то він виконує від’ємну роботу, якщо об’єм газу збільшується, то він виконує додатну роботу, і якщо об’єм газу не змінюється, то газ не виконує роботи.
Перший закон термодинаміки: зміна внутрішньої енергії газу
 дорівнює роботі
дорівнює роботі
 ,
виконаній над газом, та кількості
теплоти
,
наданої системі:
,
виконаній над газом, та кількості
теплоти
,
наданої системі:
![]()
Перший закон термодинаміки: кількість теплоти , надана термодинамічній
системі, спричиняє зміну її внутрішньої енергії та виконання системою
роботи :
![]()
Обидва формулювання є абсолютно рівноправними і одне рівняння отримується з
Іншого,
якщо врахувати, що
![]()
«Вічний» двигун першого роду – машина, яка б нескінченно довго виконувала роботу, не дістаючи теплоти ззовні.
Для
такої машини
![]() ,
тоді
,
тоді
![]() можна записати наступним чином
можна записати наступним чином
![]() або
або
![]() ,
тобто робота може виконуватись лише за
рахунок зменшення внутрішньої енергії.
Отже можна зробити висновок: не
можна нескінченно довго виконувати
роботу за рахунок скінченного значення
внутрішньої енергії машини.
,
тобто робота може виконуватись лише за
рахунок зменшення внутрішньої енергії.
Отже можна зробити висновок: не
можна нескінченно довго виконувати
роботу за рахунок скінченного значення
внутрішньої енергії машини.
Перший закон термодинаміки для ізотермічного процесу: при ізотермічному процесі вся підведена до газу кількість теплоти йде на виконання газом роботи
![]() .
.
(Під
час ізотермічного процесу температура
газу не змінюється
![]() ,
тобто
,
тобто
![]() ,
а це означає, що внутрішня енергія
системи не змінюється
,
а це означає, що внутрішня енергія
системи не змінюється
![]() )
)
Перший закон термодинаміки для ізохорного процесу: при ізохорній зміні стану газу вся підведена до нього кількість теплоти йде на зміну внутрішньої енергії газу
![]()
(Під
час ізохорного процесу об’єм газу не
змінюється
![]() ,
тобто
,
тобто
![]() ,
а це означає, що газ не буде виконувати
роботи
,
а це означає, що газ не буде виконувати
роботи
![]() )
)
Перший закон термодинаміки для ізобарного процесу: при ізобарному розширенні кількість підведеної до газу теплоти більша за виконану ним роботу на величину, що дорівнює зростанню її внутрішньої енергії
Адіабатний процес – процес зміни стану газу, який відбувається без теплообміну з навколишніми тілами ( ).
Адіабатними можна вважати процеси, які відбуваються дуже швидко, так що теплообмін «не встигає» відбутись або процеси, які відбуваються в дуже великих об’ємах газу
Перший закон термодинаміки для адіабатного процесу: при стисканні газу без теплообміну з навколишнім середовищем його внутрішня енергія збільшується, при розширенні – зменшується.
![]()
Перший закон термодинаміки для адіабатного процесу: при адіабатному процесі робота газу здійснюється за рахунок його внутрішньої енергії
О тже
можна стверджувати, що при адіабатному
стисканні температура газу різко
збільшується, а при розширенні –
зменшується. р
тже
можна стверджувати, що при адіабатному
стисканні температура газу різко
збільшується, а при розширенні –
зменшується. р
Графік адіабатного процесу називають адіабатою.
При адіабатному розширені тиск газу зменшується
швидше ніж при ізотермічному (за одних і тих самих ізотермічний
умов), оскільки зниження тиску обумовлене не лише
збільшенням об’єму (як при ізотермічному), а й адіабатний зниженням температури. V
Оборотний процес – процес, при якому можливе повернення системи до початкового стану без будь-яких змін у навколишньому середовищі (тобто це процес, який може довільно протікати як в одному так і в іншому напрямку)
Необоротний процес - процес, при якому неможливе повернення системи до початкового стану без будь-яких змін у навколишньому середовищі (тобто це процес, який може протікати тільки в одному напрямку, в зворотному напрямку він можливий лише як ланка більш складного процесу при якому над системою виконується робота).
Другий закон термодинаміки: неможливо передати тепло від менш нагрітого тіла до більш нагрітого тіла, якщо при цьому не виконується робота.
Другий закон термодинаміки: неможливий періодичний процес, єдиним результатом якого є перетворення теплоти, отриманої від нагрівника на еквівалентну їй роботу.
«Вічний» двигун другого роду – машина, яка перетворювала б всю отриману теплову енергію на механічну роботу.
Неможливість створення такої машини пояснює другий закон термодинаміки, відповідно до якого неможливо перетворити на механічну роботу всю отриману системою кількість теплоти.
Теплові машини – машини, в яких відбувається перетворення внутрішньої енергії палива на механічну енергію (виконується робота).
 Принцип
дії теплової машини:
якщо газ в циліндрі під поршнем, який
може рухатись, нагріти, то тиск газу
збільшиться і він почне розширюватись,
штовхаючи поршень вгору. Внаслідок
теплового розширення газ виконає роботу
по підніманню поршня, але його температура
буде ще досить висока, тому для того
щоб газ зміг знову виконати таку саму
роботу його треба охолодити до початкової
температури (тоді поршень опуститься
на початкову висоту).
Принцип
дії теплової машини:
якщо газ в циліндрі під поршнем, який
може рухатись, нагріти, то тиск газу
збільшиться і він почне розширюватись,
штовхаючи поршень вгору. Внаслідок
теплового розширення газ виконає роботу
по підніманню поршня, але його температура
буде ще досить висока, тому для того
щоб газ зміг знову виконати таку саму
роботу його треба охолодити до початкової
температури (тоді поршень опуститься
на початкову висоту).К
 руговий
або замкнений цикл – термодинамічний
процес, в результаті якого робоче тіло
(газ) повертається в початковий стан.
руговий
або замкнений цикл – термодинамічний
процес, в результаті якого робоче тіло
(газ) повертається в початковий стан.Основні елементи теплової машини: робочим тілом теплової машини є газ, який отримує певну кількість теплоти
 від нагрівника, і за рахунок отриманої
енергії виконує роботу
.
Оскільки вся внутрішня енергія не може
повністю перетворитись на механічну,
то після виконання роботи температура
газу досить висока, тому для наступного
виконання
роботи газ потрібно попередньо охолодити
за допомогою
холодильника, забравши в нього не
використану енергію
від нагрівника, і за рахунок отриманої
енергії виконує роботу
.
Оскільки вся внутрішня енергія не може
повністю перетворитись на механічну,
то після виконання роботи температура
газу досить висока, тому для наступного
виконання
роботи газ потрібно попередньо охолодити
за допомогою
холодильника, забравши в нього не
використану енергію

Ц
 икл
Карно – цикл
роботи
теплової
машини, який складається з двох
ізотермічних і двох адіабатних процесів
і є найбільш вигідним. В результаті
такого циклу газ виконує роботу під
час ізотермічного (1-2) та адіабатного
(2-3) розширення, отримуючи певну кількість
теплоти
,
а робота над газом по його стисканню
виконується під час ізотермічного
(3-4) і адіабатного (4-1) стискання газу,
при цьому газ віддає певну кількість
теплоти
оточуючому середовищу. Тому робота
газу за один цикл Карно визначається
як площа фігури 1234 .
икл
Карно – цикл
роботи
теплової
машини, який складається з двох
ізотермічних і двох адіабатних процесів
і є найбільш вигідним. В результаті
такого циклу газ виконує роботу під
час ізотермічного (1-2) та адіабатного
(2-3) розширення, отримуючи певну кількість
теплоти
,
а робота над газом по його стисканню
виконується під час ізотермічного
(3-4) і адіабатного (4-1) стискання газу,
при цьому газ віддає певну кількість
теплоти
оточуючому середовищу. Тому робота
газу за один цикл Карно визначається
як площа фігури 1234 .
ККД теплової машини – фізична величина, що є характеристикою ефективності теплової машини і дорівнює відношенню роботи , виконаної машиною, до отриманої нею від нагрівника кількості теплоти
![]()
Якщо врахувати, що роботу газу , відповідно до закону збереження енергії, можна визначити як різницю між кількістю теплоти , яку отримав газ від нагрівника, і кількістю теплоти , яку газ віддав холодильнику, то формулу для ККД теплової машини можна записати наступним чином
![]() або
або
![]()
