
- •Графік залежності х(t) для рівномірного
- •Одиниця прискорення руху тіла в сі
- •Як рухається тіло, якщо напрямок його
- •Формула для розрахунку проекції переміщення в разі вільного падіння тіла.
- •Динаміка №1
- •Динаміка №2
- •Вага тіла, що перебуває в стані спокою або рівномірного прямолінійного руху (в стані рівноваги)
- •Вага тіла, що рухається з прискоренням , напрямленим вертикально вгору
- •Вага тіла, що рухається з прискоренням , напрямленим вертикально вниз
- •Закони збереження в механіці
- •Розрахунок швидкості ракети за умови миттєвого згоряння палива
- •Робота сили тяжіння
- •Потенціальна енергія тіла піднятого над поверхнею Землі .
- •Потенціальна енергія пружно деформованого тіла
- •Робота сили пружності
- •Механічні коливання і хвилі.
- •Основні характеристики коливальної системи здатної здійснювати вільні коливання:
- •Г еометрична модель коливального руху.
- •Рівняння гармонічних коливань (залежність зміщення тіла від часу)
- •Чому під час коливань тіло не зупиняється в положенні рівноваги?
- •Рівняння коливань пружинного маятника
- •Опишіть коливання математичного маятника
- •Рівняння коливань математичного маятника
- •Перетворення енергії під час коливань пружинного маятника
- •Перетворення енергії під час коливань математичного маятника
- •Чим визначається частота вимушених коливань?
- •Від чого залежить амплітуда вимушених коливань?
- •Від чого залежить амплітуда коливань під час резонансу
- •Основні елементи автоколивальної системи
- •Чим відрізняються і чим подібні вільні коливання і автоколивання?
- •Чим відрізняються і чим подібні вимушені коливання і автоколивання?
- •У творення пружних хвиль
- •Основні особливості хвильового руху
- •В яких середовищах поширюються поздовжні хвилі?
- •В яких середовищах поширюються поперечні хвилі?
- •Що означає вираз: «Хвиля є періодичною у просторі і часі»
- •Основи молекулярно – кінетичної теорії
- •Експериментальні факти, що підтверджують взаємодію між молекулами:
- •Твердий стан речовини
- •Рідкий стан речовини
- •Газоподібний стан речовини
- •Зв’язок між середньою кінетичною енергії руху атомів і молекул речовини та її температурою :
- •Зв’язок між тиском і температурою ідеального газу
- •Співвідношення, що визначають зв’язок між температурним шкалами Цельсія і Кельвіна
- •Універсальна газова стала
- •Графіки ізотермічного процесу – ізотерми.
- •Графіки ізобарного процесу – ізобари
- •Графіки ізохорного процесу – ізохори
- •Властивості пари, рідини і твердих тіл
- •Чинники, що впливають на швидкість випаровування:
- •Прилади для вимірювання відносної вологості:
- •Способи збільшення відносної вологості повітря:
- •Чинники, що впливають на значення поверхневого натягу рідини:
- •Методи визначення поверхневого натягу
- •Висота підняття рідини по капіляру :
- •Властивості полімерів:
- •Основи термодинаміки
- •Розрахунок кількості теплоти , яку необхідно передати тілу при його нагріванні або яка виділяється при його охолодженні
- •Максимальний ккд теплової машини:
Фізичні явища, що є доказом взаємодії молекул: виникнення сил пружності внаслідок деформації тіла.
Експериментальні факти, що підтверджують взаємодію між молекулами:
Два свинцеві відполіровані циліндри при стискуванні злипаються настільки сильно, що витримують підвішування до них тягаря в декілька кілограмів;
Утворення на різальних інструментах «наросту» металу, який ріжеться;
Виготовлення деталей методом порошкової металургії:
Якщо заповненні полу свинцеву кулю водою і заварити її, а потім почати стискати, то вода почне просочуватись крізь стінки кулі.
Природа сил міжмолекулярної взаємодії: електромагнітна природа.
Відстані на яких проявляються сили міжмолекулярної взаємодії: вони короткодіючі і суттєво залежать від відстані між молекулами ( сили притягання
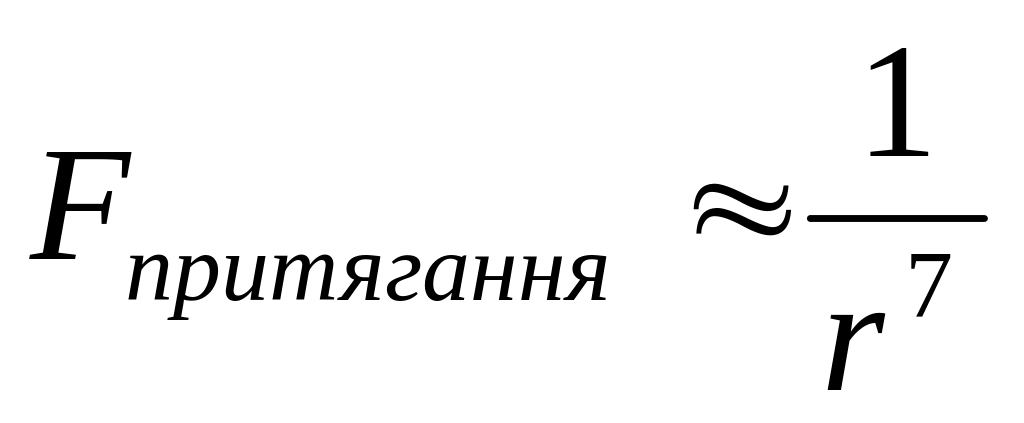 , сили відштовхування
, сили відштовхування
 ).
Сила взаємодії практично відсутня,
коли молекули знаходяться на відстанях,
що в кілька разів перевищують їх розміри.
).
Сила взаємодії практично відсутня,
коли молекули знаходяться на відстанях,
що в кілька разів перевищують їх розміри.Г
 рафік
залежності сил міжмолекулярної взаємодії
двох молекул від відстані між цими
молекулами. Залежність
сил взаємодії молекул
F
від відстані між ними можна зобразити
графічно, вважаючи сили відштовхування
додатними, а сили притягання — від'ємними.
Нехай одна з молекул знаходиться в
початку координат, а друга — на деякій
відстані г, від неї. Між ними діє дуже
мала сила взаємного притягання і ще
менша сила відштовхування. В міру
зближення молекул спочатку швидше
зростає сила притягання, а потім — сила
відштовхування. На відстані r0,
що становить приблизно суму радіусів
молекул, сила притягання дорівнює силі
відштовхування. Ця відстань OВ = г0
відповідає положенню стійкої рівноваги
молекул і називається рівноважною.
При дальшому зближенні молекул (r <
r0)
сила відштовхування переважає силу
притягання. На графіку показано також
залежність рівнодійної сил взаємодії
двох частинок від відстані між ними.
Ця сила дорівнює алгебраїчній сумі сил
відштовхування і притягання. Кожна
ордината кривої взаємодії, яка відповідає
будь-якій відстані r, є результатом
алгебраїчного додавання ординат двох
перших кривих. Крива зміни сили взаємодії
молекул показує, що при відстанях між
частинками r > r0
переважають
сили взаємного притягання, а при r <
r0
— сили відштовхування. Це пояснює
виникнення сил пружності під час
деформації тіл.
рафік
залежності сил міжмолекулярної взаємодії
двох молекул від відстані між цими
молекулами. Залежність
сил взаємодії молекул
F
від відстані між ними можна зобразити
графічно, вважаючи сили відштовхування
додатними, а сили притягання — від'ємними.
Нехай одна з молекул знаходиться в
початку координат, а друга — на деякій
відстані г, від неї. Між ними діє дуже
мала сила взаємного притягання і ще
менша сила відштовхування. В міру
зближення молекул спочатку швидше
зростає сила притягання, а потім — сила
відштовхування. На відстані r0,
що становить приблизно суму радіусів
молекул, сила притягання дорівнює силі
відштовхування. Ця відстань OВ = г0
відповідає положенню стійкої рівноваги
молекул і називається рівноважною.
При дальшому зближенні молекул (r <
r0)
сила відштовхування переважає силу
притягання. На графіку показано також
залежність рівнодійної сил взаємодії
двох частинок від відстані між ними.
Ця сила дорівнює алгебраїчній сумі сил
відштовхування і притягання. Кожна
ордината кривої взаємодії, яка відповідає
будь-якій відстані r, є результатом
алгебраїчного додавання ординат двох
перших кривих. Крива зміни сили взаємодії
молекул показує, що при відстанях між
частинками r > r0
переважають
сили взаємного притягання, а при r <
r0
— сили відштовхування. Це пояснює
виникнення сил пружності під час
деформації тіл.Основні агрегатні стани речовини: твердий, рідкий і газоподібний.
Фазовий перехід речовини у фізиці означає таку трансформацію внутрішньої структури речовин, при якій відбувається різкий стрибок певної фізичної характеристики системи, викликаний малою зміною іншої характеристики. Розрізняють фазові переходи першого і другого роду.
Різні фази тієї самої речовини можуть знаходитися у рівновазі, стикаючись одна з одною. Подібна рівновага спостерігається лише в обмеженому інтервалі температур.
Температури, при яких речовина переходить з однієї фази у іншу називають температурою переходу (перетворення).
Загалом розрізняють три температури переходу, які залежать від тиску (перша – найменше)
а) температура плавлення;
б) температура пароутворення;
в) температура сублімації (возгонки).
За умови, що зовнішній тиск є нормальним (760 мм.рт.ст.) і залишається сталим говорять про:
а) точку плавлення при переході з твердої фази у рідку або про точку затвердіння для зворотного переходу;
б) точку кипіння при переході рідини у газ (пару) або про точку зрідження (конденсації) для зворотного переходу;
в) точку сублімації (возгонки) при переході тіла у газоподібний стан (в деяких випадках такий перехід можливий за нормального тиску).
Перехід речовини з однієї фази в іншу супроводжується поглинанням або виділенням енергії, яка називається теплотою фазового перетворення. Переходи, які супроводжуються поглинанням або виділенням теплоти, називають фазовими переходами першого роду. Під час фазових переходів речовини першого роду змінюється порядок розташування молекул в речовині, характер їх руху та сили міжмолекулярної взаємодії.
