
- •1 Основное кинетическое уравнение массопередачи. Коэффициент массопередачи и движущая сила процесса.
- •2 Движущая сила массообменного процесса при нелинейной равновесной зависимости. Число единиц переноса и его физический смысл.
- •3.Выражение для средней движущей силы и числа единиц переноса при линейной равновесной зависимости.
- •4.Модифицированные уравнения массопередачи. Число единиц переноса. Высота эквивалентная единице переноса.
- •6.Массобмен в системах без твердой фазы . Молекулярная и конвективная диффузия.
- •8.Молекулярная диффузия. Первый закон Фика. Коэффициент диффузии и его физический смысл.
- •9.Уравнение Щукарева. Коэффициент масоотдачи и его физический смысл, сопоставление с коэф. Массопередачи.
- •10.Выражение коэф массопередачи через коэф массоотдачи.
- •11.Равновесие в системах газ-жидкость. Закон Генри. Ур-е равновесной зависимости. Влияние давления и температуры на абсорбцию.
- •12.Равновесие в процессах пар-ж для идеальных смесей. Закон Рауля. Диаграммы t-X-y и X-y.
- •13. Принципиальная схема противоточной абсорбции и графическое изображение процесса.
- •14. Принципиальная схема абсорбции с рециркуляцией жидкости и графическое изображение процесса.
- •15. Схема ректификационной установки непрерывного действия. Материальный баланс ректификационной колонны. Флегмовое число.
- •16. Уравнения рабочих линий процесса ректификации для непрерывно действующей ректификационной колонны. Минимальное и оптимальное флегмовое число.
- •18. Влияние флегмового числа на размеры ректификационной колонны и расход тепла при ректификации. Оптимальное флегмовое число.
- •20. Схема периодически действующей ректификационной установки. Изображение процесса в у-х диаграмме при постоянном составе дистиллята.
- •22Построение кинетической кривой и определение числа тарелок.
- •23. Порядок расчета ректификационной тарельчатой колонны.
- •24.Гидравлический расчет тарельчатых абсорбционных(ректификационных)колонн.
- •21. Тепловой баланс процесса ректификации
- •27.Непрерывная противоточная экстракция .Материальный баланс.Графическое изображение процесса.
- •28.Ступенчатая противоточная экстракция .Принципиальная схема .Графическое изображение процесса.
- •29. Многократная экстракция с противотоком растворителя.
- •30. Массопередача в системах с твёрдой фазой.Массопроводность.Диф-ные ур-ния массопров-ти.
- •31. Процесс сушки. Технические способы проведения процесса. Виды связи влаги с материалом.
- •32. Основные способы сушки. Материальный баланс конвективной сушки.
- •33 Диаграмма состояния влажного воздуха (Диаграмма Рамзина)
- •34 Изображение в диаграмме н-х процессов изменения параметров влажного воздуха. Температура точки росы, охлаждение, нагревание, смешивание.
- •35 Уравнение рабочей линии сушки. Построение рабочей линии в н-х диаграмме.
- •36 Тепловой баланс воздушной сушки. Уравнение рабочей линии процесса сушки.
- •37.Параметры, влияющие на процесс сушки. Способы интенсификации сушка.
- •38.Сушка с многократным промежуточным подогревом воздуха. Схема и н-х диаграмма.
- •39.Сушка с частичным возвратом отработанного воздуха.Схема и н-х диаграмма.
- •40.Сушка с замкнутой циркуляцией высушиваемого газа. Схема и н-х диаграмма.
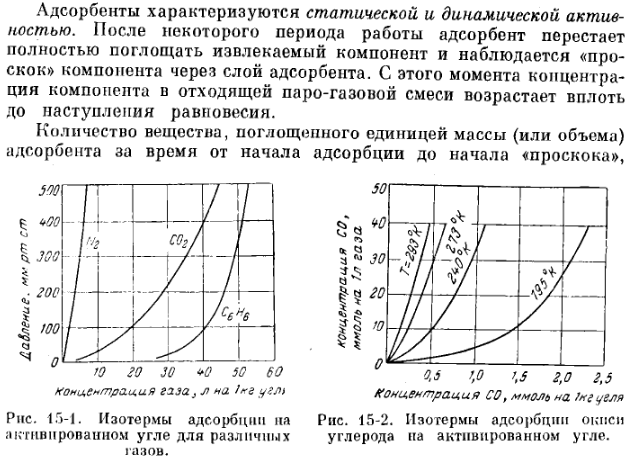
- •41. Процесс адсорбции. Динамическая и статическая активности адсорбентов. Условия, влияющие на
- •42. Физическая сущность процесса адсорбции. Адсорбенты. Условия, способствующие протеканию процесса адсорбции.
- •43. Ионообменные процессы – основные закономерности,
- •44. Кристаллизация. Основные способы проведения кристаллизация. Равновесие в процессах кристаллизации.
- •45. Мембранные процессы. Классификация мембранных процессов в зависимости от их механизма. Область применения.
- •46. Влияние различных параметров на селективность и проницаемость мембран
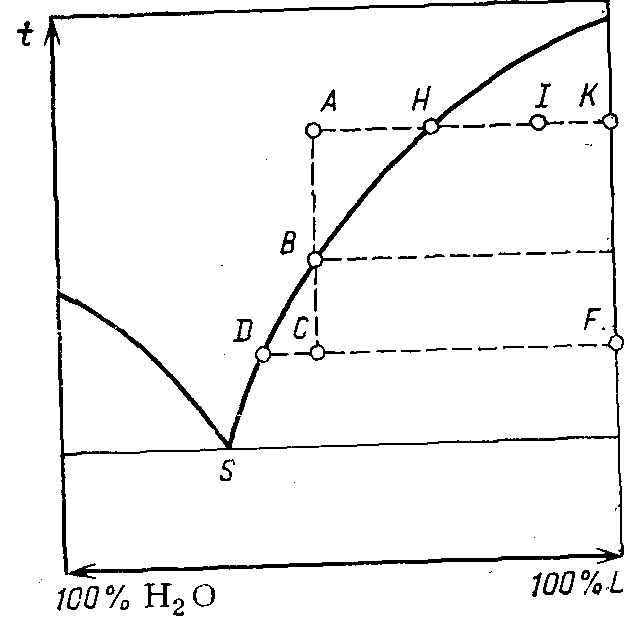
- •47. Материальный и тепловой баланс изогидрической кристаллизации
- •48. Материальный и тепловой баланс кристаллизации с удалением части растворителя.
41. Процесс адсорбции. Динамическая и статическая активности адсорбентов. Условия, влияющие на
проведение процесса адсорбции
1)

2)
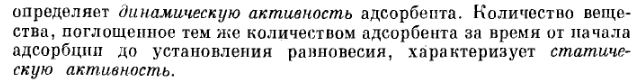

Da<Ca
3)


Так же наличие примесей в фазе, из которой поглощается вещество уменьшает равновесию активности. Равновесные кривые для адсорбции носят название изотермо-собция. И они связывают количество адсорбируемого вещества с единицей массы адсорбента.
42. Физическая сущность процесса адсорбции. Адсорбенты. Условия, способствующие протеканию процесса адсорбции.
1) Для описания физической адсорбции наиболее широкое распространение получила теория Ленгмюра:
x= A1b1c / 1+b1c x= A2b2p / 1+b2p a= A3b3y / 1+b3y
A1 A2 A3 и b1 b2 b3 – коэф., зависящие от природы адсорбента и адсорбируемых веществ и от температуры.
c и p - концентрации и порциальные давления компонентов в гзовых и жид. фазах.
y- концентрация компонентов входящий в газовую или жидкую фазу
x=a

I – для малых концентрации ( a= Гу)
II – для средних концентрации ( а= A3b3y / 1+b3y)
III – для больших концентрации (а= а стремится в бесконечности) t2>t1
2)

3


Так же наличие примесей в фазе, из которой поглощается вещество уменьшает равновесию активности. Равновесные кривые для адсорбции носят название изотермо-собция. И они связывают количество адсорбируемого вещества с единицей массы адсорбента.
43. Ионообменные процессы – основные закономерности,
область применения. Регенерация ионитов.

Используется так же в аналитических целях. Улавливание малых концентрации примеси в больших объемах; для извлечение ценных веществ ( золото из морской воды)
Особенность: селективность и обратимость.
Все иониты можно разделить на природные и искусственные.
Природные: (глина, уголь, апотиты). Недостаток: не стойки в щелочах и кислотах, что ограничивают и применение.
Искусственные: (молекулярные сито, синтетические смолы, плавленые цеолиты, гидрооксиды железа алюминия)
Ионообменные смолы состоят из матрицы ( пространственно сшитые углеродные цепи) и закрепленные на ней активные ионогеные группы ( либо при соединениях имеющихся каркасу исходного мономеров, либо в самом процессе образование высокомолекулярное соединение)
Сухая ионообменная смола ионитом не является, а становится после набухания, т.е. контакта с раствором.
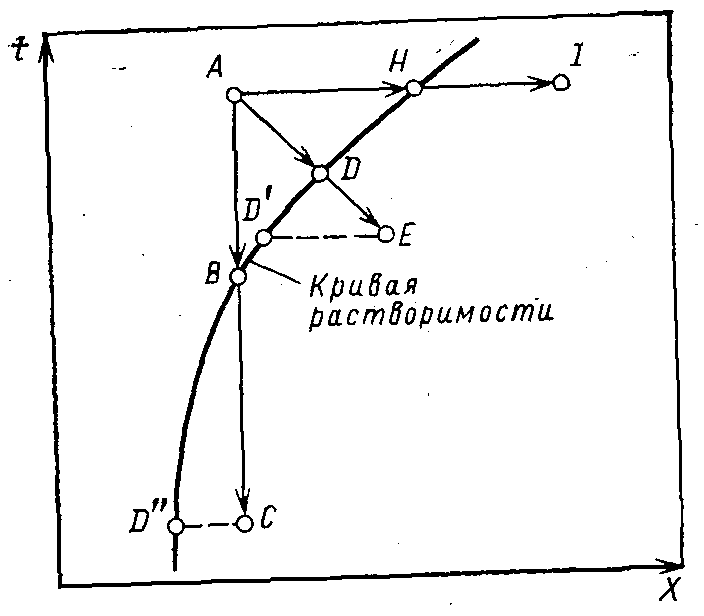
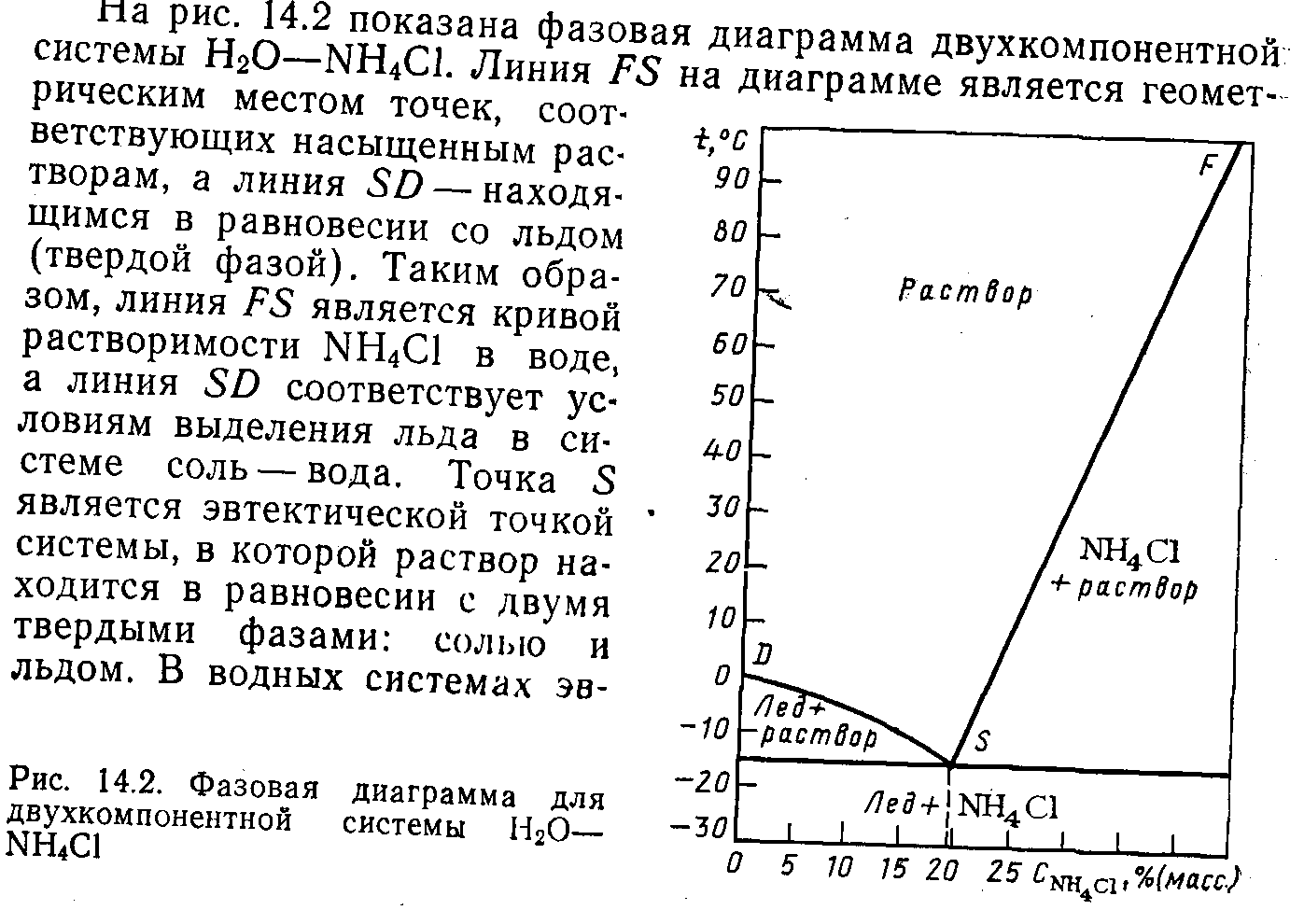
44. Кристаллизация. Основные способы проведения кристаллизация. Равновесие в процессах кристаллизации.
это массообменный процесс, выделение твердой фазы из растворов, расплавов или паров. Ж (П) – Т
Где Т – компонент.
Имеет широкое распространение, но наиболее важное место занимает в процессе производственных химических реактивов и особо чистых веществ.
Особенность: возможность получение распределенного компонента в чистом виде, что связанная с различной растворимостью, выделившегося вещества и примеси, которые остаются в растворе.




![]()



45. Мембранные процессы. Классификация мембранных процессов в зависимости от их механизма. Область применения.
Это процессы разделения смесей с помощью полупроницаемых мембран.
Применение:очистка и концентрирование растворов; разделение близкокипящих компонентов, азеотропных и нетермостойких смесей; отделение высокомолекулярных веществ от низкомолекулярных растворителей; глубокая очистка сточных вод и т.п.
«+» простота ап-го оформления; прведение процессов при t окружюсреды; экономичность с т.з. энергосбережения
«-» недолговечность функционирования мембран
Разделяемая в ап-те 1 смесь вводится в соприкосновение с полупроницаемой мембраной 2 с одной стороны. Фильтрат обогащается одним из компонентов смеси. Разделение происходит настолько полно,что в фильтрате прак-ки нет компонентов,зедержив-ся мембраной. Не прошедшая через мембрану смесь компонентов в виде концентрата выв-ся из ап-та.
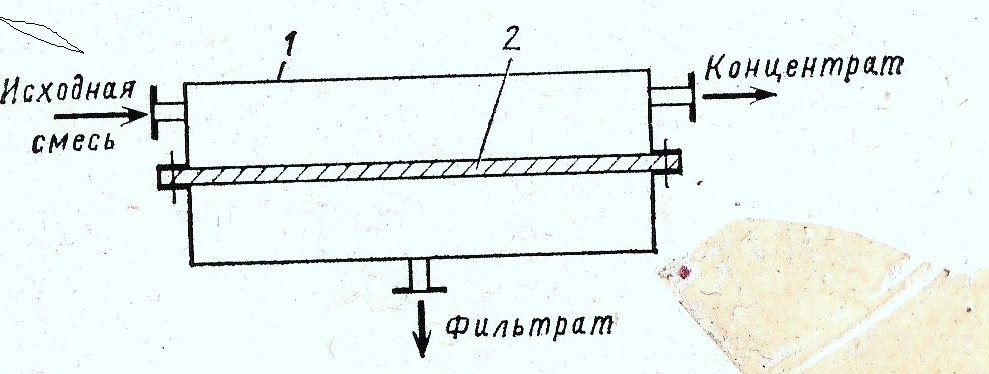
1-аппарат; 2-мембрана
Классификация:
-
Баро-мембранные процессы
Движ. сила ∆Р; служат для разделения жид. Сред и подр-ся на :
-микрофильтрация ↓ р-р задержив-х
-ультрафильтрация ↓ ч-ц ↓
-обратный осмос ↓
Микрофильтрация прим. Для очистки жид-й от коллоидных ч-ц и микроч-ц
0,02-10 мкм ∆Р= 0,1-1 МПа
Ультрафильтрация служит для разделения высокомол-х и низкомол-х соед-й в жидкой фазе 0,01-0,02 мкм ∆Р=0,3-2 МПа
Обратный осмос- прим-ся для разделения растворов низкомол-х в-в
0,0001-0,001 мкм ∆Р=1-25 МПа
-
Диффузионное разделение газовых смесей
Основано на различии коэф.диф-ии газов в непористых полимерных мембранах под действием градиента конц-й . подчиняется з-ну мол-й диф-ии
-
Испарение ж-ти через мембрану
Проникающий компонент в виде пара отводится с противоположной стороны мембраны в вакуум или поток инертного газа.
