
- •Ответы к экзамену по физике.
- •Кинематика поступательного движения материальной точки. (путь, перемещение, скорость, ускорение).
- •Ускорение и его составляющие.
- •1,2,3 Законы Ньютона.
- •Импульс тела, сила. Закон сохранения импульса.
- •Центр масс движение центра масс.
- •Уравнение движения тела переменной массы.
- •Кинематика вращательного движения материальной точки.
- •Момент силы.
- •Момент инерции твёрдого тела. Теорема Штейнера.
- •Основное уравнение динамики вращательного движения.
- •Момент импульса. Закон сохранения момента импульса.
- •Работа силы. Мощность.
- •Кинетическая и потенциальная энергия поступательного и вращательного движения.
- •Механическая энергия. Закон сохранения механической энергии.
- •Абсолютно упругий удар.
- •Абсолютно неупругий удар.
- •Поле тяготения, напряжённость, потенциал.
- •Неинерциальная система отсчёта. Силы инерции при ускоренном поступательном движении системы отсчёта.
- •Силы инерции, действующие на тело, покоящееся во вращающейся системе отсчёта.
- •Силы инерции, действующие на тело, движущееся во вращающейся системе отсчёта. Кориолисова сила.
- •Гидростатическое давление, закон Архимеда, закон неразрывности струи.
- •Закон Бернулли.
- •Формула Торричелли.
- •Внутреннее трение (вязкость). Режимы течения.
- •Метод Стокса.
- •Метод Пуазейля.
- •Поверхностное натяжение.
- •Смачивание и не смачивание.
- •Давление под искривлённой поверхностью жидкости. Формула Лапласа.
- •Капиллярные явления.
- •31. Преобразования Галлилея.
- •32. Постулаты сто. Преобразования Лоренца.
- •33. Одновременность событий в разных системах отсчёта.
- •34. Длина тел в разных системах отсчёта.
- •Длительность событий в разных системах отсчёта.
- •36. Основной закон релятивистской динамики материальной точки.
- •Закон взаимосвязи массы и энергии.
- •38. Модель идеального газа. Изозаконы.
- •39. Основное уравнение мкт.
- •40. Распределение молекул идеального газа по скоростям и энергиям теплового движения.
- •41. Барометрическая формула. Распределение Больцмана.
- •Средняя длина свободного пробега молекул.
- •Явление переноса в термодинамически неравновесных системах. Теплопроводность. Диффузия. Внутреннее трение (вязкость).
- •Теплоёмкость.
- •Диффузия.
- •Внутреннее трение (вязкость).
- •44. Число степеней свободы молекулы.
41. Барометрическая формула. Распределение Больцмана.
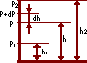
Молекулы любого газа находятся в потенциальном поле тяготения Земли. Тяготение, с одной стороны, и тепловое движение молекул – с друугой, приводят к некоторому стационирному состоянию газа, при котором давление газа с высотой убывает.
Выведем
закон изменения давления с высотой,
предполагая, что поле тяготения
однородно,температура постоянна и
масса всех молекул одинакова. Если
атмосферное давление на высоте h
равно p,
то на высоте
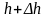 оно равно
оно равно
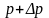 ,
значит:
,
значит:
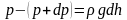 ,
где
-
плотность газа на высоте h.
Следовательно,
,
где
-
плотность газа на высоте h.
Следовательно,
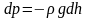 .(*)
.(*)
Воспользумся
уравнением состояния ид. газа
 ,
,
находим,
что
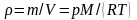 .
Подставив это выражение в (*) получим:
.
Подставив это выражение в (*) получим:
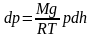 ,
или
,
или
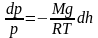 .
.
С
изменением высоты от
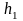 до
до
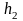 давление изменяется от
давление изменяется от
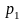 до
до
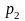 т.е.
т.е.
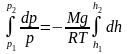 ,
,
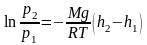 ,
или
,
или
 .
.
Это выражение называется барометрической формулой. Она позволяет найти атмосферное давление в зависимости от высоты или, измерив давление найти высоту. Этоже выражение может быть записано относительно уровня моря:
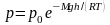 , где p-давление
на высоте h.
Прибор для определения высоты над
земной поверхностью называется
высотомером (или
альтиметром).
Давление с высотой убывает тем быстрее,
чем тяжелее газ.
, где p-давление
на высоте h.
Прибор для определения высоты над
земной поверхностью называется
высотомером (или
альтиметром).
Давление с высотой убывает тем быстрее,
чем тяжелее газ.
Эту
арометрическубю формулу можно
преобразовать, если воспользоваться
выражением
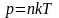 :
:
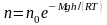 , где
, где
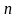 -концентрация
молекул на высоте
-концентрация
молекул на высоте
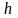 ,
,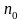 -
то же на высоте
-
то же на высоте
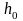 =0.
Так как
,
а
=0.
Так как
,
а
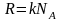 ,
то
,
то
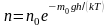 ,
где
,
где
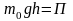 - потенциальная энергия молекулы в поле
тяготения, т.е.
- потенциальная энергия молекулы в поле
тяготения, т.е.
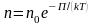 .
.
Это выражение называется распределением Больцмана во внешнем потенциальном поле. Из него следует, что при постоянной температуре плотность газа больше там, где меньше потенциальная энергия его молекул. Если частицы имеют одинаковую массу и находятся в состоянии хаотического движения, то распределение Больцмана справедливо в любом внешнем потенциальном поле, а не только в поле сил тяжести.
Средняя длина свободного пробега молекул.
Молекулы
газа, находясь в состоянии хаотического
движения, непрерывно сталкиваются друг
с другом. Между двумя столкновениями
молекулы проходят некоторый путь
 ,
который называется длиной
свободного пробега.
Т.к. мы имеем дело с большим числом
молекул, то можно говорить о средней
длине свободного пробега молекул
,
который называется длиной
свободного пробега.
Т.к. мы имеем дело с большим числом
молекул, то можно говорить о средней
длине свободного пробега молекул
 .
Минимальное расстояние, на которое
сближаются при столкновении центры
двух молекул, называется
эффективным диаметром молекулы
.
Минимальное расстояние, на которое
сближаются при столкновении центры
двух молекул, называется
эффективным диаметром молекулы
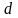 . Он зависит от скорости сталкивающихся
молекул, т.е. от темпратуры газа.
. Он зависит от скорости сталкивающихся
молекул, т.е. от темпратуры газа.
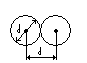
Так как
за 1с молекула проходит в среднем путь,
равный средней арифметической скорости
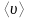 ,
и если
,
и если
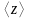 -
среднее число столкновений, испытываемых
молекулой газа за 1с, то средняя длина
свбодного пробега:
-
среднее число столкновений, испытываемых
молекулой газа за 1с, то средняя длина
свбодного пробега:
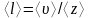 .
.![]()
Для определения : молекула столкнётся только с теми «застывшими» молекулами, центры которых находятся на расстояниях равных или меньших , т.е. лежат внутри «ломаного» цилиндра радиусом .
Среднее число столкновений за 1с равно числу молекул в объёме «ломаного» цилиндра:
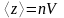 ,
где
-концентрация
молекул;
,
где
-концентрация
молекул;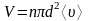 .
Таким образом,
среднее число столкновений:
.
Таким образом,
среднее число столкновений:
 .
.
Расчёты показывают, что при учёте движения других молекул:
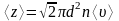 .
.
Тогда средняя длина свободного пробега:
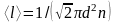 ,
т.е.
обратно пропорциональна концентрации
,
т.е.
обратно пропорциональна концентрации
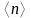 молекул. С другой стороны, из
следует, что при постоянной температуре
пропорциональна давлению
молекул. С другой стороны, из
следует, что при постоянной температуре
пропорциональна давлению
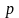 .
Следовательно,
.
Следовательно,
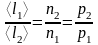 .
.
