
- •1.Техническая тд как теоретическая основа теплоэнергетики.
- •2.Первый закон термодинамики как закон сохранения и превращения энергии
- •3.Термодинамические свойства и процессы идеального газа
- •4.Смеси (смесь) идеальных газов
- •5.Обратимые и необратимые процессы.
- •6.Возрастание энтропии изолированной системы
- •7.Эксергия как мера работоспособности системы
- •8.Статистический смысл второго закона тд
- •9.Характеристические функции и дифференциальные уравнения
- •10.Формулировки и аналитическое выражение третьего закона тд гипотеза планка абсолютная энтропия
- •10.Третий закон тд
- •Отметим, что в модели идеального газа т. Н. Места нет!
- •Закон Дальтона нарушается
- •13. Вириальное уравнение состояния для умеренно сжатых газов.
- •14. Принцип соответственных состояний и подобие
Техническая термодинамика.
Лекции (70 часов) - 3,4 семестр
Практические занятия (70 часов) - 3,4 семестр
Лабораторные занятия (17 часов) - 4 семестр
Расчетные задания - 3,4 семестр
(3 семестр)
ЦЕЛИ И ЗАДАЧИ.
Знания в области производства, распределения и потребления тепловой энергии (тепловая энергия принципиально отличается от других видов энергии, пример - только тепловое излучение может быть равновесным, находиться в равновесии с окружающей средой): проектирование, эксплуатация, ремонт, монтаж, управление режимами работы тепловых энергоустановок, расчет режимов работы.
Промышленные предприятия, проектные, монтажные, наладочные и научно-исследовательские организации энергетической отрасли промышленности.
Системные знания естественнонаучного строения мира и его единства, системные принципы математического и физического моделирования процессов и явлений; методы самостоятельного обучения, развития и повышения профессиональной квалификации.
ЕСТЕСТВЕННОНАУЧНАЯ ПОДГОТОВКА
Основы высшей и вычислительной математики, спецметоды анализа теплоэнергоустановок
Основы физики и физических процессов в энергоустановках
Основы химии и химических процессов в энергоустановках
ОБЩЕТЕХНИЧЕСКАЯ ПОДГОТОВКА
Теоретические основы теплотехники:
Техническая термодинамика
Тепломассообмен
Методы расчета теплотехнических процессов и циклов, тепловых эффектов, теплотехнических устройств.
ВВЕДЕНИЕ
Термодинамика (ТД) - наука, изучающая макроскопические свойства материи и, на этой основе, закономерности превращения энергии:
рассматривает материю (вещество) как сплошную среду
для описания использует м а к р о параметры (давление, объем, температура и др., определяемые путем измерения)
“therme” - тепло, “dynamis” - сила: о силах, связанных с теплом.
Феноменологическая наука. В основе - опыт (эксперимент), два основных закона (начала), установленных опытным путем:
1-й закон - характеризует превращение энергии количественно.
2-й закон - характеризует превращение энергии качественно (направленность процесса)
Основана - в начале 19 века.
1.Техническая тд как теоретическая основа теплоэнергетики.
**ввести сокращения ТТ - ТД устройств, используемых в теплоэнергетике (и технике в целом).
ТТ - изучает:
закономерности взаимного преобразования теплоты и работы в технических устройствах
свойства рабочих тел (газы, жидкости, пары жидкостей и т.д.), процессы изменения их состояния
взаимосвязи между физическими, химическими и механическими процессами, протекающими в тепловых двигателях, холодильных установках и т.д. с помощью методов ТД
Задача ТТ - отыскание рациональных (оптимальных) способов взаимного преобразования теплоты и работы (превращения теплоты в работу и работы в теплоту).
Одна из конкретных задач - определение конечного состояния ТС в к.-л. процессе и количества затрачиваемого тепла и совершенной работы.
Для решения ее необходимо знание исходных идей ТД, ТД-метода и его математического аппарата.
Как и все науки для описания реальных объектов использует их модели и свой язык - язык ТД.
ТД-СИСТЕМА И ОКРУЖАЮЩАЯ СРЕДА
Термодинамическая система (ТС) - объект исследования в ТД. Совокупность макроскопических объектов (тел и полей), обменивающихся энергией как друг с другом, так и с внешней средой (окружающей средой).
Окружающая среда - другие тела и системы, окружающие ТС и не являющиеся объектом исследования в ТД.
РАВНОВЕСНЫЕ И НЕРАВНОВЕСНЫЕ СОСТОЯНИЯ И ПРОЦЕССЫ
Равновесное состояние ТС - состояние, характеризующееся неизменностью ТД-параметров во времени (и отсутствием в системе потоков) при постоянных внешних условиях (неизменность во времени не обусловлена протеканием какого-либо внешнего по отношению к ТС процесса).
Неpавновесное состояние ТС - состояние не удовлетворяющее вышеуказанному определению.
Равновесный процесс - непрерывная последовательность бесконечно мало отличающихся друг от друга равновесных состояний ТС, для которой процесс перехода от одного состояния к другому протекает при бесконечно малой разности параметров и ТС (при этом изменение параметров ТС происходит бесконечно медленно - с бесконечно малой скоростью)
НеРавновесный процесс - последовательность состояний, среди которых не все являются равновесными. Отличие состояний друг от друга, разность параметров и скорость изменения параметров ТС имеют определенные (конечные) значения. Все реальные процессы таковы.
РАВНОВЕСНЫЙ ПРОЦЕСС - модель реальных процессов, позволяющая описывать их при определенных условиях.
2.Первый закон термодинамики как закон сохранения и превращения энергии
Невозможен процесс возникновения или исчезновения энергии, возможен лишь процесс преобразования ее из одного вида в другой.
ТЕПЛОТА И РАБОТА - ФОРМЫ ПЕРЕДАЧИ ЭНЕРГИИ
Энергия ТС меняется в результате передачи ей (или отвода от нее) теплоты и (или) совершения ею (или над нею) работы. Теплота или работа не называются (не являются) видами энергии, а являются формами переноса энергии. Понятия теплота и работа имеют смысл (используются) для описания ТД-процесса.
РАБОТА РАСШИРЕНИЯ
Р.р. - механическая работа, совершаемая ТС против сил внешнего давления в процессе ее расширения.
Пример: цилиндр с поршнем:
![]()
p - внешнее давление, равномерно распределенное по площади взаимодействия. В случае равновесного процесса расширения внешнее давление равно давлению в ТС.
В большинстве случаев именно эта работа рассматривается в технической ТД.
Удельная работа:
![]()
Если
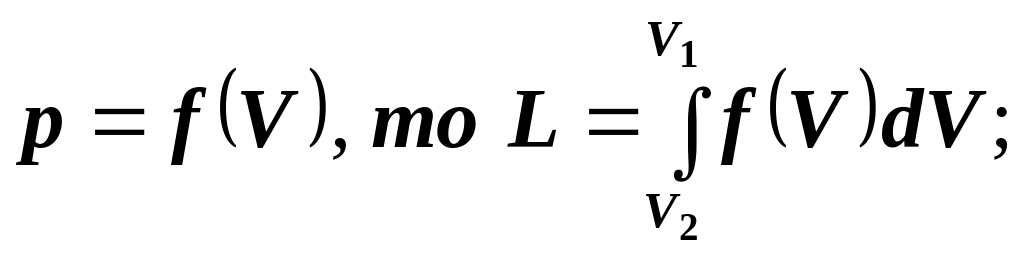
Подсчет ведется или численно, если известен аналитический вид f(v), или графически, если имеется рабочая диаграмма (график процесса в координатах p,v). На ней работа определяется как площадь под графиком p=f(v).
Работа является функцией процесса (зависит от вида процесса, т.е. вида f(v)).
ВНУТРЕННЯЯ ЭНЕРГИЯ (U) И ЭНТАЛЬПИЯ (H)
Внутренняя энергия - сумма кинетической и потенциальной энергии микрочастиц (атомов и молекул), из которых состоит ТС. Внешняя кинетическая энергия ТС (как целого) и ee внешняя потенциальная энергия (например, в поле силы тяжести или в электромагнитном поле) не являются составляющими внутренняя энергия.
является функцией состояния, т.е. значение внутренней энергии (изменение ее) не зависит от процесса (пути), в результате которого ТС пришла в данное состояние. Ее изменение одинаково для различных процессов, которые протекают между одинаковыми начальными и конечными состояниями ТС, т.е. всегда U=U2 -U1.
дифференциал ее является полным дифференциалом.
Энтальпия
(теплосодержание) -
![]() .
Также является функцией состояния, так
как определена через функцию состояния
U
и параметры состояния p
и V
.
Также является функцией состояния, так
как определена через функцию состояния
U
и параметры состояния p
и V
АНАЛИТИЧЕСКОЕ ВЫРАЖЕНИЕ ПЕРВОГО ЗАКОНА
Установлено экспериментально.
Представляет собой уравнение теплового баланса (закон сохранения энергии): dQ=dU+dL, т.е. если к ТС подводится тепло, то оно расходуется на изменение внутренней энергии и на совершение ею работы.
Частные случаи:
1.Если
![]() то
то
![]() (без подвода тепла работа может совершаться
ТС за счет уменьшения внутренней энергии)
(без подвода тепла работа может совершаться
ТС за счет уменьшения внутренней энергии)
2.Если
![]() (например,
(например,
![]() ),
то все подведенное тепло идет на
увеличение внутренней энергии ТС
),
то все подведенное тепло идет на
увеличение внутренней энергии ТС
3.Если![]() , то все подведенное тепло затрачивается
на совершение ТС работы
, то все подведенное тепло затрачивается
на совершение ТС работы
Для удельных
величин:
![]()
Физический смысл энтальпии:
![]()
и, если
![]() (т.е. в процессах с постоянным давлением
изменение энтальпии численно равно
подведенной теплоте)
(т.е. в процессах с постоянным давлением
изменение энтальпии численно равно
подведенной теплоте)
Уравнение
![]() иногда называют первой формой 1-ого
закона ТД, уравнение
иногда называют первой формой 1-ого
закона ТД, уравнение
![]() - второй формой.
- второй формой.
Закон сохранения и превращения энергии можно записать так же, как:
![]() (изменить внутреннюю
энергию ТС можно за счет подвода к ТС
тепла и совершения над нею внешней
работы dL,
например, работы сжатия).
(изменить внутреннюю
энергию ТС можно за счет подвода к ТС
тепла и совершения над нею внешней
работы dL,
например, работы сжатия).
УРАВНЕНИЕ ПЕРВОГО ЗАКОНА ТД ДЛЯ СТАЦИОНАРНОГО ОДНОМЕРНОГО ПОТОКА
Описывает изменение состояния газа при изменении положения в пространстве (1-й закон ТД справедлив для любых систем, в частности, и движущихся).
Нижеприведенное уравнение (данная модель) записывается при условии, что:
Направление и значение скорости в каждой точке постоянно во времени.
Скорость потока представляется как:
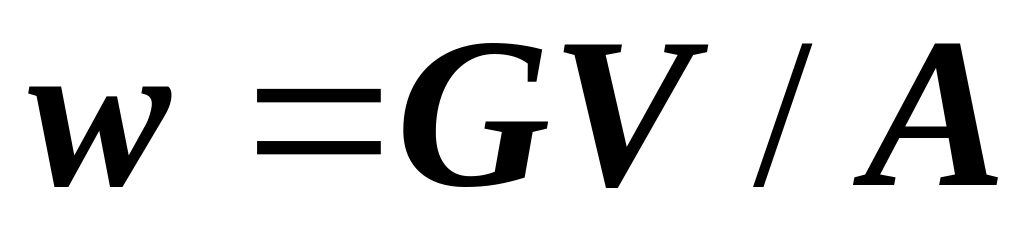 ,
где [
,
где [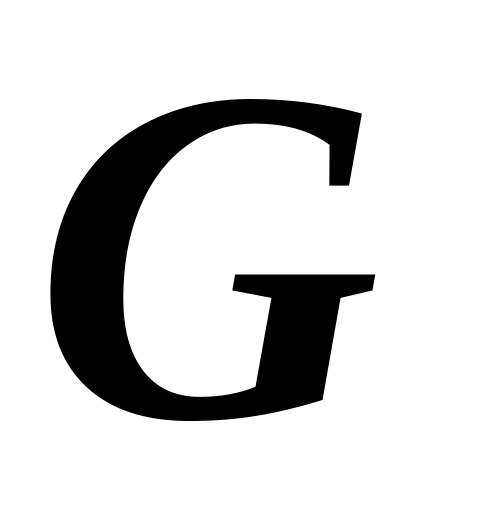 ]=кг/с
- массовый расход; [A]
= м2
- площадь поперечного сечения потока;
[v]=м3/кг
- удельный объем, причем массовый расход
]=кг/с
- массовый расход; [A]
= м2
- площадь поперечного сечения потока;
[v]=м3/кг
- удельный объем, причем массовый расход
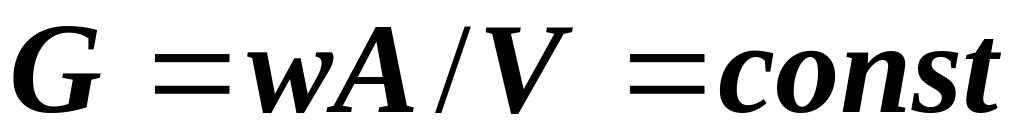 - величина постоянная (движение
установившееся, поток стационарный) в
любом сечении потока (это равенство
представляет собой уравнение сплошности
(неразрывности) потока).
- величина постоянная (движение
установившееся, поток стационарный) в
любом сечении потока (это равенство
представляет собой уравнение сплошности
(неразрывности) потока).
Тогда для единицы массы потока:
![]() ,
,
где, dl - работа против внешних сил (работа проталкивания),
d(w2/2) - энергия, расходуемая на разгон потока - изменение внешней кинетической энергии газа (располагаемая работа). Она может быть преобразована в полезную (например, механическую) работу.
Данное уравнение получено опытным путем.
Можно показать,
что работа проталкивания
![]() и тогда:
и тогда:
![]()
Видно, что теплота, подведенная к потоку, расходуется на изменение энтальпии и на приращение внешней кинетической энергии потока.
Можно показать,
что располагаемая работа
![]() .
Отсюда видно, для того, чтобы поток
разгонялся - его скорость увеличивалась,
в начале потока давление должно быть
больше.
.
Отсюда видно, для того, чтобы поток
разгонялся - его скорость увеличивалась,
в начале потока давление должно быть
больше.
Когда поток газа
в процессе движения совершает полезную
техническую работу
![]() ,
подъем газа на высоту
,
подъем газа на высоту
![]() и работу
против сил трения в трубе
и работу
против сил трения в трубе
![]() 1-й закон ТД для потока записывается
как:
1-й закон ТД для потока записывается
как:
![]()
Или
![]()
Сравним две записи 1-ого закона ТД:
общую (для произвольной системы):
и
частную (для потока):
Тогда:
![]()
Отсюда следует, что все происходящее в потоке связано с расширением газа, а также следующие возможные записи 1-го закона ТД для потока:
1.
![]()
2.
![]()
3.
Если 1-й закон
ТД написать для общего случая произвольной
ТС как:
![]() ,
то для потока одна из возможных записей
будет выглядеть:
,
то для потока одна из возможных записей
будет выглядеть:
![]()
4.
![]()
