
- •Опорные конспекты лекций по дисциплине
- •Лектор: доц. Каф. Пр-1, к.Ф.- м.Н. Игорь Михайлович Колдаев.
- •Рекомендуемая литература:
- •Дополнительная литература:
- •Тема 1. Введение. Пассивные фотометирические методы.
- •1. Объект и предмет научного исследования; модели электромагнитного излучения
- •2. Научное исследование, его цели, задачи и этапы; принцип и метод научного исследования
- •3. Систематизация оптических методов исследований, критерии качества оптического метода
- •4 Взаимосвязь световых и энергетических параметров излучения.
- •5 Типовые погрешности оэип, погрешности косвенных измерений
- •6 Способы измерения основных фотометрических параметров. Светомерный шар
- •7 Способы измерения силы света удаленного источника и яркости объекта
- •8 Способы сравнения оптических параметров объекта с мерой
- •9 Фотоплетизмография в исследованиях медико-биологических объектов
- •Задачи к теме 1.
- •Тема 2. Активные фотометрические методы
- •10 Концентрационная колориметрия в исследованиях веществ
- •11 Оптическая плотность, ее аддитивность.
- •12 Спектрофотометрический анализ многокомпонентных систем
- •13 Оксигемометрия
- •14 Комбинированные методы: фото-каллориметрия, способы термо – оптические и оптико – акустические способы регистрации сигнала
- •15 Систематизация и классификация приборов фотометрии; визуальный фотометр, фотоэлектрические фотометры.
- •1 6. Влияние отклонений от закона Бугера - Бера – Ламберта на результаты колориметрических исследований
- •17 Нефелометрические методы исследований веществ и окружающей среды
- •18 Турбидиметрия в исследованиях дисперсных сред
- •19 Методы микроскопии в исследованиях рассеивающих сред
- •Задачи к теме 3
- •Тема 3 Спектральные методы научных исследований
- •20 Цели, задачи, классификация методов и областей спектрального анализа
- •21 Классификация спектральных элементов и приборов
- •22 Развитие атомно–эмиссионной спектроскопии
- •23 Естественная ширина спектральных линий
- •24 Приборы атомно - эмиссионной спектроскопии
- •25 Принципы атомно-абсорбционной спектроскопии
- •26 Приборы абсорбционной спектроскопии
- •27 Молекулярная спектроскопия
- •Задачи к теме 3
- •Тема 4 Люминесцентные и лазерные методы
- •28 Принципы люминесцентной спектроскопии, сравнение люминесцентных и спектральных методов.
- •29 Количественный люминесцентный анализ
- •30 Методы спектроскопии комбинационного рассеяния
- •31 Лазерные спектрометры, области лазерной спектроскопии
- •32 Лазерные методы исследования сверхбыстрых процессов на примере динамики белков
- •33 Принципы рефрактометрии; молекулярная рефракция, формула Лорентц - Лоренца.
- •34 Систематизация методов и приборов рефрактометрии
- •Способы определения направления луча:
- •35 Принципы интерферометрии и голографических исследований
- •36 Волоконно-оптические и интегрально-оптические интерферометрические датчики
- •37 Классические интерферометры в научных исследованиях
- •Задачи к теме 4
- •Тема 5 Поляризационные, эллипсометрические и квантовые методы
- •38 Систематизация поляризационных исследований
- •39 Поляриметрия
- •40 Спектрополяриметрический анализ; законе Био
- •41 Приборы на основе интерференционно-поляризационных явлений
- •42 Исследование двулучепреломляющих сред
- •43 Люминесцентно – поляризационный анализ
- •44 Эллипсометрия в исследованиях поверхностных слоев и пленок
- •45 Квантовые методы исследования нанообъектов
- •Задачи к теме 5
- •Экзаменационные вопросы
- •Объект и предмет научного исследования; модели электромагнитного излучения.
Задачи к теме 3
Задача 18 (п.21). Потенциал ионизации атома рубидия составляет 4.18 эВ. Наблюдается ли в его эмиссионном спектре линии с λ< 200 нм ?.
Задача 19 (п.21). Найти спиновое расщепление уровня 4р атома кадмия, если длины волн компонент дуплета равны 769,9 нм и 766,5 нм.
Задача 20 (п.22). Вычислить волновое число и длину волны спектра эмиссии атома водорода для перехода электрона со второй на невозбуждённую орбиту. Постоянная Ридберга R = 10973,7 [м-1].
Задача 21 (п.23) Определить естественную ширину спектральной линии квантового перехода со второго на основной энергетический уровень для атома водорода. Время жизни носителя на энергетическом уровне принять равным 10 – 8 с. (Ответ: 4∙10 – 8 нм).
Задача (п.24). До какой температуры следует нагреть пары ртути, чтобы столкновения атомов обеспечивало их эмиссионное свечение? Потенциал перехода атома в возбужденное состояние принять равным 4,9 эВ.
Задача 23 (п.25). Оценить верхний температурный предел наблюдения абсорбционного спектра атомов калия. Потенциал ионизации атомов калия 4,35 эВ.
Задача 24 (п.25). Два состава нефти (А и Б) распылили в пламени атомно – абсорбционного спектрометра. Измеренные оптические плотности на длине волны линии ванадия составили 0,74 и 0,52. Вычислить массовую долю ванадия в составе Б, если в составе А она равнялась 0,1%.
Задача 25 (п.25). Два состава смеси загрязняющих атмосферу веществ (А и Б) распылили в пламени атомно – абсорбционного спектрометра. Измеренные коэффициенты пропускания на длине волны линии кадмия составили 0,82 и 0,81. Определить концентрацию кадмия в составе Б, если в составе А она равнялась 0,5 г/л. Принять приведенный удельный показатель поглощения равным ε’=7 см2/г, длину резервуара 10см.
Тема 4 Люминесцентные и лазерные методы
28 Принципы люминесцентной спектроскопии, сравнение люминесцентных и спектральных методов.
По определению
Вавилова, люминесцентным называется
излучение, избыточное над тепловым.
Люминесцентная спектроскопия
рассматривает
флуоресценцию и фосфоресценцию. Механизм
фосфоресценции поясняется 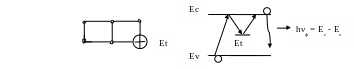 рисунком.
рисунком.
Флуоресценция наблюдается на приборе активного типа.

Основные законы люминесценции определяют принципы люминесцентных исследований.
З
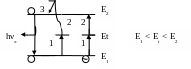 акон
Стокса:
длина волны фотолюминесценции не меньше
длины волны возбуждающего света:
акон
Стокса:
длина волны фотолюминесценции не меньше
длины волны возбуждающего света:
hνвозб ≥ hνизл,
т.е. νвозб ≥ νизл, или λизл ≥ λвозб
Однако, возможна антистоксовая люминесценция. Механизм представлен на рисунке.
Правило Коши. Спектр люминесценции не зависит от спектра и энергии возбуждения.
Правило Левшина. Спектры флуоресценции и поглощения зеркально симметричны.
Закон Вавилова. Квантовый выход фотолюминесценции не зависит от энергии возбуждающих люминесценцию квантов и определяется только веществом.
Следствие закона Вавилова:
Спектр возбуждения фотолюминесценции совпадает со спектром собственного поглощения люминесцирующего вещества.
Очевидно:
![]() .
.
Отсюда следует:
![]() .
.
Применяется формула Штерна – Фольмера:
![]() ;
;
По люминесцентному свечению различают вещества:
0,1≤ η ≤ 1 – люминофоры;
10-2< η< 10-1 – слабо люминесцирующие;
η < 10-2 – практически не люминесцирующие.
Сравним люминесцентный метод с колориметрией.
Преимущества колориметрии: относительная простота приборов и методов наблюдения. Так, устройство спектро-колориметра содержит один спектральный элемент. У флуориметра их два, так как надо контролировать две частоты: возбуждения и люминесценции.
В то же время, преимущества люминесцентного анализа по сравнению с концентрационной колориметрией следующие:
Более высокая селективность люминесцентного метода.
Чувствительность люминесцентного метода выше.
