
- •Роль физико-химических процессов в технологии и конструировании электронных средств.
- •Основные термодинамические понятия.
- •Законы термодинамики.
- •Энтропия.
- •Условия равновесия термодинамических систем. Правило фаз.
- •Диаграммы состояния различных систем и их роль при проектировании технологических процессов.
- •Однокомпонентные системы.
- •Объемные диаграммы состояния.
- •Многокомпонентные системы.
- •Основные типы диаграмм равновесия бинарных систем.
- •Статистический характер второго закона термодинамики.
- •Характеристические функции и термодинамические потенциалы системы.
- •Явления и процессы на поверхности раздела двух фаз. Адсорбция физическая и химическая.
- •Термодинамическое равновесие поверхностного слоя с объемными фазами.
- •Растворы и их применение в технологии эс.
- •Виды химической связи между атомами. Равновесное состояние системы атомов. Основные свойства материалов, определяемые особенностями химической связи.
- •Металлическая связь:
- •Молекулярная связь:
- •Пространственное расположение частиц при образовании кристалла.
- •Кристаллические решётки. Типы симметрии и виды решёток. Индексы Миллера.
- •Структура жидкости.
- •Структура полимеров.
- •Жидкие кристаллы.
- •Образование и структура пленок.
- •2. Ионно-плазменное распыление:
- •3. Электрохимическое осаждение:
- •Получение тонких пленок на ориентирующих подложках (эпитаксия).
- •Особенности структуры пленок. Влияние физико-химических факторов на структуру и свойства пленок.
- •Влияние физико-химических факторов на свойства пленок.
- •Закономерности и механизмы диффузии в полупроводниковых и планарных структурах.
- •Диффузия в твердых телах. Механизмы диффузии.
- •Законы диффузии Фика.
- •Использование диффузии для введения примеси в полупроводниковые кристаллы. Диффузия из ограниченного и неограниченного источника.
- •Физические основы ионной имплантации.
Законы термодинамики.
Первый закон термодинамики является постулатом; он не может быть по существу доказан логическим путем, а вытекает из суммы человеческого опыта. Справедливость этого закона доказывается тем, что ни одно из следствий, к которым он приводит, не находится в противоречии с опытом.
Можно дать несколько формулировок первого закона, которые по существу равноценны.
U-внутренняя энергия системы - это функция состояния системы, являющаяся суммарной мерой всех энергий системы.
Закон сохранения энергии в применении его к термодинамическим процессам является одним из выражений первого закона термодинамики.
Если в каком-нибудь процессе энергия одного вида исчезает, то взамен ее появляется энергия в другой форме в количестве, строго эквивалентном первому.
Другими словами: Внутренняя энергия системы находящейся в данном состоянии имеет одно значение и не зависит от того, каким изменениям подвергалась система при переходе к данному состоянию.
U-однозначная, непрерывная и конечная функция.
![]()
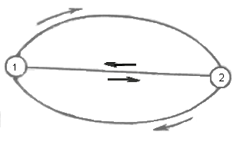
Разобьем интеграл по замкнутому контуру на 2 простых интеграла:
![]()
![]()
Приращение внутренней энергии системы при переходе её из одного состояния в другое, не зависит от пути процесса, а зависит только от начального и конечного состояния системы.
Из первого закона термодинамики нельзя определить возможность протекания процесса и его направление, что важно в конкретных случаях науки и техники.
Все процессы делятся на равновесные и неравновесные:
Равновесные процессы-процессы для течения которых не требуются затраты работы извне и в результате которых не может быть получена работа против внешних сил (передвижение шара по строго горизонтальной плоскости или качание маятника без трения).
Реальные процессы являются неравновесными.
Термодинамическая система, изменяясь, приближается к состоянию равновесия. С наступлением равновесия процесс заканчивается.
Существует два вида неравновесных процессов:
Неравновесные процессы, которые идут в направлении равновесия без воздействия внешней силы.
Обратные процессы, которые удаляют систему от состояния равновесия, и не могут идти без внешнего воздействия.
Процессы первого вида называются самопроизвольными или «положительными», процессы второго вида несамопроизвольными или «отрицательными».
В изолированной системе идут только положительные процессы, так как внешние воздействия исключены.
Второй закон термодинамики дает возможность предсказать направление хода процесса.
Существует две формулировки второго закона термодинамики:
Постулат Клаузиуса: - единственным результатом любой совокупности процессов не может быть переход теплоты от менее нагретой системы к более нагретой. Процесс теплопроводности необратим.
Постулат Томпсона: - теплота наиболее холодного тела из участвующих в круговом процессе не может служить источником работы. Самопроизвольный процесс превращения работы в теплоту (путем трения) необратим.
Энтропия.
Второй закон термодинамики вводит новую функцию состояния системы энтропию - S.
Математическое выражение для энтропии можно записать следующим образом:
![]()
![]()
Энтропия – это функция состояния системы, изменение которой равно сумме приведенных теплот поглощенных системой в равновесном состоянии.
Это однозначная, непрерывная, конечная функция состояний.
![]() -
энтропийная единица.
-
энтропийная единица.
Рассчитав энтропию S можно предсказать направление процесса, если в изолированной системе для какого-либо процесса энтропия S возрастает, процесс может идти самопроизвольно, если энтропия S уменьшается, то процесс невозможен. Если S=const, процесс равновесен, система бесконечно близка к состоянию равновесия.
Для неизолированной системы, обменивающейся с окружающей средой теплотой и работой, возможны процессы, сопровождающиеся как увеличением, так и уменьшением S.
Для того чтобы решить однозначно вопрос о направлении процесса в неизолированной системе, необходимо включить в систему все тела участвующие в процессе, сделав систему изолированной.
Условие изолированной системы можно записать так: U=const, V=const.
Признак равновесия изолированной системы заключается в том, что изолированная система находится в состоянии равновесия, если S – системы имеет максимальное значение (S=Smax) при U=const, V=const.
Математически условие S=Smax записывается так:

Третий закон термодинамики дает возможность вычислить абсолютное значение энтропии системы, с помощью постулата Планка:
Энтропия индивидуального идеального кристаллического вещества при абсолютном нуле равна нулю.
![]()
Для
реальных кристаллов энтропия
![]() .
Это подтверждено расчетами статистической
термодинамики. Это выражение справедливо
и для температуры абсолютного нуля,
поэтому для реальных кристаллов
.
Это подтверждено расчетами статистической
термодинамики. Это выражение справедливо
и для температуры абсолютного нуля,
поэтому для реальных кристаллов
![]() .
.
Для идеального твердого тела:
![]() (1)
(1)
где
![]() -
теплоемкость данного вещества при
постоянном давлении (P=const);
-
теплоемкость данного вещества при
постоянном давлении (P=const);
T- температура.
Для
большинства реальных кристаллических
веществ:
~![]() .
.
При
Т0
0
то есть
![]() .
.
Было замечено, что при Т0 к нулю стремиться не только S и , но и объем тела и давление насыщенного пара изменяются с температурой так, что их производные по температуре стремятся к нулю.
Ни какие процессы не могут снизить температуру тела до абсолютного нуля – это принцип недостижимости абсолютного нуля.
Энтропия твердого тела определяется по выражению (1).
При плавлении и переходе в жидкую фазу энтропия возрастает на величину приведенной теплоты плавления:
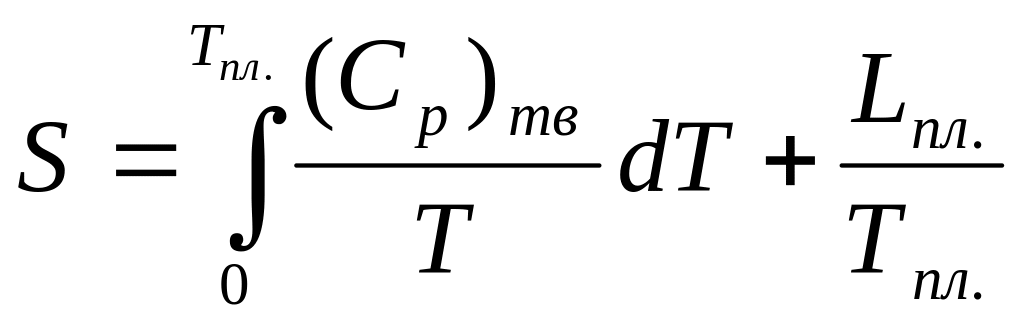 (2)
(2)
где
![]() -
теплота плавления;
-
теплота плавления;
![]() -
температура плавления.
-
температура плавления.
Если
нагреть жидкость от
до
температуры![]() ,
то получим:
,
то получим:
 (3)
(3)
Энтропия пара может быть рассчитана:
 (4)
(4)
Д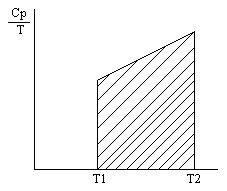 ля
практических расчетов необходимо знать
значение теплоемкости при постоянном
давлении при температуре Т=10-80К, затем
используют уравнение Дебая или Тарасова
экстраполируют значение
к абсолютному нулю. По выражению (4)
рассчитывается энтропия реального
газа.
ля
практических расчетов необходимо знать
значение теплоемкости при постоянном
давлении при температуре Т=10-80К, затем
используют уравнение Дебая или Тарасова
экстраполируют значение
к абсолютному нулю. По выражению (4)
рассчитывается энтропия реального
газа.
На
практике интегральные выражения
рассчитываются графически (см рис.) -
численное значение интеграла определяют
по площади заключенной между
![]() и
.
и
.
Энтропия зависит от молекулярного веса, агрегатного состояния (твердоежидкоегазообразное энтропия возрастает), кристаллического строения (углерод, алмаз), от структуры молекул.
