
- •Роль физико-химических процессов в технологии и конструировании электронных средств.
- •Основные термодинамические понятия.
- •Законы термодинамики.
- •Энтропия.
- •Условия равновесия термодинамических систем. Правило фаз.
- •Диаграммы состояния различных систем и их роль при проектировании технологических процессов.
- •Однокомпонентные системы.
- •Объемные диаграммы состояния.
- •Многокомпонентные системы.
- •Основные типы диаграмм равновесия бинарных систем.
- •Статистический характер второго закона термодинамики.
- •Характеристические функции и термодинамические потенциалы системы.
- •Явления и процессы на поверхности раздела двух фаз. Адсорбция физическая и химическая.
- •Термодинамическое равновесие поверхностного слоя с объемными фазами.
- •Растворы и их применение в технологии эс.
- •Виды химической связи между атомами. Равновесное состояние системы атомов. Основные свойства материалов, определяемые особенностями химической связи.
- •Металлическая связь:
- •Молекулярная связь:
- •Пространственное расположение частиц при образовании кристалла.
- •Кристаллические решётки. Типы симметрии и виды решёток. Индексы Миллера.
- •Структура жидкости.
- •Структура полимеров.
- •Жидкие кристаллы.
- •Образование и структура пленок.
- •2. Ионно-плазменное распыление:
- •3. Электрохимическое осаждение:
- •Получение тонких пленок на ориентирующих подложках (эпитаксия).
- •Особенности структуры пленок. Влияние физико-химических факторов на структуру и свойства пленок.
- •Влияние физико-химических факторов на свойства пленок.
- •Закономерности и механизмы диффузии в полупроводниковых и планарных структурах.
- •Диффузия в твердых телах. Механизмы диффузии.
- •Законы диффузии Фика.
- •Использование диффузии для введения примеси в полупроводниковые кристаллы. Диффузия из ограниченного и неограниченного источника.
- •Физические основы ионной имплантации.
Молекулярная связь:
Низкоэнергетическая связь, порядка
единиц и десятка кДж/моль, создается за
счет сил Вандервальса. Такой тип связи
создают молекулы с насыщенными химическими
связями:
![]() ,
,
![]() ,
,
![]() ,
атомы инертных газов. Так как связь
низкоэнергетическая – вещества
малоустойчивы, летучи, температура
плавления мала, прозрачны.
,
атомы инертных газов. Так как связь
низкоэнергетическая – вещества
малоустойчивы, летучи, температура
плавления мала, прозрачны.
Пространственное расположение частиц при образовании кристалла.
Имеем две частицы на расстоянии
друг от друга. Взаимодействие этих
частиц характеризуется потенциальной
энергией. При сближении частиц действуют
и силы притяжения и силы отталкивания:
![]() .
.
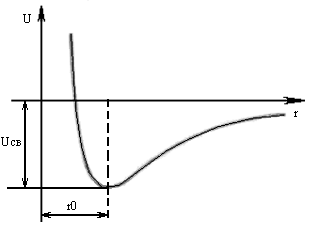

Если =а, то
![]() ,
это более выгодное состояние с
энергетической точки зрения. Если
перенести эти рассуждения на большое
количество частиц, то окажется, что
система будет находиться в равновесии
и обладать минимумом потенциальной
энергии, если частицы будут находиться
на строгом расстоянии друг от друга.
,
это более выгодное состояние с
энергетической точки зрения. Если
перенести эти рассуждения на большое
количество частиц, то окажется, что
система будет находиться в равновесии
и обладать минимумом потенциальной
энергии, если частицы будут находиться
на строгом расстоянии друг от друга.
Кристаллические решётки. Типы симметрии и виды решёток. Индексы Миллера.
Большинство полупроводниковых материалов представляет собой кристаллические твердые вещества с упорядоченной периодической структурой.
Н аименьший
объем кристаллического вещества,
перемещением которого вдоль трех
независимых направлений можно получить
весь кристалл, называют элементарной
ячейкой.
аименьший
объем кристаллического вещества,
перемещением которого вдоль трех
независимых направлений можно получить
весь кристалл, называют элементарной
ячейкой.
Кристаллографические оси в
кристалле определяют направление ребер
элементарной ячейки, а система трех
векторов а, в, с (![]() ),
образующая ячейку – базис.
),
образующая ячейку – базис.
Расстояние между двумя соседними атомами вдоль одного из направлений решетки определяет постоянную решётки.
Кристаллы состоят из атомов или ионов, занимающих определенные положения в пространстве, условно называемые узлами пространственной решётки.
Существует семь простейших кристаллических систем (сингонии, типов симметрии) пространственных решёток.
Они отличаются длинами базисных векторов и углами между ними.
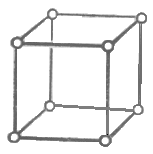
1) кубическая сингония
а1=а2=а3; ===90о.

2) тетрагональная сингония
а1=а2а3; ===90о.

3) ромбическая сингония
а1а2а3; ===90о.

4) гексагональная сингония
а1=а2а3; ==90о
=120о
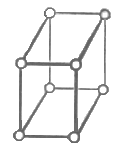
5) моноклинная сингония
а1а2а3; ===90о
6 )
триклинная сингония
)
триклинная сингония
а1а2а3; 90о

7) тригональная сингония
а1=а2=а3; ==90о
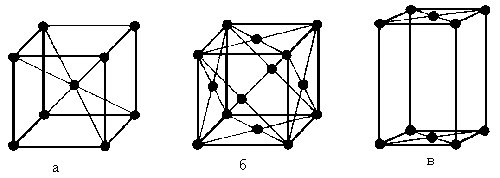
К простым типам симметрии относятся еще 3 вида решеток: а) объемно-центрированная; б) гранецентрированная; в) базоцентрированная.
Кристаллические вещества анизотропные, то есть их свойства зависят от кристаллографического направления.
Для описания закономерностей строения
кристаллов необходимо знание направления.
Так как выбор начала координат в
бесконечном кристалле произволен то
параллельные прямые описываются
одинаковыми символами. Поэтому для
задания направления в кристалле
достаточно задать координаты любого
атома, лежащего на прямой, проходящей
через начало координат и данный атом
(узел). Координаты узла в трехмерном
пространстве по направлениям x,
y, z выражаются
в длинах единичных базисных векторов:
![]() .
.
![]()
Под кристаллографической плоскостью понимают плоскость, проходящую через три узла кристалла, за основу индексации плоскостей понимают длины отрезков отсекаемых плоскостью на осях координат. Длины отрезков отсекаемых плоскостью на осях координат равны n, m и p. От них берутся обратные величины 1/n; 1/m; 1/p которые затем приводятся к наименьшему общему знаменателю S: h/S; k/S; l/S.
Числители полученных дробей являются индексами Миллера и служат для обозначения кристаллографических плоскостей. Они записываются в круглых скобках (h, k, l). Параллельные плоскости, как и направления, имеют одинаковые индексы Миллера. Если плоскость параллельна, какой – либо из координатных осей, то индекс Миллера, соответствующий этой оси, будет равен нулю.
Если в индексах обозначения направления
или плоскостей необходим знак «минус»,
он выносится над нужным индексом
![]() .
.
