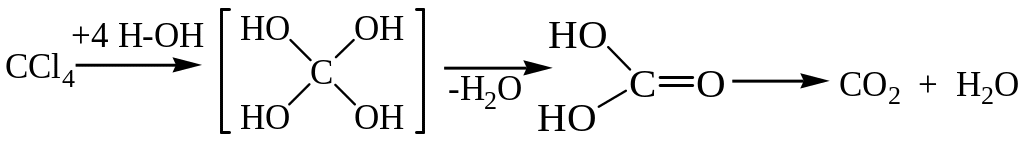- •7.0917.06 “Технологія зберігання, консервування і переробки плодів та овочів”
- •7.0917.07 “Технологія зберігання, консервування та переробки м’яса”
- •7.0917.11 “Технологія харчування”
- •Програма курсу вступ
- •Теоретичні уявлення в органічній хімії
- •Вуглеводні алкани
- •Алкадієни
- •Циклоалкани і циклоалкени
- •Галогенпохідні вуглеводнів
- •Похідні вуглеводнів, що містять гідроксил
- •Карбонільні сполуки (оксосполуки) альдегіди і кетони
- •Карбонові кислоти
- •Окси- і оксокислоти
- •Вуглеводи
- •Органічні сполуки, що містять азот
- •Амінокислоти
- •Гетероциклічні сполуки
- •Пестициди
- •Методичні рекомендації
- •Класифікація органічних сполук
- •Правила техніки безпеки у лабораторії органічної хімії та надання першої допомоги ( загальні правила )
- •Перша допомога при опіках та отруєннях
- •Гасіння місцевої пожежі та одягу що горить
- •Лабораторна робота №1 виділення та очищення органічних сполук, визначення фізичних констант, якісний аналіз
- •1. Перекристалізація
- •Перекристалізація з води
- •2. Сублімація (возгонка)
- •3. Екстракція (витяг)
- •4. Фракційна (дробна) перегонка
- •5. Визначення температури плавлення
- •6. Відкриття вуглецю і водню в органічній речовині
- •Лабораторна робота № 2 насичені та ненасичені вуглеводні
- •1. Одержання метану і дослідження його властивостей.
- •2. Одержання етилену і вивчення його властивостей
- •3. Одержання та властивості ацетилену
- •Завдання для самостійної роботи
- •Лабораторна робота №3 ароматичні вуглеводні
- •1. Одержання бензолу з бензойнокислого натрію
- •2. Відношення бензолу до брому
- •3. Взаємодія бензолу з водним розчином марганцевокислого калію
- •4. Властивості гомологів бензолу.
- •Завдання для самостійної роботи
- •Лабораторна робота № 4 галогенпохідні вуглеводнів
- •1. Одержання хлористого етилу
- •2. Утворення йодоформу з етилового спирту
- •3. Взаємодія хлороформу і чотирихлористого карбону з лугом Реактиви: хлороформ, чотирихлористий карбон, 10% розчин NaOh, нітратна кислота, AgNo3, kMnO4, аміак.
- •Завдання для самостійної роботи
- •Лабораторна робота №5 одно- й багатоатомні спирти. Феноли. Етери
- •1. Виявлення води у спирті
- •2. Розчинність спиртів у воді
- •3. Утворення алкоголяту і його гідроліз
- •4. Окиснення спиртів
- •5. Виявлення домішки метилового спирту в етиловому спирті
- •6. Відкриття сивушної олії
- •7. Якісна реакція на багатоатомні спирти
- •8. Розчинність, кислотний характер фенолів і нафтолів
- •9. Бромування фенолів
- •10. Кольорові реакції фенолів
- •Завдання для самостійної роботи
- •Лабораторна робота № 6 альдегіди і кетони
- •1.Одержання оцтового альдегіду при окисленні етилового спирту
- •2.Одержання ацетону з ацетату кальцію
- •Лабораторна робота №7 карбонові кислоти
- •1. Визначення реакції середовища деяких кислот
- •2. Доведення кислотних властивостей карбонових кислот
- •3. Дослідження окиснюваності деяких органічних кислот
- •4.Розклад мурашиної кислоти
- •5. Розклад щавлевої кислоти
- •6. Проба на ненасиченість олеїнової кислоти
- •7. Ізомеризація олеїнової кислоти в елаїдинову
- •8. Дія хлориду заліза (ііі) на оцтову кислоту (якісна реакція)
- •Завдання для самостійної роботи
- •Лабораторна робота №8 гідроксикислоти. Альдегідокислоти. Кетокислоти
- •1. Якісна реакція на a- оксикислоти з FeCl3
- •2.Розкладання молочної кислоти
- •3. Окислення молочної кислоти у піровиноградну
- •4. Утворення кислої і середньої солі винної кислоти
- •5. Доведення наявності оксигруп у винній кислоті
- •6. Розкладання лимонної кислоти
- •7. Взаємодія галової кислоти і таніну з FeCl3
- •Завдання для самостійної роботи
- •Лабораторна робота №9 естери. Жири та масла. Мила
- •1. Розчинність жирів у різноманітних розчинниках
- •2. Емульгування жирів
- •3. Одержання складних естерів
- •4. Акролеїнова проба на жири
- •5. Омилення жиру
- •6. Дослідження властивостей мила
- •В). Виділення вільних жирних кислот з мила.
- •7. Визначення йодного числа
- •Завдання для самостійної роботи
- •Лабораторна робота № 10 вуглеводи (моносахариди,дисахариди, полісахариди)
- •1. Загальна реакція на вуглеводи з - нафтолом
- •(Реакція Моліша)
- •2.Осмолення моносахаридів
- •3. Окислення моносахаридів реактивом Фелінга
- •4. Окислення моносахаридів аміачним розчином оксиду срібла (реакція срібного дзеркала)
- •9.Виявлення лактози у молоці
- •10. Кольорові реакції на сахарозу.
- •11.Карамелізація сахарози
- •12. Реакція крохмалю з йодом
- •13. Кислотний гідроліз крохмалю
- •14. Одержання рослинного пергаменту
- •15. Розчинення целюлози у мідно-аміачному розчині (реактиві Швейцера)
- •Завдання для самостійної роботи
- •Лабораторна робота №11 тема: аміни . Амінокислоти. Білки
- •1. Одержання аміну і дослідження деяких його властивостей
- •2.Реакції - амінокислот
- •3. Буферні властивості розчину білка
- •4. Осадження білків солями важких металів
- •5. Осадження білків мінеральними кислотами
- •6. Висолювання білків з розчинів
- •7. Осадження білків при нагріванні
- •8. Кольорові реакції білка.
- •Б) Ксантопротеінова реакція на білки й ароматичні амінокислоти
- •9. Відкриття аміногруп і сірки у білках
- •Завдання для самостійної роботи
- •Список рекомендованої літератури Основна
- •Додаткова
3. Взаємодія бензолу з водним розчином марганцевокислого калію
Реактиви: бензол, 0,1% розчин КМnО4, 10% H2SO4.
У пробірку з 1,0 мл бензолу долити 2,0 мл розчину КMnО4 та 1,0мл розчину H2SO4. Суміш струснути. Чи змінюється колір перманганату калію? Висновок.
4. Властивості гомологів бензолу.
Реактиви: толуол (ксилол), бромна вода, розчини0,1 Н KМnO4, 2н H2SO4.
а) Окиснення бічних ланцюгів гомологів бензолу.
У пробірку з1,0 мл толуолу додати 2,0 мл КМnO4; 1,0 мл H2SO4. Енергійно струшуючи, обережно нагріти. Які зміни спостерігаються при нагріванні? Навести хімізм процесу.
б) Бромування толуолу.
У пробірку з 1,0 мл толуолу додати 1,0 мл брому в ССI4. Пробірку закрити пробкою з повітряним холодильником і нагріти на водяній бані. Спостерігати хід реакції. У даних умовах бромування протікає по бензольному ядру або в бічному ланцюзі? Навести хімізм процесу.
Завдання для самостійної роботи
Н
 азвіть
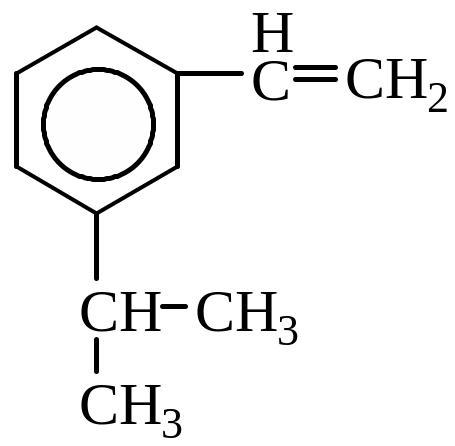
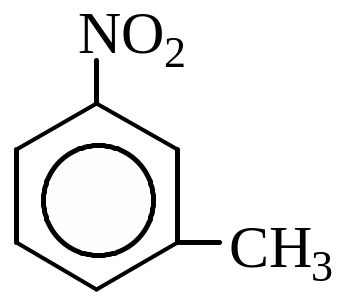
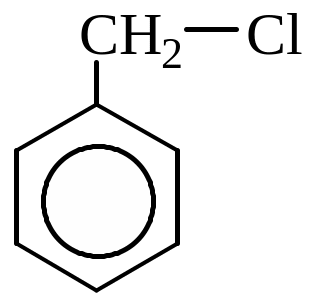
за номенклатурою IUPAC такі сполуки:
азвіть
за номенклатурою IUPAC такі сполуки:
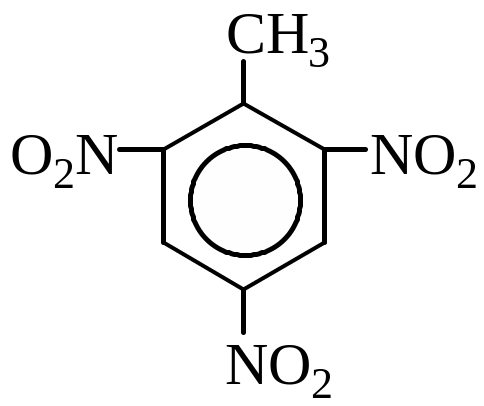
![]()
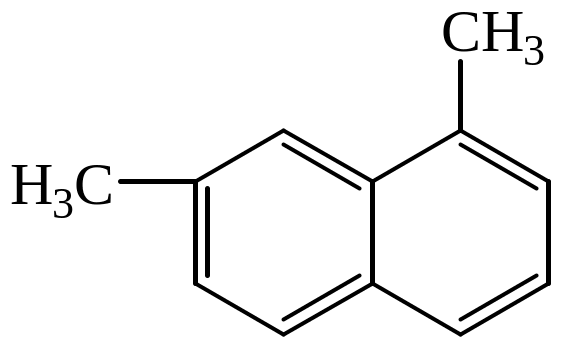
Дайте назву радикалам:
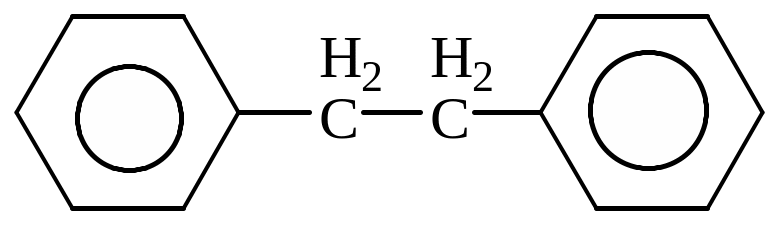
![]()
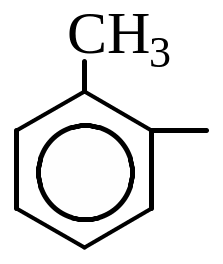
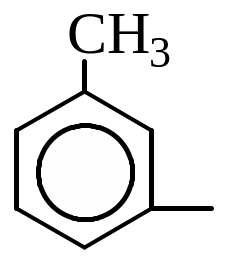
![]()
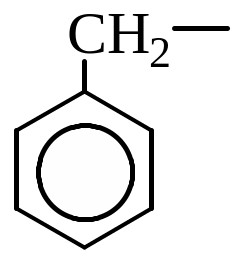
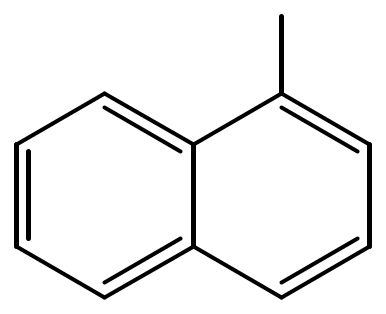
Користуючись реакцією Фріделя-Крафтса, отримайте бензол.
Напишіть схеми реакцій нітрування (з 1 молекулою азотної кислоти.). Назвіть одержані сполуки.
а) пропілбензолу;
б) нітробензолу.
Здійсніть ряд перетворень: бензол → метилбензол → бензойна кислота → м-нітробензойна кислота.
Як з метану отримати етилбензол? Складіть відповідні рівняння реакцій.
Здійсніть ряд перетворень: бензол → етилбензол → вінілбензол (стирол) → полістирол.
Напишіть рівняння,які ілюструють механізм реакцій електрофільного заміщення на прикладі нітрування толуолу та нітробензолу.
Лабораторна робота № 4 галогенпохідні вуглеводнів
1. Одержання хлористого етилу
Реактиви: суміш етилового спирту з концентрованою сульфатною кислотою, хлорид натрію.
У пробірку помістити 0,5 мл суміші етилового спирту з концентрованою сульфатною кислотою. Додати 0,5-1 г хлориду натрію. Закрити пробірку пробкою з газовідвідною трубкою й обережно нагріти. Через якийсь час до отвору газовідвідної трубки піднести запалену лучину. Хлористий етил, що виділяється, горить , створюючи характерне зелене кільце, по краю газовідвідної трубки. Навести хімізм процесу.
2. Утворення йодоформу з етилового спирту
Реактиви: етиловий спирт, розчин йоду в йодиді калію,10% розчин NaOH.
У пробірку внести 1 мл води, 0,5 мл етилового спирту , 3 мл розчину йоду в йодиді калію, по краплях в отриману суміш додати 10% розчин лугу до зникнення бурого кольору. Через якийсь час випадає жовтий осад йодоформу.
I2 + 2 NaOH →NaI + NaIO + H2O
CH3–CH2–OH + NaIO → CH3 –C –H + NaI +H2O
| |
O
CH3 –C –H + I2 + 2NaOH→ H–C –ONa + NaI +H2O + CH3 – I
| | | |
O O
3. Взаємодія хлороформу і чотирихлористого карбону з лугом Реактиви: хлороформ, чотирихлористий карбон, 10% розчин NaOh, нітратна кислота, AgNo3, kMnO4, аміак.
У пробірку помістити декілька крапель хлороформу і 2-3 мл. Розчину NaOH. Обережно нагрійте суміш до початку кипіння при частому струшуванні. Охолодіть пробірку у воді. Одержаний лужний розчин злийте із залишку хлороформу і розділіть на три частини.
До однієї порції налийте розведену азотну кислоту до кислої реакції і декілька крапель AgNO3. Що спостерігається? Якою реакцією ви доведете наявність у розчині галогенід – іону?
До другої порції гідролізату долийте декілька крапель аміачного розчину AgNO3. Що спостерігається? Напишіть реакцію “срібного дзеркала”
До третьої порції гідролізату додайте декілька крапель розчину марганцевокислого калію. Як змінюється колір розчину і чому?
Реакція гідролізу хлороформу проходить за схемою:
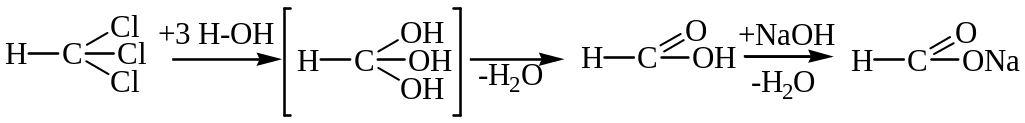
Реакція окислення мурашиної кислоти марганцевокислим калієм в лужному розчині проходить за схемою:
2KMnO4+3NaOH+H–C–ONa→ K2MnO4+Na2MnO4 + Na2CO3 + 2H2О
| |
O
Чотирихлористий карбон в цих умовах майже не гідролізується. Гідроліз його в більш жорстких умовах призводить до утворення H2CO3.