
- •7.0917.06 “Технологія зберігання, консервування і переробки плодів та овочів”
- •7.0917.07 “Технологія зберігання, консервування та переробки м’яса”
- •7.0917.11 “Технологія харчування”
- •Програма курсу вступ
- •Теоретичні уявлення в органічній хімії
- •Вуглеводні алкани
- •Алкадієни
- •Циклоалкани і циклоалкени
- •Галогенпохідні вуглеводнів
- •Похідні вуглеводнів, що містять гідроксил
- •Карбонільні сполуки (оксосполуки) альдегіди і кетони
- •Карбонові кислоти
- •Окси- і оксокислоти
- •Вуглеводи
- •Органічні сполуки, що містять азот
- •Амінокислоти
- •Гетероциклічні сполуки
- •Пестициди
- •Методичні рекомендації
- •Класифікація органічних сполук
- •Правила техніки безпеки у лабораторії органічної хімії та надання першої допомоги ( загальні правила )
- •Перша допомога при опіках та отруєннях
- •Гасіння місцевої пожежі та одягу що горить
- •Лабораторна робота №1 виділення та очищення органічних сполук, визначення фізичних констант, якісний аналіз
- •1. Перекристалізація
- •Перекристалізація з води
- •2. Сублімація (возгонка)
- •3. Екстракція (витяг)
- •4. Фракційна (дробна) перегонка
- •5. Визначення температури плавлення
- •6. Відкриття вуглецю і водню в органічній речовині
- •Лабораторна робота № 2 насичені та ненасичені вуглеводні
- •1. Одержання метану і дослідження його властивостей.
- •2. Одержання етилену і вивчення його властивостей
- •3. Одержання та властивості ацетилену
- •Завдання для самостійної роботи
- •Лабораторна робота №3 ароматичні вуглеводні
- •1. Одержання бензолу з бензойнокислого натрію
- •2. Відношення бензолу до брому
- •3. Взаємодія бензолу з водним розчином марганцевокислого калію
- •4. Властивості гомологів бензолу.
- •Завдання для самостійної роботи
- •Лабораторна робота № 4 галогенпохідні вуглеводнів
- •1. Одержання хлористого етилу
- •2. Утворення йодоформу з етилового спирту
- •3. Взаємодія хлороформу і чотирихлористого карбону з лугом Реактиви: хлороформ, чотирихлористий карбон, 10% розчин NaOh, нітратна кислота, AgNo3, kMnO4, аміак.
- •Завдання для самостійної роботи
- •Лабораторна робота №5 одно- й багатоатомні спирти. Феноли. Етери
- •1. Виявлення води у спирті
- •2. Розчинність спиртів у воді
- •3. Утворення алкоголяту і його гідроліз
- •4. Окиснення спиртів
- •5. Виявлення домішки метилового спирту в етиловому спирті
- •6. Відкриття сивушної олії
- •7. Якісна реакція на багатоатомні спирти
- •8. Розчинність, кислотний характер фенолів і нафтолів
- •9. Бромування фенолів
- •10. Кольорові реакції фенолів
- •Завдання для самостійної роботи
- •Лабораторна робота № 6 альдегіди і кетони
- •1.Одержання оцтового альдегіду при окисленні етилового спирту
- •2.Одержання ацетону з ацетату кальцію
- •Лабораторна робота №7 карбонові кислоти
- •1. Визначення реакції середовища деяких кислот
- •2. Доведення кислотних властивостей карбонових кислот
- •3. Дослідження окиснюваності деяких органічних кислот
- •4.Розклад мурашиної кислоти
- •5. Розклад щавлевої кислоти
- •6. Проба на ненасиченість олеїнової кислоти
- •7. Ізомеризація олеїнової кислоти в елаїдинову
- •8. Дія хлориду заліза (ііі) на оцтову кислоту (якісна реакція)
- •Завдання для самостійної роботи
- •Лабораторна робота №8 гідроксикислоти. Альдегідокислоти. Кетокислоти
- •1. Якісна реакція на a- оксикислоти з FeCl3
- •2.Розкладання молочної кислоти
- •3. Окислення молочної кислоти у піровиноградну
- •4. Утворення кислої і середньої солі винної кислоти
- •5. Доведення наявності оксигруп у винній кислоті
- •6. Розкладання лимонної кислоти
- •7. Взаємодія галової кислоти і таніну з FeCl3
- •Завдання для самостійної роботи
- •Лабораторна робота №9 естери. Жири та масла. Мила
- •1. Розчинність жирів у різноманітних розчинниках
- •2. Емульгування жирів
- •3. Одержання складних естерів
- •4. Акролеїнова проба на жири
- •5. Омилення жиру
- •6. Дослідження властивостей мила
- •В). Виділення вільних жирних кислот з мила.
- •7. Визначення йодного числа
- •Завдання для самостійної роботи
- •Лабораторна робота № 10 вуглеводи (моносахариди,дисахариди, полісахариди)
- •1. Загальна реакція на вуглеводи з - нафтолом
- •(Реакція Моліша)
- •2.Осмолення моносахаридів
- •3. Окислення моносахаридів реактивом Фелінга
- •4. Окислення моносахаридів аміачним розчином оксиду срібла (реакція срібного дзеркала)
- •9.Виявлення лактози у молоці
- •10. Кольорові реакції на сахарозу.
- •11.Карамелізація сахарози
- •12. Реакція крохмалю з йодом
- •13. Кислотний гідроліз крохмалю
- •14. Одержання рослинного пергаменту
- •15. Розчинення целюлози у мідно-аміачному розчині (реактиві Швейцера)
- •Завдання для самостійної роботи
- •Лабораторна робота №11 тема: аміни . Амінокислоти. Білки
- •1. Одержання аміну і дослідження деяких його властивостей
- •2.Реакції - амінокислот
- •3. Буферні властивості розчину білка
- •4. Осадження білків солями важких металів
- •5. Осадження білків мінеральними кислотами
- •6. Висолювання білків з розчинів
- •7. Осадження білків при нагріванні
- •8. Кольорові реакції білка.
- •Б) Ксантопротеінова реакція на білки й ароматичні амінокислоти
- •9. Відкриття аміногруп і сірки у білках
- •Завдання для самостійної роботи
- •Список рекомендованої літератури Основна
- •Додаткова
2. Сублімація (возгонка)
При сублімації тверда речовина, минаючи рідкий стан, переходить у пароподібний стан, а пари при охолодженні переходять у твердий. Не всі речовини можуть піддаватися очищенню цим методом. Цей метод можна використовувати при очищенні хінонів, багатоядерних сполук, органічних кислот.
Реактиви: забруднені нафталін або хінон.
На дно стакана тонким шаром помістити 2-3 г забрудненого нафталіну або хінону. Нагріти стакан повільно і невеличким полум'ям, попередньо опустити в стакан скляну лійку. З'являються пари і при охолодженні дають звільнені від домішок кристали, що осідають на охолоджених стінках лійки.
Сублімацію можна проводити в порцеляновій чашці, покритій конічною лійкою. Якщо сублімації піддаються невеличкі кількості речовин, то її проводять на годинниковому склі, поверх прикритим іншим годинниковим склом. Годинникові стекла поміщають у порцелянову чашу, наповнену піском і нагрівають.
3. Екстракція (витяг)
Екстракцію застосовують для виділення речовини з твердої суміші або розчинів визначеним розчинником. На практиці речовину з водяного розчину частіше усього витягають органічним розчинником. Розчинник повинний задовольняти таким вимогам: розчинник не повинний змішуватися з водяною фазою, мати невисоку температуру кипіння. Крім того, розчинність речовини, що екстрагується повинна бути значно вищою, ніж у вихідному розчині; різна густина речовин.
Екстрагування рідин частіше усього проводять у ділильній лійці. Для екстрагування органічних сполук з водних розчинів застосовують бензин, бензол, хлороформ, діетиловий етер і ін.
Перед початком роботи верхню пробку і нижній край ділильної лійки змащують тонким прошарком вазеліну. Потім у неї наливають розчин, що підлягає екстрагуванню і добавляють розчинник, з огляду на те, що загальний обсяг рідини в лійці не перевищував 2/3 її об’єму. Ділильну лійку закривають пробкою й обережно струшують, плавно перевертаючи догори-вниз на протязі 5-10 хвилин, притримуючи пробку і край руками. При струшуванні підвищується тиск усередині лійки. Для його зменшення, ділильну лійку повертають пробкою униз і відкривають кран. Пари розчинника виходять і тиск зрівнюється з атмосферним. Після цього ділильну лійку закріплюють у штативі і лишають до повного поділу прошарків. Знявши пробку з лійки, випускають нижній прошарок через кран, а верхній прошарок зливають через верхній отвір. Для більш повного витягу речовини екстрагування повторюють декілька разів підряд, підливаючи щоразу нові порції розчинника.
Щоб визначити закінчення екстрагування, декілька крапель останньої порції екстракту випаровують на годинниковому склі досуха. Якщо проба випаровується без залишку, то екстрагування закінчене.
Реактиви та посуд: розчин йоду, CCl4, ділильна лійка, колбочки.
У ділильну лійку ємністю до 100 мл помістити приблизно 10 мл розчину йоду та 20 мл CCl4. Зробити екстракцію йоду по вище викладеній методиці.
4. Фракційна (дробна) перегонка
Реактиви та посуд: Суміші: а) чотирьоххлористий вуглець і ксилол;
б) ксилол і хлороформ;
в) хлороформ і скипидар, прилад для перегонки
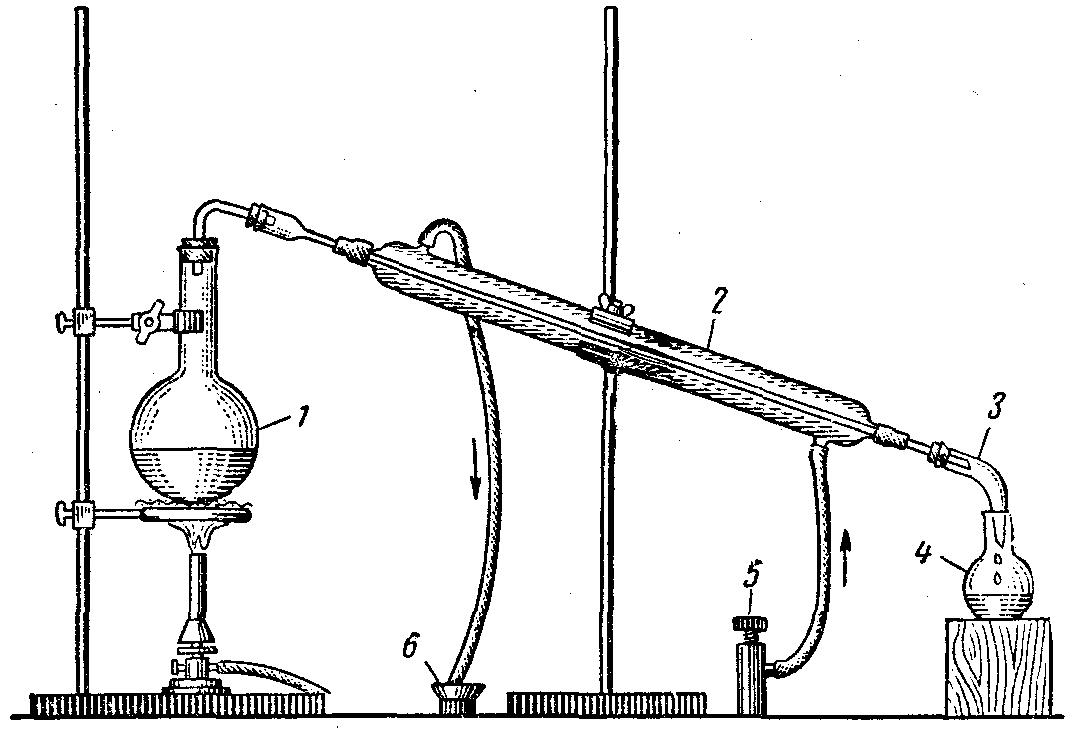
Мал. 1 Прилад з водяним холодильником для перегонки
У перегінну колбу помістити 22,0 - 22,5 мл вихідної суміші (відношення компонентів суміші 1:1). Наприклад, суміш чотирьоххлористого вуглецю і ксилолу. (температура кипіння чотирьоххлористого вуглецю - 700С; температура кипіння ксилолу - 1390С). Підключають перегінну установку і збирають фракції, що киплять приблизно в рівних температурних інтервалах.
І фракція до 95 0С
ІІ фракція - від 950С до 1100С
ІІІ фракція - від 1100С до 1250С
Коли температура парів досягне 1250С, припиняють перегонку. Цей метод використовують також для визначення температури кипіння.
