
- •Лекция 1
- •1.1. Органические топлива
- •1.1.1. Классификация углеводородных горючих
- •1.1.2. Состав топлив
- •1.1.3. Характеристики топлив
- •1.1.4. Разновидности горения
- •1.1.5. Основные стадии гетерогенного горения
- •1.1.6. Фазы горения
- •Лекция 2
- •1.1.7. Скорость горения
- •1.2. Расчет процессов горения
- •2. Определение количества и состава продуктов сгорания.
- •1.2.1. Определение потребного количества окислителя для полного сжигания 1кг горючего
- •1.2.2. Определение массы воздуха для сжигания 1кг топлива
- •1.2.3. Коэффициент избытка воздуха
- •1.2.4. Определение количества и состава продуктов сгорания
- •1.2.5. Определение состава продуктов сгорания
- •1.2.6. Определение температуры конца сгорания
- •1.2.7. Упрощенная форма уравнения теплового баланса
- •Лекция 3
- •2.1. Основные понятия и определения термодинамики
- •2.2. Параметры состояния системы
- •2.3. Первый закон термодинамики. Работа и теплота.
- •2.4. Свойства рv – и Тs – диаграмм
- •Лекция 4
- •2.5. Термодинамические процессы идеальных газов
- •2.5.1. Политропный процесс
- •Вывод уравнения политропного процесса
- •Соотношения между параметрами состояния в политропном процессе
- •Определение изменения внутренней энергии
- •Определение изменения энтальпии
- •Определение изменения энтропии
- •Определение теплоты, подводимой (отводимой) в ходе политропного процесса
- •Определение работы расширения в ходе политропного процесса
- •2.5.2. Частные случаи политропного процесса
- •2.5.3. Изохорный процесс
- •2.5.4. Изобарный процесс
- •2.5.5. Изотермический процесс
- •2.5.6. Адиабатный процесс
- •2.5.7. Графическое изображение процессов
- •Лекция 5 сжатие газов в компрессорах
- •Работа компрессора.
- •Действительная индикаторная диаграмма компрессора.
- •Объемный кпд компрессора.
- •Гидравлические потери в распределительных органах компрессора.
- •Многоступенчатые компрессоры.
- •Лекция 6 истечение газов и паров Первый закон термодинамики для потока газа.
- •Адиабатное течение идеального газа по горизонтальному каналу без совершения технической работы.
- •Закон геометрического обращения воздействия
- •Определение скорости потока на выходе из канала
- •Массовый секундный расход газа
- •Анализ соплового течения газа через суживающееся сопло
- •Сопло Лаваля
- •Лекция 7 реальные газы
- •Устройство pv – диаграммы реального газа
- •Области pv- диаграммы
- •Уравнение состояния реального газа
- •Определение параметров влажного насыщенного пара
- •Диаграммы водяного пара
- •Лекция 8
- •Оновной закон теплопроводности. Гипотеза фурье.
- •В практике теплотехнических расчетов широко пользуются понятием теплового потока:
- •Конвекция
- •Процесс теплообмена между поверхностью твердого тела и жидкостью, омывающей поверхность, называется теплоотдачей.
- •Основной закон теплоотдачи. Уравнение ньютона – рихмана.
- •Теплопередача
- •Теплообмен излучением
- •Лекция 9 дифференциальное уравнение теплопроводности
- •Частные случаи дифференциального уравнения теплопроводности.
- •Для неподвижной среды (для твердого тела).
- •Дифференциальное уравнение теплопроводности для твердого тела в цилиндрической системе координат.
- •Простейший случай дифференциального уравнения теплопроводности для одномерного стационарного поля.
- •Краевые условия (условия однозначности).
- •Граничные условия.
- •Рассмотрим пример.
1.2.2. Определение массы воздуха для сжигания 1кг топлива
Массовая доля кислорода в воздухе составляет 0,23. Поэтому количество воздуха, теоретически необходимое для сжигания 1 кг топлива будет равно
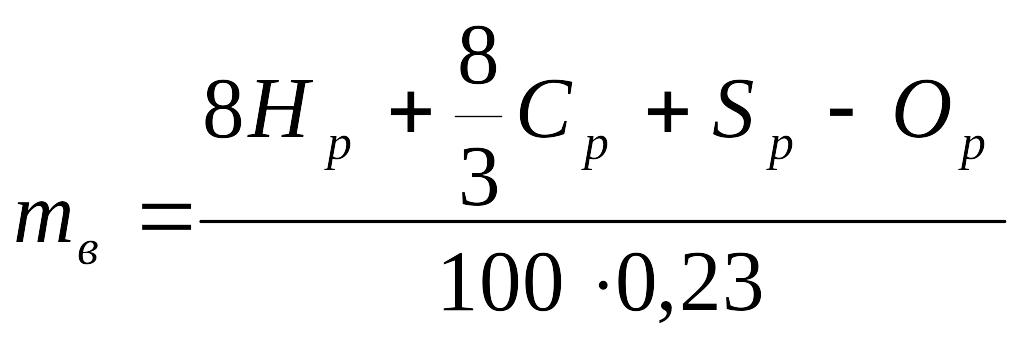 ,
кгвоздуха/кгтоплива.
,
кгвоздуха/кгтоплива.
1.2.3. Коэффициент избытка воздуха
В действительности подаваемое количество воздуха отличается от теоретически необходимого. Из-за несовершенства процессов смесеобразования в энергетических установках, где стремятся максимально полно использовать энергию топлива, приходится подавать воздух в количествах, превышающих теоретически необходимое. В печах безокислительного нагрева металла, чтобы поддержать восстановительную атмосферу печи, воздуха подают меньше, то есть сознательно идут на недожег топлива.
Отношение
действительно поданного воздуха (![]() )
к его теоретически необходимому
количеству (
)
к его теоретически необходимому
количеству (![]() )
представляет собой коэффициент избытка
воздуха (
)
представляет собой коэффициент избытка
воздуха (![]() ):
):
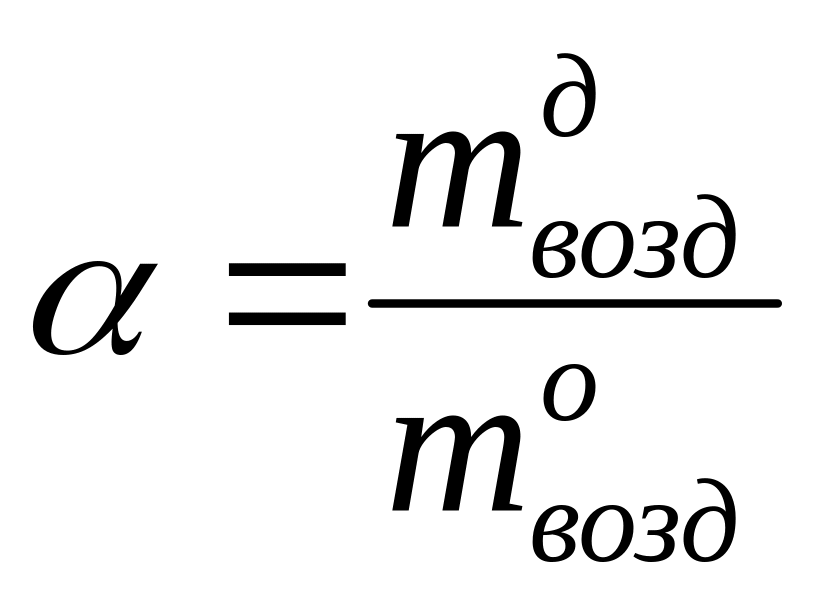 .
.
При
сжигании древесины
![]() ;
углей -
;
углей -
![]() ;
при сжигании газа и мазута
;
при сжигании газа и мазута
![]() ;
в дизелях минимальные значения
близки к 1,3; карбюраторные двигатели
работают в диапазоне значений
от 0,8 до 1,2 (в зависимости от режима работы
и конструкции двигателя).
;
в дизелях минимальные значения
близки к 1,3; карбюраторные двигатели
работают в диапазоне значений
от 0,8 до 1,2 (в зависимости от режима работы
и конструкции двигателя).
Различают три вида топливных смесей, в зависимости от значения .
При
![]() смеси
называются бедными
(окислителя в зону реакции подается
больше, чем требуется для полного
сгорания горючего). В продуктах сгорания
таких смесей содержатся следующие
элементы: Н2О,
СО2,
SO2,
N2,
О2.
смеси
называются бедными
(окислителя в зону реакции подается
больше, чем требуется для полного
сгорания горючего). В продуктах сгорания
таких смесей содержатся следующие
элементы: Н2О,
СО2,
SO2,
N2,
О2.
При
![]() смеси
называются стехиометрическими
(окислителя в зону реакции подается
столько, сколько требуется для полного
сгорания горючего). В продуктах сгорания
таких смесей содержатся следующие
элементы: Н2О,
СО2,
SO2,
N2.
смеси
называются стехиометрическими
(окислителя в зону реакции подается
столько, сколько требуется для полного
сгорания горючего). В продуктах сгорания
таких смесей содержатся следующие
элементы: Н2О,
СО2,
SO2,
N2.
При
![]() смеси
называются богатыми
(окислителя в зону реакции подается
меньше, чем требуется для полного
сгорания горючего). В продуктах сгорания
таких смесей содержатся следующие
элементы: Н2О,
СО2,
СО, С, N2.
смеси
называются богатыми
(окислителя в зону реакции подается
меньше, чем требуется для полного
сгорания горючего). В продуктах сгорания
таких смесей содержатся следующие
элементы: Н2О,
СО2,
СО, С, N2.
1.2.4. Определение количества и состава продуктов сгорания
Масса продуктов сгорания в соответствии с законом сохранения массы равняется сумме масс сожженного топлива и использованного для этих целей окислителя. Если в качестве окислителя использовался кислород воздуха, то масса продуктов сгорания, образовавшихся при сжигании 1 кг топлива, определяется соотношением:
![]()
![]() ,
,
то есть при прочих равных условиях масса продуктов сгорания растет с увеличением коэффициента избытка воздуха. Это приводит к снижению жаропроизводительности, а также увеличивает количество теплоты, уносимой с уходящими газами.
1.2.5. Определение состава продуктов сгорания
Определение состава продуктов сгорания производится аналогично определению потребного количества окислителя. В основу этого расчета также кладутся балансовые уравнения 1.1, 1.2 и 1.3.
Количество влаги определяется по соотношению:
![]()
![]() .
.
Количество диоксида углерода:
![]()
![]()
Количество диоксида серы:
![]()
![]()
Кроме того, надо учесть, что в продукты сгорания переходит практически весь азот поданного для горения воздуха:
![]()
![]() ,
,
где 0,77 – массовая доля содержания азота в воздухе.
А также кислород, содержащийся в избыточной части поданного воздуха:
![]() .
.
1.2.6. Определение температуры конца сгорания
Температура конца сгорания определяется из уравнения теплового баланса сжигающего устройства:
![]() ,
,
где
![]() – коэффициент полноты сгорания горючего;
– коэффициент полноты сгорания горючего;
![]() – масса горючего;
– масса горючего;
![]() – низшая теплота сгорания горючего;
– низшая теплота сгорания горючего;
![]() – теплоемкость горючего;
– теплоемкость горючего;
![]() – температура
горючего при поступлении его в зону
реакции;
– температура
горючего при поступлении его в зону
реакции;
![]() – температура
начала реакции;
– температура
начала реакции;
![]() – теплоемкость окислителя;
– теплоемкость окислителя;
![]() – масса окислителя;
– масса окислителя;
![]() – температура
окислителя;
– температура
окислителя;
![]() – теплоемкость продуктов сгорания;
– теплоемкость продуктов сгорания;
![]() – масса продуктов сгорания;
– масса продуктов сгорания;
![]() – температура
конца сгорания (адиабатная температура).
– температура
конца сгорания (адиабатная температура).
В этом уравнении первое слагаемое означает количество теплоты, образующееся в результате сгорания горючего. Второе – количество теплоты, вносимое горючим в зону реакции. Третье – количество теплоты, вносимое окислителем в зону реакции. Правая часть уравнения означает количество теплоты содержащейся в продуктах сгорания.
