
- •Лекция 1
- •1.1. Органические топлива
- •1.1.1. Классификация углеводородных горючих
- •1.1.2. Состав топлив
- •1.1.3. Характеристики топлив
- •1.1.4. Разновидности горения
- •1.1.5. Основные стадии гетерогенного горения
- •1.1.6. Фазы горения
- •Лекция 2
- •1.1.7. Скорость горения
- •1.2. Расчет процессов горения
- •2. Определение количества и состава продуктов сгорания.
- •1.2.1. Определение потребного количества окислителя для полного сжигания 1кг горючего
- •1.2.2. Определение массы воздуха для сжигания 1кг топлива
- •1.2.3. Коэффициент избытка воздуха
- •1.2.4. Определение количества и состава продуктов сгорания
- •1.2.5. Определение состава продуктов сгорания
- •1.2.6. Определение температуры конца сгорания
- •1.2.7. Упрощенная форма уравнения теплового баланса
- •Лекция 3
- •2.1. Основные понятия и определения термодинамики
- •2.2. Параметры состояния системы
- •2.3. Первый закон термодинамики. Работа и теплота.
- •2.4. Свойства рv – и Тs – диаграмм
- •Лекция 4
- •2.5. Термодинамические процессы идеальных газов
- •2.5.1. Политропный процесс
- •Вывод уравнения политропного процесса
- •Соотношения между параметрами состояния в политропном процессе
- •Определение изменения внутренней энергии
- •Определение изменения энтальпии
- •Определение изменения энтропии
- •Определение теплоты, подводимой (отводимой) в ходе политропного процесса
- •Определение работы расширения в ходе политропного процесса
- •2.5.2. Частные случаи политропного процесса
- •2.5.3. Изохорный процесс
- •2.5.4. Изобарный процесс
- •2.5.5. Изотермический процесс
- •2.5.6. Адиабатный процесс
- •2.5.7. Графическое изображение процессов
- •Лекция 5 сжатие газов в компрессорах
- •Работа компрессора.
- •Действительная индикаторная диаграмма компрессора.
- •Объемный кпд компрессора.
- •Гидравлические потери в распределительных органах компрессора.
- •Многоступенчатые компрессоры.
- •Лекция 6 истечение газов и паров Первый закон термодинамики для потока газа.
- •Адиабатное течение идеального газа по горизонтальному каналу без совершения технической работы.
- •Закон геометрического обращения воздействия
- •Определение скорости потока на выходе из канала
- •Массовый секундный расход газа
- •Анализ соплового течения газа через суживающееся сопло
- •Сопло Лаваля
- •Лекция 7 реальные газы
- •Устройство pv – диаграммы реального газа
- •Области pv- диаграммы
- •Уравнение состояния реального газа
- •Определение параметров влажного насыщенного пара
- •Диаграммы водяного пара
- •Лекция 8
- •Оновной закон теплопроводности. Гипотеза фурье.
- •В практике теплотехнических расчетов широко пользуются понятием теплового потока:
- •Конвекция
- •Процесс теплообмена между поверхностью твердого тела и жидкостью, омывающей поверхность, называется теплоотдачей.
- •Основной закон теплоотдачи. Уравнение ньютона – рихмана.
- •Теплопередача
- •Теплообмен излучением
- •Лекция 9 дифференциальное уравнение теплопроводности
- •Частные случаи дифференциального уравнения теплопроводности.
- •Для неподвижной среды (для твердого тела).
- •Дифференциальное уравнение теплопроводности для твердого тела в цилиндрической системе координат.
- •Простейший случай дифференциального уравнения теплопроводности для одномерного стационарного поля.
- •Краевые условия (условия однозначности).
- •Граничные условия.
- •Рассмотрим пример.
1.1.4. Разновидности горения
Горением называется химическая реакция взаимодействия горючего с окислителем, сопровождающаяся интенсивным выделением теплоты и резким повышением температуры.
Горение возможно только в газообразной фазе.
Если горючее и окислитель находятся в одной газообразной фазе, то горение называют гомогенным.
Если один из компонентов топлива находится в отличном от газообразного состояния, то горение называют гетерогенным.
При гетерогенном горении происходит изменение агрегатного состояния вещества.
1.1.5. Основные стадии гетерогенного горения
1. Подогрев (до 100 0С).
2. Подсушка или испарение влаги (102 - 105 0С).
3. Выход летучих соединений (200 - 400 0С).
4. Воспламенение или инициирование горения (600 - 800 0С).
5. Горение (800 - 3000 0С).
6. Догорание или тление (600 - 800 0С).
1.1.6. Фазы горения
Время, за которое происходит полное сгорание топлива можно условно разделить на два этапа:
г = ф + к,
где г продолжительность горения;
ф физическая фаза (время смесеобразования);
к кинетическая фаза (время химической реакции окисления).
В зависимости от продолжительности той или иной фазы, различают два предельных случая:
1)ф >>к диффузионное горение (факельное сжигание топлива, горение спички, горелки);
2) к >> ф кинетическое горение (взрыв).
Лекция 2
1.1.7. Скорость горения
Под скоростью горения понимают скорость, с которой перемещается фронт пламени.
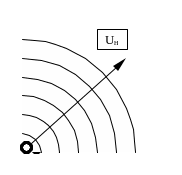
Нормальная скорость распространения фронта пламени (Uн), обозначается вектором, направленным перпендикулярно ко фронту пламени.
В зависимости от величины скорости перемещения фронта пламени, различают нормальное и детонационное горение.
Uн = 0,4 50 м/с нормальное горение,
где Uн = 0,4 13 м/с ламинарное горение (пламя);
Uн = 13 50 м/с турбулентное горение.
Uн = 1500 3500 м/с детонационное горение.
а) б)
Рис.1.1
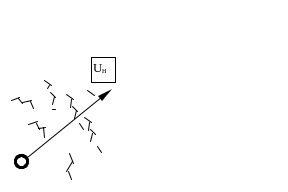
На рисунке 1.1 а приведена схема ламинарного горения от точечного источника. При этом режиме горения фронт пламени гладкий (горение спички, свечи). На рисунке. 1.1 б приведена схема турбулентного горения от точечного источника. При этом режиме горения фронт пламени размытый (горение горелки при большой подаче горючего).
1.2. Расчет процессов горения
Основные цели расчета процесса горения сводятся к определению следующих величин.
1. Определение потребного количества окислителя для полного сжигания 1кг горючего.
2. Определение количества и состава продуктов сгорания.
3. Определение температуры конца сгорания продуктов сгорания.
4. Определение теплосодержания (энтальпии) продуктов сгорания.
1.2.1. Определение потребного количества окислителя для полного сжигания 1кг горючего
Расчет ведут обычно на 1 кг рабочей массы сжигаемого топлива. В основу положены уравнения баланса, использование которых можно понять на примере окисления горючих элементов, входящих в состав рабочей массы топлива.
Рассмотрим стехиометрические реакции окисления горючих веществ, входящих в состав горючего.
Окисление водорода рабочей массы топлива
2H2 + O2 = 2H2O (1.1)
4кг H2 +32кг O2 = 36кгH2O
1кг H2+ 8кг O2 = 9кгH2O
Из этого уравнения следует, что каждый килограмм сжигаемого водорода требует 8 кг кислорода, при этом образуется 9 кг воды. Если в рабочей массе сжигаемого топлива содержится Hp % водорода, то для окисления водорода, входящего в 1 кг такого топлива, необходимо иметь массу кислорода (в кг), равную
![]() .
.
Аналогично можно определить потребное количество кислорода для окисления углерода и серы.
С + O2 = СO2 (1.2)
12кг С + 32кг O2 = 44кг СО2
1кг С + 8/3кгO2 = 11/3кгСО2
S + O2 = SO2 (1.3)
32кг S + 32кгO2 = 64кг SО2
1кг S + 1кг O2 = 2кг SО2
Если вычесть уже содержащийся в топливе кислород, то его потребность (в кг) на каждый килограмм сжигаемого топлива выразится соотношением
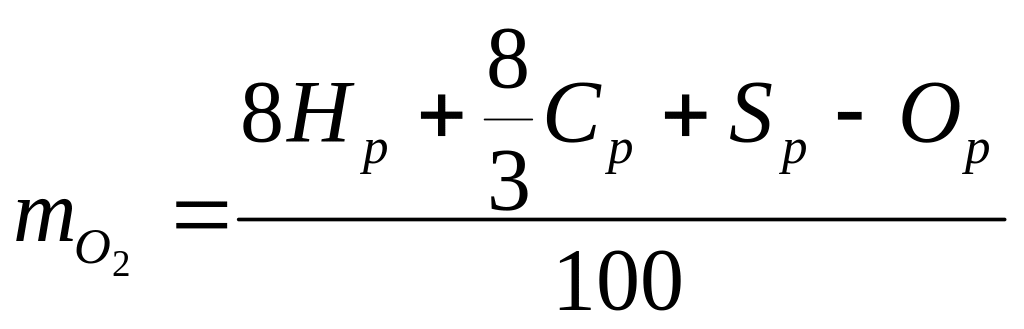 кгкислорода/кгтоплива.
кгкислорода/кгтоплива.
В этом соотношении сумма величин, стоящих в числителе, показывает потребное количество кислорода необходимое для полного окисления рабочей массы горючих элементов топлива. Рабочая масса кислорода Ор горючего входит в состав горючего в виде соединений и участвует в реакции окисления, поэтому она вычитается.
