
- •Лекция 1
- •1.1. Органические топлива
- •1.1.1. Классификация углеводородных горючих
- •1.1.2. Состав топлив
- •1.1.3. Характеристики топлив
- •1.1.4. Разновидности горения
- •1.1.5. Основные стадии гетерогенного горения
- •1.1.6. Фазы горения
- •Лекция 2
- •1.1.7. Скорость горения
- •1.2. Расчет процессов горения
- •2. Определение количества и состава продуктов сгорания.
- •1.2.1. Определение потребного количества окислителя для полного сжигания 1кг горючего
- •1.2.2. Определение массы воздуха для сжигания 1кг топлива
- •1.2.3. Коэффициент избытка воздуха
- •1.2.4. Определение количества и состава продуктов сгорания
- •1.2.5. Определение состава продуктов сгорания
- •1.2.6. Определение температуры конца сгорания
- •1.2.7. Упрощенная форма уравнения теплового баланса
- •Лекция 3
- •2.1. Основные понятия и определения термодинамики
- •2.2. Параметры состояния системы
- •2.3. Первый закон термодинамики. Работа и теплота.
- •2.4. Свойства рv – и Тs – диаграмм
- •Лекция 4
- •2.5. Термодинамические процессы идеальных газов
- •2.5.1. Политропный процесс
- •Вывод уравнения политропного процесса
- •Соотношения между параметрами состояния в политропном процессе
- •Определение изменения внутренней энергии
- •Определение изменения энтальпии
- •Определение изменения энтропии
- •Определение теплоты, подводимой (отводимой) в ходе политропного процесса
- •Определение работы расширения в ходе политропного процесса
- •2.5.2. Частные случаи политропного процесса
- •2.5.3. Изохорный процесс
- •2.5.4. Изобарный процесс
- •2.5.5. Изотермический процесс
- •2.5.6. Адиабатный процесс
- •2.5.7. Графическое изображение процессов
- •Лекция 5 сжатие газов в компрессорах
- •Работа компрессора.
- •Действительная индикаторная диаграмма компрессора.
- •Объемный кпд компрессора.
- •Гидравлические потери в распределительных органах компрессора.
- •Многоступенчатые компрессоры.
- •Лекция 6 истечение газов и паров Первый закон термодинамики для потока газа.
- •Адиабатное течение идеального газа по горизонтальному каналу без совершения технической работы.
- •Закон геометрического обращения воздействия
- •Определение скорости потока на выходе из канала
- •Массовый секундный расход газа
- •Анализ соплового течения газа через суживающееся сопло
- •Сопло Лаваля
- •Лекция 7 реальные газы
- •Устройство pv – диаграммы реального газа
- •Области pv- диаграммы
- •Уравнение состояния реального газа
- •Определение параметров влажного насыщенного пара
- •Диаграммы водяного пара
- •Лекция 8
- •Оновной закон теплопроводности. Гипотеза фурье.
- •В практике теплотехнических расчетов широко пользуются понятием теплового потока:
- •Конвекция
- •Процесс теплообмена между поверхностью твердого тела и жидкостью, омывающей поверхность, называется теплоотдачей.
- •Основной закон теплоотдачи. Уравнение ньютона – рихмана.
- •Теплопередача
- •Теплообмен излучением
- •Лекция 9 дифференциальное уравнение теплопроводности
- •Частные случаи дифференциального уравнения теплопроводности.
- •Для неподвижной среды (для твердого тела).
- •Дифференциальное уравнение теплопроводности для твердого тела в цилиндрической системе координат.
- •Простейший случай дифференциального уравнения теплопроводности для одномерного стационарного поля.
- •Краевые условия (условия однозначности).
- •Граничные условия.
- •Рассмотрим пример.
2.3. Первый закон термодинамики. Работа и теплота.
Закон сохранения и превращения энергии является наиболее общим универсальным законом природы, применяемым ко всем явлениям и процессам.
Этот закон формулируется так:
Энергия изолированной системы, при любых происходящих в ней процессах, не меняется; энергия не уничтожается и не создается.
Первый закон термодинамики является частным случаем этого закона применительно к процессам, протекающим в термодинамических системах.
В соответствии с первым законом термодинамики внутренняя энергия термодинамической системы может изменяться лишь в результате энергетического обмена с окружающей средой.
В термодинамике первое начало обычно записывают так (применительно к 1кг массы):
q = Δu + l (2.6)
или в дифференциальной форме:
dq = du +dl. (2.7)
Таким образом, в общем случае тепло, подводимое к системе, расходуется как на изменение энергии, так и на совершение работы.
Работа 1 кг газа в элементарном равновесном процессе:
dl = pdv. (2.8)
Для конечного процесса:
l
=
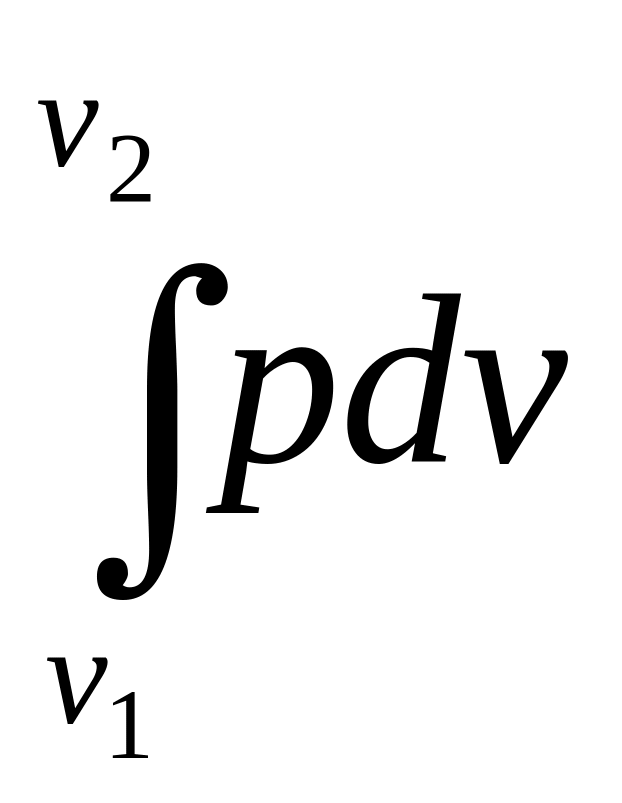 .
(2.9)
.
(2.9)
Чтобы решить интеграл (2.9), надо знать зависимость, связывающую давление и объем в ходе процесса. Таким образом, работа, производимая газом, в отличие от параметров состояния, зависит от вида процесса.
2.4. Свойства рv – и Тs – диаграмм
Если воспользоваться системой координат рv, то величину работы можно определить графически.
Нетрудно
видеть (рис. 2.1), что элементарная площадка
аbcd = рdv
= dl,
а площадь АВСD
=
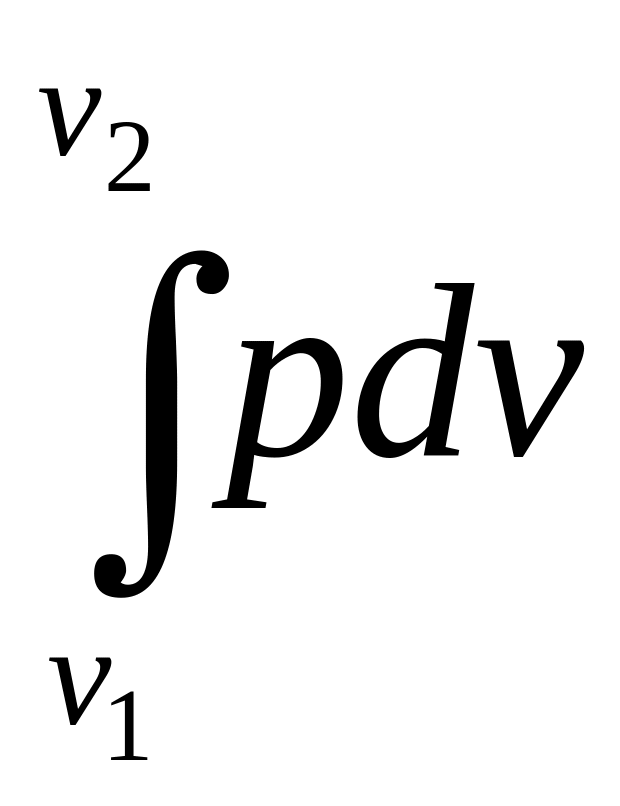 =
l.
Таким
образом, в системе координат рv
работа, приведенная в ходе процесса
численно равна площади, ограниченной
кривой процесса, осью абсцисс и крайними
ординатами.
=
l.
Таким
образом, в системе координат рv
работа, приведенная в ходе процесса
численно равна площади, ограниченной
кривой процесса, осью абсцисс и крайними
ординатами.
Из-за этого свойства рv- диаграмму называют иногда рабочей диаграммой.
Теплота, подведенная (отведенная) в ходе элементарного обратимого процесса может быть, в частности, вычислена при использовании уравнений (2.4) и (2.5)
dQ = TdS или dq = Tds. (2.10)
Для всего процесса
Q
=
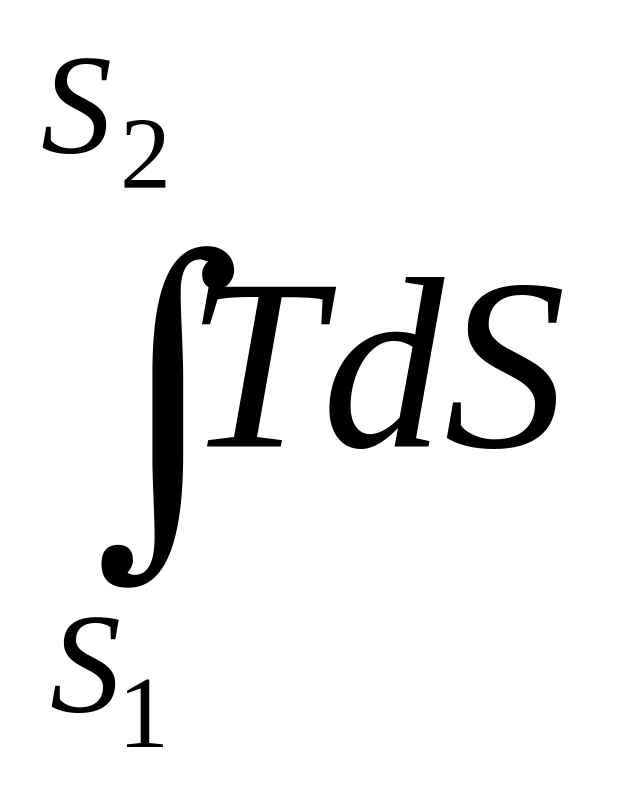 или
q
=
или
q
=
![]() .
(2.11)
.
(2.11)
Взаимосвязь между Т и S в разных процессах различна. Поэтому количество теплоты (как и работы) зависит не только от начального и конечного состояний системы, но и от вида процесса.
Решение интегралов (2.11) можно осуществить графическим путем, если воспользоваться диаграммой Тs. Нетрудно видеть (рис. 2.2), что элементарная площадка аbcd = Tds = dq, a площадь АВСD = = q.
Таким образом, в системе координат Тs площадь, ограниченная кривой процесса, осью абсцисс и крайними ординатами численно равна подведенной (отведенной) теплоте. Поэтому Тs- диаграмму иначе называют тепловой.
Следует добавить, что по изменению энтропии в обратимых процессах можно сделать вывод, о направлении теплообмена.
Как следует из уравнений (2.10) знак dq и знак ds совпадают, т.к. абсолютная температура сугубо положительная величина.
Если рассмотреть совместно уравнения (2.7), (2.8) и (2.10), то уравнение первого начала может быть приведено к виду
Тds = du + pdv. (2.12)
T
а
d
b
c
T
A
B
C
D
P








B


b
p
c


C
а
d
A
D
ds
S
dv
V

Рис. 2.1. Рис. 2.2.
