
- •Линейные полиэфиры
- •Основные стадии образования полиэфиров
- •Число функциональных групп в кислотах и спиртах
- •Величина и строение молекул кислот и спиртов
- •Механизм реакции этерефикации
- •Сырьё для производста полиэфиров
- •Диэтиленгликоль но – сн2– сн2–о– сн2– сн2–он
- •Полиэтилентерефталат
- •Технологический процесс производства пэтф
- •Свойства, переработка и применение пэтф
- •Волокно
- •Полиэтиленфталат
- •Поликарбонаты
- •Свойства, применение и переработка поликарбонатов
- •Переработка поликарбонатов
- •Поликонденсация хлорангидридов дикарбоновых кислот с двухатомными фенолами при повышенных температурах
- •Межфазная полиэтерефикация
- •Основные типы полиарилатов
- •Свойства, применение и переработка полиарилатов
- •Ненасыщенные полиэфиры
- •Мономеры
- •Инициаторы и ускорители
- •Реакция обрыва
- •Ингибиторы, стабилизаторы
- •Наполнители и красители
- •Производство ненасыщенных полиэфиров
- •Растворение олигомера в мономере
- •Марки ненасыщенных полиэфирных олигомеров
- •Свойства и применение ненасыщенных полиэфиров
Сырьё для производста полиэфиров
Этиленгликоль НО – СН2– СН2–ОН
t кип.= 197,50С; ρ = 1,115 г/см3.
В технике получают из этилена.
I стадия: обработка этилена гипохлоритом (НОСl) и получение этиленхлоргидрина НО– СН2– СН2–Сl
II
стадия: дегидрохлорирование
этиленхлоргидрина при добавлении
гашеной известии получение окиси этилена
![]() .
.
III стадия: реакция гидратации окиси этилена до этиленгликоля.
Окись этилена может получаться прямым окислением этилена кислородом воздуха при t 200-3000С.
Этиленгликоль – гигроскопичная бесцветная жидкость, почти без запаха, смешивается с водой и спиртом во всех соотношениях.
Диэтиленгликоль но – сн2– сн2–о– сн2– сн2–он
t кип.=245,8 0С; ρ = 1,118 г/см3.
Получается при взаимодействии этиленгликоля и окиси этилена при 1000С. Диэтиленгликоль - гигроскопичная бесцветная жидкость с очень слабым запахом. С водой и спиртом смешивается во всех соотношениях.
Фталевая
кислота
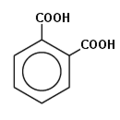 имеет две карбоксильные группы,
расположенные в орто – положении
бензольного ядра и способные образовывать
ангидридную связь, поэтому чаще используют
не кислоту, а ангидрид.
имеет две карбоксильные группы,
расположенные в орто – положении
бензольного ядра и способные образовывать
ангидридную связь, поэтому чаще используют
не кислоту, а ангидрид.
Получают фталевый ангидрид окислением нафталина кислородом воздуха в газовой фазе над ванадиевым катализатором.
Фталевый ангидрид получают в промышленности окислением нафталина или о-ксилола:

Применяется синтез фталевого ангидрида окислением орто – ксилола воздухом над ванадиевым катализатором.
Фталевый ангидрид – прозрачные кристаллы с t пл.= +12 0С, растворимые в воде, спирте, эфире.
Терефталевая кислота является пара – изомером фталевой кислоты.
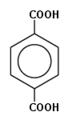
Основной метод синтеза – окисление пара – ксилола. Трудности при очистке терефталевой кислоты (она сублимируется без разложения при t = 3000С) привели к тому, на производстве получают её диметиловый эфир, легко поддающийся тщательной очистке.
Диметилтерефталат по сравнению с кислотой более низкую температуру плавления. Лучше всего его очищать перегонкой в вакууме, а затем кристаллизацией из метанола. Диметилтерефталат имеет t пл.= 1420С со значительной сублимацией.
Диметилтерефталат
(диметиловый
эфир
терефталевой кислоты):
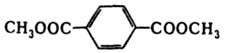
Из большого числа разнообразных линейных полиэфиров практическое применение нашли полимеры на основе этиленгликоля и кислот: фталевой, адипиновой, себациновой и терефталевой, а такжена основе ароматическихдиоксисоединений и угольной кислоты (поликарбонаты).
Полиэтилентерефталат
Описаны три способа получения полиэтилентерефталата (ПЭТФ).
Прямое взаимодействие терефталевой кислоты и гликоля, взятого в избытке в присутствии катализатора этерефикации.
Переэтерефикация низших эфиров терефталевой кислоты и гликоля, взятого в избытке в присутствии катализатора этерефикации.
Взаимодействие хлорангидрида кислоты и этиленгликоля в среде инертного разбавителя (например, хлороформа) в присутствии щелочного катализатора (например, пиридина).
Низкомолекулярные полиэфиры, полученные по любому из способов, могут превращаться в высокомолекулярные полимеры нагреванием в атмосфере инертного газа. Реакция заканчивается при уменьшенном давлении.
Первый и третий методы синтеза практически не нашли применения. В промышленности применяется метод переэтерификации между диметилтерефталатом и этиленгликолем с последующей поликонденсацией дигликольтерефталата.
Процесс производства ПЭТФ можно представить следующей схемой, включающей две стадии:
1. Переэтерификация
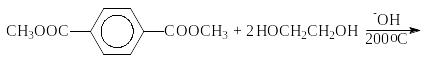
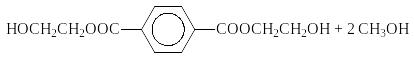
2. Поликонденсация
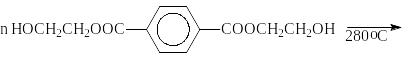
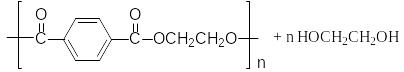
Концевые группы:
и –ОСН2СН2ОН.
Важнейшие преимущества этого метода – более простая очистка диметилового эфира и его повышенная растворимость в этиленгликоле. Диметитилтерефталат плавится при 1420С и может быть хорошо очищен путём перегонки и перекристаллизации.
Для ускорения реакций используются катализаторы. Алкоголяты щелочных металлов обычно применяются в качестве катализатора реакции переэтерификации сложных эфиров, вызывают окраску расплава полимера. В большинстве случаев используются алкоголяты цинка, свинца, магния и сурьмы.
Наряду с описанной ранее реакцией пертеэтерификации протекают также некоторые побочные реакции, оказывающие влияние на структуру образующегося полиэфира. К их числу можно отнести образование простых эфирных связей при взаимодействии гидроксильных групп, приводящих к получению сегментов дигликолевого эфира, вследствие чего несколько снижается температура плавления ПЭТФ, а также образование карбоновых кислот за счёт разложения сложноэфирных групп.
...–СН2СН2ОН + ОНСН2СН2–... → ...–СН2СН2ОСН2СН2–... +Н2О

СООН
+ СН2=СН –...Последние реакции препятствуют получению полиэфиров с большим молекулярным весом, тек как происходит уменьшение числа гидрокисльных групп, необходимых для дальнейшего роста полимерной цепи.
