
- •Линейные полиэфиры
- •Основные стадии образования полиэфиров
- •Число функциональных групп в кислотах и спиртах
- •Величина и строение молекул кислот и спиртов
- •Механизм реакции этерефикации
- •Сырьё для производста полиэфиров
- •Диэтиленгликоль но – сн2– сн2–о– сн2– сн2–он
- •Полиэтилентерефталат
- •Технологический процесс производства пэтф
- •Свойства, переработка и применение пэтф
- •Волокно
- •Полиэтиленфталат
- •Поликарбонаты
- •Свойства, применение и переработка поликарбонатов
- •Переработка поликарбонатов
- •Поликонденсация хлорангидридов дикарбоновых кислот с двухатомными фенолами при повышенных температурах
- •Межфазная полиэтерефикация
- •Основные типы полиарилатов
- •Свойства, применение и переработка полиарилатов
- •Ненасыщенные полиэфиры
- •Мономеры
- •Инициаторы и ускорители
- •Реакция обрыва
- •Ингибиторы, стабилизаторы
- •Наполнители и красители
- •Производство ненасыщенных полиэфиров
- •Растворение олигомера в мономере
- •Марки ненасыщенных полиэфирных олигомеров
- •Свойства и применение ненасыщенных полиэфиров
Число функциональных групп в кислотах и спиртах
При взаимодействии двухосновных кислот с двухатомными спиртами образуются полиэфиры, состоящие из смеси полимеров, имеющих линейное строение. Рост полиэфира может происходить с одного или обоих концов цепи (при условии, что не происходят побочные реакции) и поэтому получается линейный продукт.
В тех случаях, когда число функциональных групп хотя бы одного из компонентов превышает два, а другого – не менее двух, в результате поликонденсации будут образовываться трёхмерные молекулы. Например, при реакции этиленгликоля и фталевой кислоты образуется линейный полиэтилентерефталат, а реакция между фталевой кислотой и глицерином приводит к образованию продуктов с трёхмерными связями.
Величина и строение молекул кислот и спиртов
Активность функциональных групп исходных молекул зависит от их строения и величины. Первичные гидроксильные группы более реакционноспособны, чем вторичные. Так в глицерине вторичные ОН-группы проявляют свою активность лишь при температурах более 1800С, тогда как первичные при значительно более низких температурах реагируют с кислотами.
На скорость реакции поликондесации влияет также молекулярный вес исходного реагента. Для учёта этой зависимости введено понятие удельной функциональности моноэфира, образованного из соответствующей кислоты и спирта.
Удельная функциональность показывает наибольшее число свободных функциональных групп, приходящихся на единицу молекулярного веса, которое может быть использовано в реакции поликонденсации.
Удельная функциональность выражается формулой:
∆
=
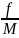 ,
где f
- число функциональных групп в молекуле
мономераЭ
,
где f
- число функциональных групп в молекуле
мономераЭ
M – молекулярный вес моноэфира.
С увеличением ∆ возрастает скорость образования полимера. Например, ∆ будет больше у пентаэритритовых эфиров различных кислот по сравнению с диэтиленгликолевыми эфирами тех же кислот.
Очень
часто вследствие неодинаковой реакционной
способности функциональных групп
(например, первичных и вторичных
ОН-групп), пространственных затруднений,
возникающих в ходе реакции и других
причин используются не все функциональные
группы. Поэтому применяют фактически
используемую удельную функциональность
(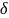 ):
):
= ∆ • p , где p – степень завершённости реакции.
Строение реагирующих в значительной степени определяет многие физические и химические свойства. Большинство линейных полиэфиров имеет кристаллическое строение, что позволяет получить из них волокна. При этом кристалличность будет зависеть от строения полиэфира, наличия гетероатомов, ненасыщенных связей, боковых групп, длины цепей гликоля и т.д.
Все линейные полиэфиры имеют сравнительно низкую температуру плавления. Для её увеличения в полимер вводят ароматические ядра.
Механизм реакции этерефикации
Полиэфиры получают чаще всего методом равновесной поликонденсации дикарбоновых кислот с гликолями. Характерным для равновесной поликонденсации является взаимодействие низкомолекулярного вещества и полимеров, образующихся в результате реакций, что приводит к разрушению образовавшихся связей макромолекулярных цепей и образованию функциональных групп исходных веществ. Чтобы превращение было максимальным равновесие сдвигают в сторону образования полимера, путём удаления из реакционной системы низкомолекулярного продукта реакции.
Реакция этерефикации катализируется протонами, источником которых является или исходная дикарбоновая кислота или кислота, специально введённая в качестве катализатора. Механизм можно изобразить следующей схемой:
Карбоксильная группа реагирует с протоном, образуя ион карбония.
:ӦH
˗ R
– C
R
– C Oᵟ+
+ H+
Oᵟ+
+ H+
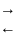 ˗
R
– C+
˗
R
– C+
:O̤H :O̤H
Ион карбония реагирует с оксигруппой гликоля с образованием нового катиона.
:ӦH :ӦH
˗ R
– C+
+ :Ӧ – R1
R
– C+
+ :Ӧ – R1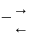 ˗
R
– C
- Ӧ+–
R1
-
˗
R
– C
- Ӧ+–
R1
-
:O̤H H :O̤H H
Катион стабилизируется, элиминируя протон.
:ӦH :ӦH
˗
R
– C
- Ӧ+–
R1
-
˗
R
– C
–
 – R1
– R1
:O̤H H :O̤H + H+
Протон реагирует с одной из оксигрупп с образованием иона оксония.
:ӦH :ӦH
˗ R – C – – R1 ˗ R – C – – R1
:O̤H + H+ :O+H
H
Ион оксония переходит в ион карбония, элиминируя воду.
:ӦH :ӦH
˗ R – C – – R1 ˗ R – Cᵟ+ – – R1 + H2O
:O+H
H
Положительно заряженный атом углерода «оттягивает» электронную пару, образующую связь ОН, что приводит к образованию сложноэфирной связи и протона, способного вновь катализировать реакцию этерефикации:
:ӦH O
˗ R – Cᵟ+ – – R1 ˗ R – C – – R1 + H+
Механизм реакции был доказан применением спирта или кислоты, содержащих изотоп О18 в группе ОН.
ПОЛИЭФИРЫ
Химическая классификация ВМС
Вещества, цепь которых построена из атомов одного какого-либо элемента – гомоцепные соединения (углерод – карбоцепные).
Вещества, цепь которых включает атомы C, O, N, S, Si и др., называются гетероцепными.
В каждом из этих классов устанавливается подразделение по отдельным группам, в зависимости от строения цепи, наличия в ней двойных связей, а во втором классе от наличия количества и природы гетероатомов.
Одна из групп гетероцепных соединений – группа кислородосодерщащих цепей (полиэфиры).
... – СН2 – О – СН2 – О – СН2 – О –...
... – (СН2)n – CО – O– (СН2)n – CО – O–...
Полиэфиры включают несколько групп различных ВМС, сильно отличающихся по своему строению.
Прежде всего следует различать простые и сложные полиэфиры.
Первые характеризуются наличием в их молекулах простых связей
– О –, а вторые – группой – CО – O–.
Второе подразделение вводим в зависимости от строения основной
цепи макромолекулы полимера, и исходя из этого полиэфиры могут принадлежать к одной из двух основных групп:
- карбоцепные соединения;
- гетероцепные соединения.
К карбоцепным относятся полиэфиры, у которых цепь макромолекулы построена из атомов углерода, а эфирные группировок находятся в боковых ответвлениях. Примером являются поливинилацетат
[—CH2—CH (OCOCH3)—]n, полиметилметакрилат
[-СН2С(СН3)(СООСН3)-]n.
К гетероцепным относятся полиэфиры, содержащие эфирные группировки в основной цепи макромолекулы. Примером гетероцепных полиэфиров являются полигексаметиленадипинат
[-(CH2)6OOC(C2H2)4COO-],
полиэтилентерефталат
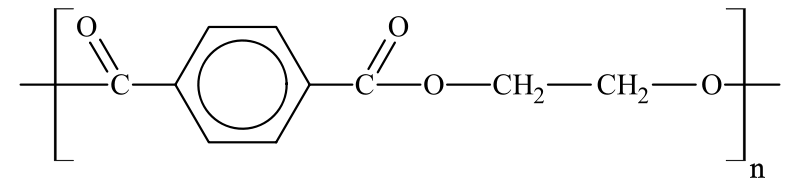
поликапролактон [-(CH2)6COO-] и др.
Дальнейшее подразделение сложны гетероцепных полиэфиров на группы и подгруппы происходит в зависимости от строения основного звена макромолекулы:
Гетероцепные макромолекулы с алифатическим звеном:
с насыщенным звеном;
с насыщенным звеном, содержащим гетероатомы (O, S);
с ненасыщенным звеном;
с циклическим звеном.
Гетероцепные полиэфиры с ароматическим звеном
Гетероцепные полиэфиры с гетероциклическим звеном, содержащим O, S и т. п.
Каждая из этих групп в свою очередь подразделяется в зависимости от наличия заместителей, их природы, количества:
алкильные (арильные) группы;
галоидные атомы;
спиртовые группы;
эфирные группы;
альдегидные группы;
кислотные группы;
амино – группы;
нитро-группы.
Применение этой классификации позволяет легко разобраться в массе соединений, относящихся к полиэфирам.
