
- •Москва 2015
- •1. Введение
- •1.1. Классификация органических соединений
- •1.2. Номенклатура органических соединений.
- •Названия некоторых органических соединений и радикалов
- •2. Строение органических соединений Различные виды изомерии
- •2.1. Пространственное строение органических соединений
- •2.2. Электронное строение органических соединений
- •3. Основные закономерности протекания органических реакций
- •3.1. Типы реагентов
- •3.2. Способы разрыва ковалентной связи
- •3.3 Классификация органических реакций
- •1) По типу разрыва связей в субстрате и реагенте
- •6) Хемо- регио- и стереоселективные реакции
- •3.4 Факторы, определяющие реакционную способность органического соединения
- •4. Кислотно-основные свойства органических соединений
- •5. Свободно-радикальные реакции
- •6. Электрофильные реакции
- •6.1. Реакции электрофильного присоединения
- •6.2. Реакции электрофильного замещения в ароматическом кольце (se)
- •7.1. Реакции нуклеофильного замещения у sp3-гибридизованного атома углерода
- •7.2. Реакции элиминирования (е)
- •8. Реакционная способность соединений с карбонильной группой
- •8.1. Реакции нуклеофильного присоединения (an) к альдегидам и кетонам
- •8.2. Реакции нуклеофильного замещения у карбонильной группы в карбоновых кислотах и их функциональных производных (sn)
- •8.3. Реакции карбонильных соединений с участием подвижного α-водородного атома (сн-кислотного центра)
- •Содержание
- •1. Введение
- •1.1 Классификация органических соединений 3
7.1. Реакции нуклеофильного замещения у sp3-гибридизованного атома углерода
SN реакции моногалогенопроизводных R–Hal (Hal = Cl, Br, I)
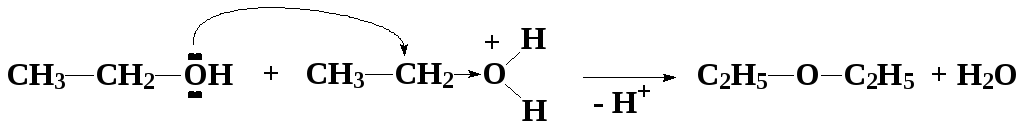
Получение спиртов и простых эфиров
R–Hal + NaOH(водн. р-р) → R–OH + NaHal
R–Hal + RONa → R–O–R + NaHal
R–Hal + R’ONa → R–O–R’ + NaHal
Получение тиолов, диалкилсульфидов (простых тиоэфиров) и солей триалкилсульфония
R–Hal + NaSH → R–SH + NaHal
2R–Hal + Na2S → R–S–R + 2NaHal
R–Hal + R’SNa → R–S–R’ + NaHal
R–Hal
+ R”SR’
→
 + NaHal
+ NaHal
Получение аминов
R–Hal + 2NH3 → R–NH2 + NH4Cl
Общая схема реакций нуклеофильного замещения

Ассоциативный механизм SN2

переходное состояние
Диссоциативный механизм SN1
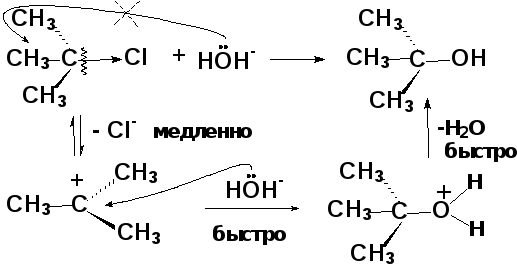
карбокатион ион оксония
Концепция хороших и плохих уходящих групп
Чем сильнее кислота, сопряженная уходящей группе в реакции нуклеофильного замещения, тем легче уходит эта группа

Биологически важные реакции нуклеофильного замещения
Гидролиз галогенопроизводных
а) соединения с неподвижным атомом галогена (винил и арилгалогениды)

Повышенная электронная плотность у атома углерода, связанного с галогеном, препятствует протеканию реакции по механизму SN2. Механизм SN1 также маловероятен, так как соответствующие карбокатионы очень неустойчивы.
н атри Натрия
амидотриазоат, рентгеноконтрастный
атри Натрия
амидотриазоат, рентгеноконтрастный
- препарат. В таких соединениях в условиях жи-
вого организма атом галогена не удаляется
(см. также тироксин и диоксин на стр. 40)
б) соединения с нормальной подвижностью атома галогена (алкилгалогениды). Гидролизуются разбавленными растворами щелочей.
Этилхлорид CH3CH2Cl — местноанестезирующее средство; хлороформ CHCl3 — средство для ингаляционного наркоза; йодоформ CHI3 — антисептическое (обеззараживающее) средство; дихлорэтан CH2ClCH2Cl – растворитель, обладает токсическим действием, воздействует на ЦНС, печень, в условиях организма частично подвергается гидролизу.
в) соединения с подвижным атомом галогена (постепенно гидролизуются водой, обладают раздражающим и слезоточивым действием)
Аллил- и бензилгалогениды:

![]()
α-галогенозамещенные карбонильные соединения:

реакция идет
по механизму SN2
Замещение гидроксильной группы
Гидроксигруппа (-ОН) — плохая уходящая группа, замещение может происходить, если ее предварительно превратить в хорошую, например, в молекулу воды, что достигается при помощи кислотного катализа.

ион оксония
или

ион оксония карбокатион
Замещение аминогруппы (дезаминирование)
Аминогруппа (–NH2) — очень плохая уходящая группа (сопряженная кислота – молекула аммиака), однако под действием азотистой кислоты за счет окислительно-восстановительной реакции она превращается в очень хорошую уходящую группу – молекулу азота:
![]()
Реакции алкилирования
Алкилирование — введение в молекулу насыщенного углеводородного радикала (в более общем случае под алкилированием могут подразумевать введение любого органического остатка).
Общая схема реакций алкилирования (в случае реакций SN):

Пример — последовательность реакций исчерпывающего метилирования аммиака метилиодидом:


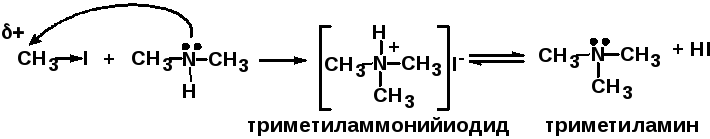

Биологически важные алкилирующие реагенты:

Образование главного метилирующего реагента в живом организме6

Примеры реакций алкилирования


уходящая группа

 уходящая
группа
уходящая
группа

противоопухолевый препарат уходящая группа
миелосан
Наращивание цепи гликогена:

АДФ-глюкоза гликоген уходящая группа (АДФ)
Биосинтез холина из коламина:
![]()
S-аденозил коламин холин уходящая группа
метионин S-аденозилгомоцистеин)
