
- •«Национальный исследовательский томский политехнический университет» грунтоведение
- •Предисловие
- •Введение
- •1. История развития и задачи грунтоведения
- •2. Состав грунтов
- •2.1. Минеральная компонента грунтов
- •2.1.1. Типы связей, состав и свойства минерального вещества грунтов
- •2.1.1.1. Типы связей в твердых компонентах грунтов
- •2.1.1.2. Состав и свойства первичных силикатов
- •2.1.1.2.1. Состав, строение и свойства глинистых минералов
- •2.1.1.3. Состав и свойства простых солей
- •2.1.1.4. Состав и свойства сульфидов и металлических соединений
- •2.1.2. Классификационные показатели грунтов, содержащих минеральную компоненту
- •2.1.2.1. Классификационные показатели скальных грунтов
- •2.1.2.2. Классификационные показатели техногенных грунтов
- •2.1.2.3. Классификационные показатели дисперсных грунтов
- •2.1.2.4. Классификационные показатели элювиальных грунтов
- •2.1.3. Определение минералогического состава грунтов
- •2.1.4. Определение гранулометрического состава дисперсных грунтов
- •2.2. Органическая компонента грунтов
- •2.2.1. Распространение, состав и свойства органического вещества в грунтах
- •2.2.2. Классификационные показатели грунтов содержащих органическую компоненту
- •2.2.2.1. Классификационные показатели органоминеральных грунтов и их определение
- •2.2.2.2. Классификационные показатели органических грунтов и их определение
- •2.3. Ледяная компонента грунтов
- •2.3.1. Распространение, состав и свойства льда в грунтах
- •2.3.2. Классификационные показатели грунтов содержащих ледяную компоненту
- •2.3.3. Распространение, состав и свойства газогидратов
- •2.4. Жидкая компонента грунтов
- •2.4.1. Распространение, классификация, состав и свойства жидкой компоненты грунтов
- •2.5. Газовая компонента грунтов
- •2.5.1. Распространение, состав и свойства газовой компоненты грунта
- •2.5.2. Характеристики газовой компоненты грунта
- •2.6. Биотическая компонента грунтов
- •2.6.1. Распространение, состав биоты грунтов
- •2.6.2. Биологическая активность грунта и ее показатели
- •3. Требования к описанию, отбору, хранению, транспортировке и качеству образцов грунта
- •3.1. Требования к описанию образцов грунта
- •3.2. Требования к отбору, хранению, транспортировке и качеству образцов грунта
- •4. Физические свойства грунтов
- •4.1. Влажность грунтов
- •4.2. Консистенция грунта и ее характеристики
- •4.3. Плотность грунтов
- •4.4. Пористость грунтов
- •5. Гидрофизические свойства грунтов
- •5.1. Водопроницаемость грунтов
- •5.2. Водопрочность грунтов
- •5.2.1. Размокаемость грунтов
- •5.2.2. Размягчаемость грунтов
- •5.2.3. Размываемость грунтов
- •5.3. Набухание грунтов
- •5.4. Усадочность грунтов
- •5.5. Просадочность лессовых и лессовидных грунтов
- •6. Теплофизические свойства грунтов
- •6.1. Показатели теплофизических свойств грунтов
- •6.2. Пучинистые свойства грунтов
- •7. Химические свойства грунтов
- •7.1. Растворимость грунтов, ее основные характеристики и методы их определения
- •7.2. Агрессивность грунтов по отношению к бетону и металлам
- •7.2.1. Химическая и биологическая агрессивность грунтов по отношению к бетону
- •7.2.2. Коррозия металлических элементов подземных конструкций
- •7.2.2.1. Определения коррозионной активности грунтов по химическому составу водной вытяжки
- •7.2.2.2. Определение удельного электрического сопротивления грунта и средней плотности катодного тока
- •7.2.2.3. Определение коррозии металлов блуждающим током
- •7.2.2.3. Определение признаков биохимической коррозии
- •8. Физико-механические свойства грунтов
- •8.1. Основные понятия о напряжениях и деформациях в грунтах
- •8.2. Реологические свойства грунтов
- •8.3. Деформационные свойства грунтов и определение их показателей
- •8.3.1. Деформационные свойства грунтов
- •8.3.2. Определение характеристик деформируемости при компрессионных испытаниях дисперсных грунтов
- •8.3.2.1. Определение показателей деформации просадочных грунтов
- •8.3.2.2. Определение характеристик деформации набухающих грунтов
- •8.3.2.3. Определение характеристик деформации засоленных грунтов
- •8.3.2.4. Определение характеристик деформации мерзлых грунтов
- •8.3.3. Определение характеристик консолидации грунтов
- •8.4. Прочностные свойства грунтов и определение их показателей
- •8.4.1. Сопротивление грунтов сдвигу
- •8.4.1.1. Определение показателей прочности на сдвиг дисперсных грунтов
- •8.4.1.2. Определение показателей прочности на сдвиг мерзлых грунтов
- •8.4.1.3. Определения показателей прочности скального грунта при срезе со сжатием
- •8.4.2. Определение угла естественного откоса грунтов
- •8.4.3. Сопротивление грунтов одноосному растяжению
- •Временное сопротивление разрыву скальных грунтов [50]
- •8.4.4. Сопротивление грунтов изгибу
- •8.5. Определение показателей прочности и деформируемости грунтов методом одноосного сжатия
- •8.5.1. Определение показателей прочности и деформируемости связных и полускальных грунтов
- •8.5.2. Определение показателей прочности и деформируемости скальных грунтов
- •8.5.3. Определение показателей прочности и деформируемости мерзлых грунтов
- •8.6. Определение показателей прочности и деформируемости грунтов методом трехосного сжатия
- •8.6.1. Определение показателей прочности и деформируемости дисперсных грунтов
- •8.6.2. Определение показателей прочности и деформируемости скальных грунтов
- •8.7. Определение показателей твердости, крепости, выветрелости и истираемости грунтов
- •8.8. Особенности определения параметров физико-механических свойств переуплотненных грунтов
- •8.9. Динамические свойства грунтов
- •8.9.1. Определение показателей динамических свойств грунтов
- •8.9.2. Разжижение грунтов
- •9. Классификации грунтов
- •9.1. Виды классификаций грунтов в инженерной геологии
- •9.2. Общая классификация грунтов
- •Список литературы
- •8.5. Определение показателей прочности и деформируемости грунтов методом одноосного сжатия 393
2. Состав грунтов
Грунт – это минеральная или органическая, органоминеральная, многокомпонентная, многофазовая динамическая система, которая изучается в инженерно-геологическом отношении. Составляющими компонентами грунтовой системы являются (рис. 2.1): твердая компонента (минеральная, ледяная и органическая составляющие), жидкая компонента (содержащиеся в пустотах пород природные воды), газообразная компонента (газы в пустотах пород) и биотическая живая компонента (макро- и микроорганизмы, обитающие в горных породах) [50].
Соотношение компонент в грунтах определяет их состояние и свойства. В зависимости от того, полностью или частично будут заполнены поры водой (или газом) и содержатся в них живые микроорганизмы или нет, грунты могут являться двух- трех- и четырехкомпонентными системами. Если грунт состоит из твердых частиц и все поры заполнены водой, то он является двухфазной системой. В большинстве случаев в грунте кроме твердых частиц и воды имеется воздух или иной газ, либо растворенный в воде, либо находящийся в виде пузырьков. Такой грунт является трехфазной системой. Содержащийся в грунте лед придает ему специфические свойства, которые приходится учитывать, особенно при строительстве в районах распространения вечномерзлых грунтов. Мерзлый грунт является четырехфазной системой. В некоторых грунтах присутствуют органические вещества в виде растительных остатков или гумуса. Наличие даже сравнительно небольшого количества таких веществ в грунте существенно отражается на его свойствах.
2.1. Минеральная компонента грунтов
2.1.1. Типы связей, состав и свойства минерального вещества грунтов
2.1.1.1. Типы связей в твердых компонентах грунтов
Рис. 2.1. Соотношение
грунтовых компонент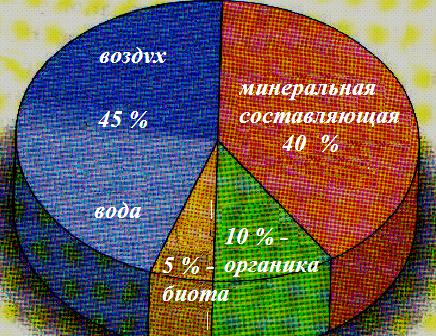
Наибольшее значение имеют минералы класса первичных силикатов, у которых преобладают внутрикристаллические связи ионно-ковалентного типа; простые соли (карбонаты, сульфаты, галоиды), имеющие ионный тип связей; глинистые минералы (гидрослюды, монтмориллонит, каолинит и др.), характеризующиеся большим разнообразием внутрикристаллизационных связей. Кроме того, в грунтах в значительном количестве может содержаться органическое вещество, в строении которого присутствуют водородные и молекулярные связи.
Свойства минералов, которые в свою очередь обусловливают свойства грунтов, связаны с особенностями их химического состава, внутреннего строения и связей, которые существуют внутри самих минералов (атомов, ионов, радикалов). Прочность самих твердых компонент определяется прочностью и характером связей внутри них. Минералы с одинаковым химическим составом могут иметь разную прочность вследствие различий в их кристаллической структуре и характере химических связей внутри самого кристалла, поэтому более обоснованно проводить подразделение твердой компоненты по преобладающему типу связей внутри компоненты – чем прочнее преобладающие в твердой компоненте связи, тем она прочнее.
По характеру связей и определенным пространственным распределением электронов в твердых компонентах грунтов выделяется пять типов связи: ковалентный, ионный, металлический, водородный, молекулярный типы.
Ковалентные связи образуют атомы (или группы атомов) на валентных орбиталях которых имеются не спаренные электроны, обобществление которых ведет к формированию общей для связывающихся атомов электронной пары (по одному электрону от каждого атома). При образовании ковалентной связи из одинаковых атомов распределение электронной плотности в орбиталях связывающихся электронных пар строго симметрично по отношению к обоим атомным центрам (неполярные связи). Атомы с различной электроотрицательностью (валентностью) образуют полярные ковалентные связи, в которых электронное облако связи смешено в сторону более электроотрицательного атома. Ковалентные связи свойственны силикатным минералам, они очень прочны и характеризуются направленностью. Многие кристаллические соединения с ковалентными связями тугоплавкие и обладают высокой твердостью (алмаз) и прочностью. Однако ковалентные связи могут существовать не только в твердых кристаллах, но и в жидкостях (в молекулах воды), а также в органических соединениях (в молекулах органических соединений, например С–С, С–Н, С–N и др., где знак «–» означает ковалентную связь).
Ионные связи образуются кулоновскими силами притяжения противоположно заряженных ионов: катионов и анионов. Ионные связи вследствие своей электростатической природы не обладают направленностью и насыщаемостью. Ненасыщенность ионной связи проявляется в склонности соединений с такой связью к образованию кристаллических решеток, в узлах которых каждый ион окружен максимально возможным числом ионов противоположного заряда. Ионные связи характерны для многих солей (галоидов, сульфатов, карбонатов). Наиболее характерное свойство соединений с ионным типом связи в отличии от ковалентного – растворимость, т. е. их способность к диссоциации ионов в растворах в полярных растворителях. Обусловлено это тем, что энергия сольватации ионов молекулами растворителя выше энергии ионной связи в кристалле.
Металлические связи образуются в соединениях между элементами, обладающими свободными валентными орбиталями и низкой энергией ионизации. Такие связи характерны для всех соединений, относящихся к металлам – веществам, с высокой электро- и теплопроводностью, обусловленными значительной подвижностью электронов в кристаллической решетке.
Металл представляет собой ряд положительных ионов, локализованных в определенных положениях кристаллической решетки погруженных в «море» свободных подвижных электронов, что отличает ненаправленную металлическую связь от направленной ковалентной. Энергия связей между электронами и ядрами в кристаллах металлов относительно мала, она минимальна у щелочных металлов и возрастает с увеличением заряда ядра, достигая наибольших значений у переходных металлов.
Водородные связи представляют собой особый тип так называемой трех-центровой связи типа X – Н ••• V (где знак «–» означает ковалентную связь, а знак «•••» водородную), в которой центральный атом водорода Н, соединенный ковалентной связью с электроотрицательным атомом X (например, атомами О, С, N, S и др.), образует дополнительную связь с атомом V (например, атомами N, О, S и др.), имеющим направленную вдоль линии этой связи не поделенную электронную пару. Различают меж- и внутримолекулярные водородные связи. Водородные связи характерны для водородсодержащих твердых компонентов грунта – льда, кристаллогидратов, некоторых глинистых минералов и др.
Молекулярные связи (силы Ван-дер-Ваальса) обусловлены взаимной поляризацией молекул и поэтому могут возникать как между полярными, так и между различными нейтральными молекулами. Это весьма слабые связи, которые могут существовать в твердых молекулярных кристаллах (например, отвердевших инертных газах, газогидратах и др.), а также в органических твердых компонентах и глинистых минералах. Твердые тела с молекулярными связями имеют низкую точку плавления и заметно сублимируют.
Основываясь на выделении преобладающего типа связи, твердые компоненты грунтов подразделяются на следующие группы, существенно различающихся по своим свойствам:
минералы с преобладанием ковалентных связей – первичные силикаты;
с преобладанием ионных связей – ионные минералы и соли;
с преобладанием металлической связи – металлические соединения;
с преобладанием ковалентной и наличием молекулярных и водородных связей – глинистые минералы;
компоненты с преобладанием молекулярных и наличием ковалентных связей – органическое вещество и органоминеральные комплексы;
компоненты с преобладанием водородных, молекулярных и наличием ковалентных связей – лед и газогидраты [50].
