
- •Лекция 1.
- •Экономические аспекты борьбы с коррозией.
- •Классификация коррозионных процессов.
- •Показатели коррозионной стойкости металлов и сплавов.
- •– Отрицательный весовой показатель, используется, когда в процессе коррозии масса образца уменьшается. Образуются либо хорошо растворимые соединения металла, либо (не сказал что).
- •Атомы водорода в дефектах кристаллической решетки могут образовывать молекулу водорода h2, которая имеет гораздо большие размеры и выйти из кристаллической решетки уже не может.
- •Условие сплошности оксидных плёнок.
- •Логарифмический закон.
- •Механизмы диффузии ионов в кристаллической решётке оксидов.
- •Лекция 4.
- •Способы защиты металлов от газовой коррозии.
- •Оксид легирующего компонента должен обладать меньшей электропроводностью по сравнению с оксидами защищаемых металлов.
- •Активные катионы, перешедшие в раствор электролита.
- •Необратимые потенциалы металлы.
- •Термодинамика коррозионных процессов.
- •Диаграмма коррозионного процесса.
- •Особенности катодной реакции водородной деполяризации.
- •Коррозионные процессы с кислородной деполяризацией.
- •Лекция 8.
- •Влияние процесса водородной деполяризации на кислородную деполяризацию.
- •Особенности катодной реакции ионизации кислорода при коррозии металлов.
- •Способы защиты металлов от процессов коррозии с кислородной деполяризацией.
- •Плёночная теория.
- •Обобщённая анодная поляризационная кривая окисления металлов.
- •Лекция 11.
- •Отрицательный защитный эффект.
- •Практические выводы из теории катодной электрохимической защиты.
- •1. Защита от внешнего источника постоянного тока. Применяют для металлоконструкций из стальных, низко- и средне легированных сталей (3-10%), сплавов меди и титана и других.
- •2. Катодная защита с помощью протектора.
- •Коррозия под действием блуждающих токов. Дренажная защита.
- •Дренажная защита.
- •Анодная электрохимическая защита.
- •Способы перевода коррозионной системы в устойчивое пассивное состояние.
- •Воздействуя на характер анодного процесса металла.
- •Лекция 14.
- •Анодная электрохимическая защита от внешнего источника тока.
- •Защита металлов от коррозии с помощью ингибиторов.
- •Анодные ингибиторы.
- •Катодные ингибиторы.
Логарифмический закон.
Отличается ряд процессов коррозии металла в области низких температур, например, Al, Fe, Zn, Ti. Характеризуется очень резким затуханием скорости коррозии во времени или по толщине оксида по сравнению с параболической зависимостью.


Столь сильное торможение для движения ионов и электронов обусловлено рядом особенностей строения и свойств оксидных плёнок:
-
Оксидные плёнки (Al2O3, TiO2…) являются мощными диэлектриками, они обладают униполярной проводимостью – пропускают через себя катионы, но не электроны. В этом случае электроны двигаются по квантовому (туннельному) механизму за счет очень большой напряженности электрического поля. Оксидные плёнки на таких металлах не бывают толще 50-100 ангстрем.
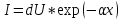
По мере увеличения толщины оксидной плёнки свыше 50-100 А напряженность электрического поля в плёнке уменьшается очень значительно. Этой энергии становится недостаточно чтобы «протащить» электрон или ион через плотно упакованный слой кристаллической решётки оксида.

Механизмы диффузии ионов в кристаллической решётке оксидов.
В зависимости от особенностей кристаллического строения оксида, электронного строения катионов металла, выделяют два механизма движения ионов через оксидную плёнку:
-
Для оксидов металлов, обладающих электронно-ионным типом полупроводимости (n-тип), процесс движения ионов протекает по междоузельным пространствам кристаллической решётки:

В этом случае идёт процесс ионизации катиона Zn в междоузельное пространство за счет протекания реакции ионизации. Чтобы сохранить электронейтральность оксидного слоя, вслед за катионом Zn выходят 2е.
Экспериментально было установлено, что при t ~ 3000 C сверхстехиометрическое содержание Zn2+ по отношению к О2- достигает 0,02 – 0,04 атомных процента. Поэтому такие оксиды, с более низким процентом содержания ионов кислорода, чем катионов металла, принято называть полупроводниками восстановления. Для них характерно, что с ростом повышения содержания кислорода в газовой фазе величина проводимости и скорость окисления уменьшаются, т.к. количество дефектов, т.е. подвижных сверхстехиометрических катионов Zn, в плёнке уменьшается.
Выходя на поверхность оксида, катион цинка достраивает новый узел кристаллической решётки, а пришедшие с ним электроны или участвуют в реакции ионизации адсорбированного атома кислорода, а образующийся ион О2- занимает свой узел рядом с Zn2+, таким образом достраивая кристаллическую решетку оксида.
Чем выше температура, тем больше катионов цинка будет переходить в междоузельное пространство кристаллической решетки, т.е. будет возрастать её дефектность -> градиент концентраций по катионам Zn, а также будут увеличиваться параметры (межионные расстояния), поэтому будет увеличиваться скорость диффузии катионов через слой оксида, а следовательно – и скорость коррозии металла.
Величина проводимости оксида по катионам металла, а следовательно – и скорость коррозии, будет в очень большой степени зависеть от наличия примесей (легирующих компонентов сплава).
-
В состав сплава будем внедрять катионы с меньшей валентностью, чем основной металл. Например, Li+. Два катиона лития заменят в двух узлах кристаллической решётки катионы Zn2+

Электронейтральность
по зарядам в оксидной плёнке нарушена,
поэтому для её установления необходимо,
чтобы в плёнке появился ещё один
сверхстехиометрический катион цинка.

С ростом дефектности, проводимость и скорость диффузии увеличатся, как и скорость коррозии. Например: при t = 3900 C
|
Zn |
K- = 8 * 10-10 |
|
Zn + 0,4% Li |
K- = 2 * 10-7. |
-
Скорость коррозии возросла на 3 порядка. При введении в состав оксидной плёнки катионов металлов с большей степенью окисленности по сравнению с Zn2+, например, Al3+.


Дефектность уменьшится, а следовательно – и скорость диффузии и коррозии. Введение дополнительных катионов в состав оксидной плёнки с целью уменьшения числа подвижных дефектов лежит в основе способа жаростойкого легирования, защиты металлов от коррозии.
-
Для большинства металлов с переменной валентностью, как правило, образуются оксиды с избыточным сверхстехиометрическим содержанием ионов кислорода в оксидной плёнке. Избыток кислорода в плёнке обусловлен наличием в ней незанятых узлов – «дырок» от катионов металлов. Такие оксиды будут обладать электронно-дырочным типом проводимости (p-тип). В данной оксидной плёнке движение ионов и электронов будет протекать по различному типу дефектов. Катионы металла будут двигаться по катионным дефектам – «дыркам», а электроны – по электронным дефектам – катионам металла в высшей степени окисленности.

При этом свойство дырки перемещается на место, откуда катион металла ушёл – вглубь оксидного слоя. Когда дырка дойдёт до границы с металлом, создастся возможность ионизации – выхода катиона из металла в пустой узел кристаллической решетки оксида.
С другой стороны, на границе оксидная пленка / газ, адсорбированный атом кислорода берет е от соседнего катиона металла, который переходит в высшую степень окисления, становится электронным дефектом и может передавать электроны от катионов никеля из более глубоких слоёв. Когда он дойдёт до металла, он будет собирать (передавать) электроны, оставленные там при ионизации катиона Ni в «дырку».
