
- •Лекция 1.
- •Экономические аспекты борьбы с коррозией.
- •Классификация коррозионных процессов.
- •Показатели коррозионной стойкости металлов и сплавов.
- •– Отрицательный весовой показатель, используется, когда в процессе коррозии масса образца уменьшается. Образуются либо хорошо растворимые соединения металла, либо (не сказал что).
- •Атомы водорода в дефектах кристаллической решетки могут образовывать молекулу водорода h2, которая имеет гораздо большие размеры и выйти из кристаллической решетки уже не может.
- •Условие сплошности оксидных плёнок.
- •Логарифмический закон.
- •Механизмы диффузии ионов в кристаллической решётке оксидов.
- •Лекция 4.
- •Способы защиты металлов от газовой коррозии.
- •Оксид легирующего компонента должен обладать меньшей электропроводностью по сравнению с оксидами защищаемых металлов.
- •Активные катионы, перешедшие в раствор электролита.
- •Необратимые потенциалы металлы.
- •Термодинамика коррозионных процессов.
- •Диаграмма коррозионного процесса.
- •Особенности катодной реакции водородной деполяризации.
- •Коррозионные процессы с кислородной деполяризацией.
- •Лекция 8.
- •Влияние процесса водородной деполяризации на кислородную деполяризацию.
- •Особенности катодной реакции ионизации кислорода при коррозии металлов.
- •Способы защиты металлов от процессов коррозии с кислородной деполяризацией.
- •Плёночная теория.
- •Обобщённая анодная поляризационная кривая окисления металлов.
- •Лекция 11.
- •Отрицательный защитный эффект.
- •Практические выводы из теории катодной электрохимической защиты.
- •1. Защита от внешнего источника постоянного тока. Применяют для металлоконструкций из стальных, низко- и средне легированных сталей (3-10%), сплавов меди и титана и других.
- •2. Катодная защита с помощью протектора.
- •Коррозия под действием блуждающих токов. Дренажная защита.
- •Дренажная защита.
- •Анодная электрохимическая защита.
- •Способы перевода коррозионной системы в устойчивое пассивное состояние.
- •Воздействуя на характер анодного процесса металла.
- •Лекция 14.
- •Анодная электрохимическая защита от внешнего источника тока.
- •Защита металлов от коррозии с помощью ингибиторов.
- •Анодные ингибиторы.
- •Катодные ингибиторы.
Особенности катодной реакции водородной деполяризации.
-
Перенапряжение выделения водорода очень сильно зависит от природы металла и состояния его поверхности.
Это обусловлено возрастанием каталитической активности и адсорбционной способности.
-
Процессы выделения водорода на катоде сопровождаются подщелачиванием прикатодного пространства либо за счет расходования протонов в кислых средах, либо за счет образования OH-ионов в нейтральных и щелочных средах.
-
Вследствие аномальной подвижности протонов, перенапряжение выделения водорода очень мало зависит от перемешивания раствора (за исключением редких случаев в нейтральных и близких к ним средах (концентрационная поляризация)).
-
Перенапряжение выделения водорода зависит от состава-кислотности среды, оно максимально в нейтральных растворах и уменьшается с ростом концентрации кислоты, т.к. возрастает количество протонов водорода, или щелочи, т.к. идёт сжатие ДЭС, возрастает эффективный скачок потенциала и поверхность приобретает более отрицательный заряд.

-
Перенапряжение выделения водорода зависит от температуры, оно уменьшается на 1-2 мВ при повышении температуры на 1 градус за счёт возрастания плотности тока обмена и средней энергии частиц в электролите.

-
На величину перенапряжения выделения водорода значительное влияние оказывают ПАВ, присутствующие в электролите, при их электростатической адсорбции (хемосорбции) будут происходить изменения в строении ДЭС вплоть до перезарядки (изменения знака), что в значительной степени может сказаться на величине пси-потенциала и плотности тока обмена. Также происходит экранирование части катодной поверхности. Изменяются значения истиной плотности тока.

-
В большинстве случаев, коррозионные процессы с катодным контролем по реакции выделения водорода идут с самоускорением, что обусловлено увеличением катодной поверхности, т.к. по мере растворения анодных участков обнажается всё большее количество примесных участков, с более низким перенапряжением выделения водорода
-
Наиболее эффективным способом уменьшения скорости процессов коррозии с водородной деполяризацией является введение ингибиторов с различным типом действия. В качестве ингибиторов мы можем вводить в состав раствора (агрессивной среды) в небольшом количестве ионы металлов, которые имеют более положительное значение обратимого потенциала реакции ионизации и большее перенапряжение выделения водорода (константу а), чем у защищаемого металла.


+CdSO4

Катионы кадмия из раствора будут восстанавливаться на катодных участках поверхности цинка (на всех микропримесях), поэтому сменится природа металла катода (на кадмий с более высоким перенапряжением выделения водорода). Возрастёт поляризуемость катодного процесса, что приведёт к уменьшению скорости коррозии металла.
Коррозионные процессы с кислородной деполяризацией.
На катоде идёт процесс восстановления молекулярного кислорода – окислителя, растворённого в электролите.
-
В кислой:


В большинстве случаев, PO2 = 1, аH2O = 1

Кислород в данном случае является значительно более мощным окислителем, чем протон водорода, обратимый потенциал катодной реакции ионизации кислорода на 1,23 В более положительный, чем для водородного электрода. Поэтому процесс ионизации кислорода с термодинамической точки зрения является более предпочтительным, чем процесс выделения водорода.
-
Нейтральной и щелочной:

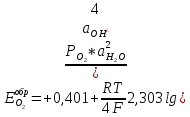
С кинетической точки зрения, коррозионный процесс будет протекать с кислородной деполяризацией, если рабочий потенциал катода будет более отрицателен, чем обратимый потенциал кислородного электрода.
Механизм катодной реакции ионизации кислорода также включает в себя целый ряд стадий:
В общем случае, сам процесс ионизации кислорода на катоде из воздуха включает в себя:
-
Растворение молекулярного кислорода из воздуха в электролите (растворимость кислорода очень мала, ~2.5*10-4 моль/л)

-
Диффузионная доставка молекулярного кислорода к поверхности катода
-
Адсорбция кислорода
-
Ионизация

-
Отвод H2O в объём р-ра
В зависимости от природы лимитирующей стадии, будут различные зависимости для перенапряжения реакции ионизации кислорода от внешних и внутренних факторов.





