
- •Лекция 1.
- •Экономические аспекты борьбы с коррозией.
- •Классификация коррозионных процессов.
- •Показатели коррозионной стойкости металлов и сплавов.
- •– Отрицательный весовой показатель, используется, когда в процессе коррозии масса образца уменьшается. Образуются либо хорошо растворимые соединения металла, либо (не сказал что).
- •Атомы водорода в дефектах кристаллической решетки могут образовывать молекулу водорода h2, которая имеет гораздо большие размеры и выйти из кристаллической решетки уже не может.
- •Условие сплошности оксидных плёнок.
- •Логарифмический закон.
- •Механизмы диффузии ионов в кристаллической решётке оксидов.
- •Лекция 4.
- •Способы защиты металлов от газовой коррозии.
- •Оксид легирующего компонента должен обладать меньшей электропроводностью по сравнению с оксидами защищаемых металлов.
- •Активные катионы, перешедшие в раствор электролита.
- •Необратимые потенциалы металлы.
- •Термодинамика коррозионных процессов.
- •Диаграмма коррозионного процесса.
- •Особенности катодной реакции водородной деполяризации.
- •Коррозионные процессы с кислородной деполяризацией.
- •Лекция 8.
- •Влияние процесса водородной деполяризации на кислородную деполяризацию.
- •Особенности катодной реакции ионизации кислорода при коррозии металлов.
- •Способы защиты металлов от процессов коррозии с кислородной деполяризацией.
- •Плёночная теория.
- •Обобщённая анодная поляризационная кривая окисления металлов.
- •Лекция 11.
- •Отрицательный защитный эффект.
- •Практические выводы из теории катодной электрохимической защиты.
- •1. Защита от внешнего источника постоянного тока. Применяют для металлоконструкций из стальных, низко- и средне легированных сталей (3-10%), сплавов меди и титана и других.
- •2. Катодная защита с помощью протектора.
- •Коррозия под действием блуждающих токов. Дренажная защита.
- •Дренажная защита.
- •Анодная электрохимическая защита.
- •Способы перевода коррозионной системы в устойчивое пассивное состояние.
- •Воздействуя на характер анодного процесса металла.
- •Лекция 14.
- •Анодная электрохимическая защита от внешнего источника тока.
- •Защита металлов от коррозии с помощью ингибиторов.
- •Анодные ингибиторы.
- •Катодные ингибиторы.
Коррозия под действием блуждающих токов. Дренажная защита.
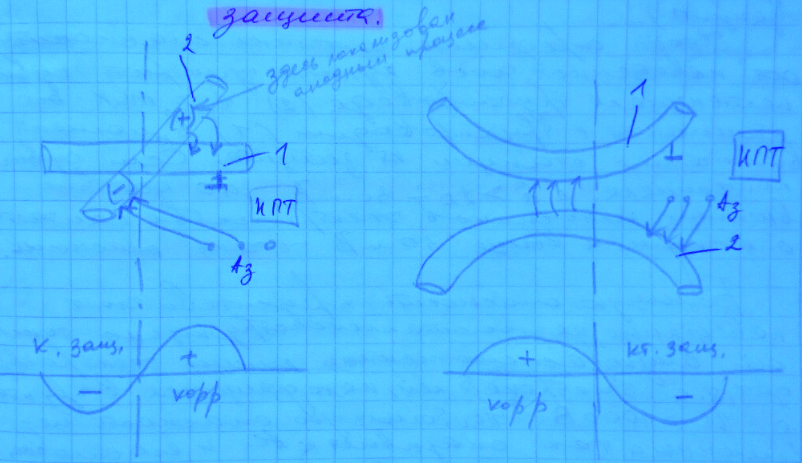
Один трубопровод пересекается с другим. Один под защитой, другой нет. Не защищенный трубопровод оказывается в радиусе действия катодной защиты. В местах максимального сближения оказывается максимальный положительный потенциал, наводятся большие внешние анодные токи. Идёт коррозия. // - болтовня не под запись.
У нас имеются два трубопровода, первый из которых подключен к станции катодной защиты, а второй пересекает его, либо где-то сближается с ним.
В области, максимально близкой к анодным заземлителям, на второй трубопровод будет наводиться более отрицательный потенциал. Входящие в него токи будут катодными и вызовут смещение потенциала в этой области в отрицательном направлении (часть второго трубопровода попадает под действие станции катодной защиты). Но в точке максимального сближения (пересечения) трубопроводов на поверхности трубопровода 2 будет наоборот достигаться максимально положительный заряд, ток будет «стекать» с трубопровода 2 на трубопровод 1. Поэтому в данной области с более положительным потенциалом будет локализован максимальный анодный ток, что будет вызывать разрушение части трубопровода 2. Эти набегающие и стекающие токи для трубопровода 2 и называются блуждающими (наведёнными от станции катодной защиты).
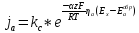
Чтобы определить степень опасности от наведённых токов, необходимо измерить сдвиг потенциала трубопровода 2 в точке максимального сближения с трубопроводом 1 в момент включения станции катодной защиты.
Если
сдвиг потенциала
 ,
то действие внешних источников
электричества считается опасным.
,
то действие внешних источников
электричества считается опасным.


Изменение потенциала на 30 мВ вызовет изменение тока в 10 раз.
Также большую опасность представляют наведённые на металлоконструкцию токи от близко расположенных линий электропередач (электрокабелей), находящихся в грунте, с напряжением >1000 В. Причем наибольшую опасность переменный ток оказывает для алюминия и его сплавов.
Дренажная защита.
Заключается в том, чтобы отвести вредное влияние блуждающих токов от металлоконструкции. Она может быть реализована двумя способами. Для пересекающихся металлоконструкций или пересечений с электрокабелем, в точке их пересечения или минимального удаления друг от друга подключается «жертвенный анод» - протектор, выполненный из того же самого дешевого материала – стального металлолома без изоляции, пучок которого приматывается или приваривается к гибкому медному проводнику и закапывается рядом с защищаемой конструкцией. Силовые линии теперь будут выходить не из трубопровода, а из жертвенного анода, который будет выполнять анодные функции и растворяться.
Второй способ заключается в том, что между трубопроводом и рельсом устанавливается диод и сопротивление, ограничивающее силу тока таким образом, чтобы на трубопровод поступали только отрицательные токи.
Анодная электрохимическая защита.
Основана на сдвиге компромиссного потенциала системы в область более положительных значений – в область полной пассивации, в которой отмечаются минимальные токи коррозии для данного металла.
Условия использования анодной защиты:
-
Область потенциалов полной пассивации сплава (металла) должна быть не менее 500 мВ.

Например, для железа это область потенциалов от -0,1 до +0,8 В; для хрома и легированных хромом сталей – от -0,2 до +0,9 В.
Область потенциала полной пассивации может ограничиваться потенциалом пробоя при наличии в среде анионов-депассиваторов Cl-, Br-, S2-.
-
В области полной пассивации скорость коррозии металла должна быть очень маленькой, чтобы обеспечить данной металлоконструкции необходимую коррозионную стойкость.
-
При наличии двух и более различных металлов и сплавов в металлоконструкции, они все должны иметь одинаковую по потенциалам область полной пассивации.
Анодную защиту эффективно использовать для таких металлов, как железо, хром, никель; легированных хромом, никелем, кремнием и молибденом сталей; сплавов на основе алюминия и титана.
Например, скорость коррозии обычной углеродистой стали в растворах серной кислоты с концентрацией до 20% и выше 60% при анодной защите снижается более, чем в 20 раз.
Коррозия
аппаратов для производства азотных
удобрений ( под анодной защитой уменьшается примерно
в 80 раз.
под анодной защитой уменьшается примерно
в 80 раз.
Изделия
из титана под анодной нагрузкой в
растворах горячей соляной кислоты с
температурой
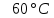 ,
корродируют примерно в 200 раз медленнее,
а в растворах серной кислоты – в 800-1000
раз.
,
корродируют примерно в 200 раз медленнее,
а в растворах серной кислоты – в 800-1000
раз.
Эффективность
анодной защиты определяется
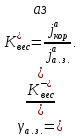
Таким образом, принцип анодной электрохимической защиты заключается в том, чтобы сместить компромиссный потенциал коррозионной системы в область потенциалов полной пассивации, при которых достигается минимальный анодный ток, равный току полной пассивации (зависящий от свойств оксидной плёнки).
