
- •Лекция 1.
- •Экономические аспекты борьбы с коррозией.
- •Классификация коррозионных процессов.
- •Показатели коррозионной стойкости металлов и сплавов.
- •– Отрицательный весовой показатель, используется, когда в процессе коррозии масса образца уменьшается. Образуются либо хорошо растворимые соединения металла, либо (не сказал что).
- •Атомы водорода в дефектах кристаллической решетки могут образовывать молекулу водорода h2, которая имеет гораздо большие размеры и выйти из кристаллической решетки уже не может.
- •Условие сплошности оксидных плёнок.
- •Логарифмический закон.
- •Механизмы диффузии ионов в кристаллической решётке оксидов.
- •Лекция 4.
- •Способы защиты металлов от газовой коррозии.
- •Оксид легирующего компонента должен обладать меньшей электропроводностью по сравнению с оксидами защищаемых металлов.
- •Активные катионы, перешедшие в раствор электролита.
- •Необратимые потенциалы металлы.
- •Термодинамика коррозионных процессов.
- •Диаграмма коррозионного процесса.
- •Особенности катодной реакции водородной деполяризации.
- •Коррозионные процессы с кислородной деполяризацией.
- •Лекция 8.
- •Влияние процесса водородной деполяризации на кислородную деполяризацию.
- •Особенности катодной реакции ионизации кислорода при коррозии металлов.
- •Способы защиты металлов от процессов коррозии с кислородной деполяризацией.
- •Плёночная теория.
- •Обобщённая анодная поляризационная кривая окисления металлов.
- •Лекция 11.
- •Отрицательный защитный эффект.
- •Практические выводы из теории катодной электрохимической защиты.
- •1. Защита от внешнего источника постоянного тока. Применяют для металлоконструкций из стальных, низко- и средне легированных сталей (3-10%), сплавов меди и титана и других.
- •2. Катодная защита с помощью протектора.
- •Коррозия под действием блуждающих токов. Дренажная защита.
- •Дренажная защита.
- •Анодная электрохимическая защита.
- •Способы перевода коррозионной системы в устойчивое пассивное состояние.
- •Воздействуя на характер анодного процесса металла.
- •Лекция 14.
- •Анодная электрохимическая защита от внешнего источника тока.
- •Защита металлов от коррозии с помощью ингибиторов.
- •Анодные ингибиторы.
- •Катодные ингибиторы.
Способы перевода коррозионной системы в устойчивое пассивное состояние.
-
Воздействуя на характер анодного процесса металла.
В общем случае, это воздействие сводится к легированию (например, углеродистой стали хромом, никелем, молибденом и другими металлами).
А) Влияние хрома как легирующего компонента сводится к сдвигу потенциала
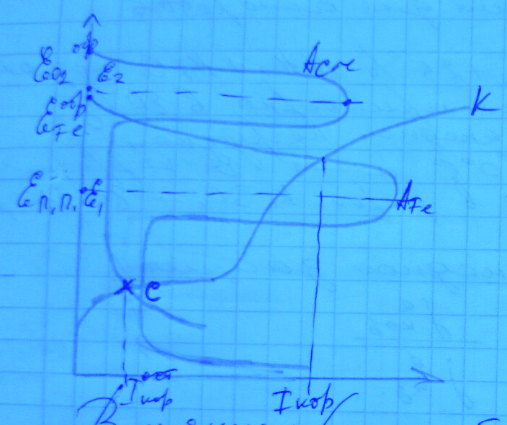
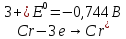


Введение хрома, обладающего более отрицательным потенциалом анодной реакции, выражается сдвигом потенциала в начало пассивации от E1 до E2 в область более электроотрицательных значений. При этом сталь, легированная хромом, будет иметь только одну точку пересечения катодной и анодной поляризационных кривых в области потенциала полной пассивации.
Содержание хрома по отношению к железу должно быть не менее n/8 (12,5%). Меньшее содержание ускорит коррозию.
Б) Легирование сталей никелем и молибденом


Никель и молибден обладают более положительными потенциалами анодных реакций как ионизации, так и образования фазового оксида, по сравнению с железом. Но имеют более отрицательное значение потенциала адсорбции.
За счёт образования адсорбционной плёнки, наблюдается большее торможение анодного процесса и уменьшается ток. Легированная сталь будет находиться в устойчивом пассивном состоянии. Молибден и кремний также способствуют значительному смещению в область более положительных значений потенциала пробоя при наличии в растворе ионов-депассиваторов, расширяя область потенциалов полной пассивации.
Лекция 14.
Способ перевода системы в устойчивое пассивное состояние воздействием на катодный процесс.
-
Если процесс коррозии протекает с чисто кислородной деполяризацией, то повышение аэрации электролита путём принудительного перемешивания электролита, либо барбатажем воздуха. В ряде случаев удаётся достичь величины предельной диффузионной плотности тока больше, чем ток начала пассивации. Тогда система переходит в устойчивое пассивное состояние. Но при отключении перемешивания система вернётся назад в активное состояние с большой скоростью коррозии.

-
С водородной и кислородной деполяризацией. Увеличение агрессивности среды (подкисление электролита) будет смещать обратимые потенциалы водородного и кислородного электродов в область более положительных значений, а также будет уменьшаться перенапряжение выделения водорода. Точка пересечения анодной и катодной поляризационной кривых – одна точка С в области устойчивого пассивного состояния.
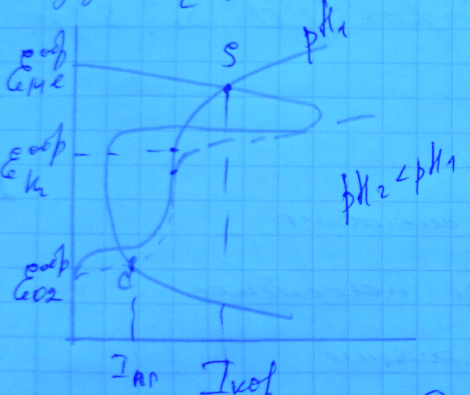
-
Если процесс коррозии протекает с чисто водородной деполяризацией, то введение в состав металла компонентов с очень низким перенапряжением выделения водорода (Pt, Pd, Ag, …) в очень незначительных количествах будет в значительной степени облегчать катодный процесс выделения водорода. Точка пересечения будет в области устойчивого пассивного состояния.

-
Добавление дополнительного окислителя (NO3, Cr2O7, MnO4) в агрессивную среду облегчает катодный процесс. Пересечение находится в области потенциалов полной пассивации. Дополнительные ионы окислителя называются окислительными ингибиторами.

Требования к окислителю:
-
Минимальная плотность тока обмена его катодной реакции.
-
Окислительно-восстановительный (обратимый) потенциал катодной реакции дополнительного окислителя не должен быть сильно положительным; иначе система будет интенсивно корродировать в транспассивной области.
Недостатком использования окислительных ингибиторов является необходимость непрерывного контроля их количества, так как они будут вырабатываться во времени
