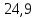- •Лекция 1.
- •Экономические аспекты борьбы с коррозией.
- •Классификация коррозионных процессов.
- •Показатели коррозионной стойкости металлов и сплавов.
- •– Отрицательный весовой показатель, используется, когда в процессе коррозии масса образца уменьшается. Образуются либо хорошо растворимые соединения металла, либо (не сказал что).
- •Атомы водорода в дефектах кристаллической решетки могут образовывать молекулу водорода h2, которая имеет гораздо большие размеры и выйти из кристаллической решетки уже не может.
- •Условие сплошности оксидных плёнок.
- •Логарифмический закон.
- •Механизмы диффузии ионов в кристаллической решётке оксидов.
- •Лекция 4.
- •Способы защиты металлов от газовой коррозии.
- •Оксид легирующего компонента должен обладать меньшей электропроводностью по сравнению с оксидами защищаемых металлов.
- •Активные катионы, перешедшие в раствор электролита.
- •Необратимые потенциалы металлы.
- •Термодинамика коррозионных процессов.
- •Диаграмма коррозионного процесса.
- •Особенности катодной реакции водородной деполяризации.
- •Коррозионные процессы с кислородной деполяризацией.
- •Лекция 8.
- •Влияние процесса водородной деполяризации на кислородную деполяризацию.
- •Особенности катодной реакции ионизации кислорода при коррозии металлов.
- •Способы защиты металлов от процессов коррозии с кислородной деполяризацией.
- •Плёночная теория.
- •Обобщённая анодная поляризационная кривая окисления металлов.
- •Лекция 11.
- •Отрицательный защитный эффект.
- •Практические выводы из теории катодной электрохимической защиты.
- •1. Защита от внешнего источника постоянного тока. Применяют для металлоконструкций из стальных, низко- и средне легированных сталей (3-10%), сплавов меди и титана и других.
- •2. Катодная защита с помощью протектора.
- •Коррозия под действием блуждающих токов. Дренажная защита.
- •Дренажная защита.
- •Анодная электрохимическая защита.
- •Способы перевода коррозионной системы в устойчивое пассивное состояние.
- •Воздействуя на характер анодного процесса металла.
- •Лекция 14.
- •Анодная электрохимическая защита от внешнего источника тока.
- •Защита металлов от коррозии с помощью ингибиторов.
- •Анодные ингибиторы.
- •Катодные ингибиторы.
Показатели коррозионной стойкости металлов и сплавов.
-
Коррозионная стойкость – это способность металла противостоять коррозионному разрушению. Для случая сплошной равномерной коррозии она оценивается по величине глубинного показателя П [мм/год]. По международной классификации и ГОСТ существует единая шкала коррозионной стойкости металлов.
|
Группа |
Балл |
П |
|
Абсолютно стойкие |
1 |
<0,001 |
|
Весьма стойкие |
2 |
0,001 – 0,005 |
|
3 |
0,005 – 0,01 |
|
|
Стойкие |
4 |
0,01 – 0,05 |
|
5 |
0,05 – 0,1 |
|
|
Понижено стойкие |
6 |
0,1 – 0,5 |
|
7 |
0,5 – 1,0 |
|
|
Малостойкие |
8 |
1,0 – 5,0 |
|
9 |
5,0 – 10,0 |
|
|
Нестойкие |
10 |
>10,0 |
Металлы первых двух групп могут быть использованы в качестве конструкционных материалов в чистом виде, без дополнительной защиты. Третья и четвертая группы предусматривают возможность эксплуатации только при использовании определенных способов защиты от коррозии. Пятая и шестая группы предусматривают эксплуатацию металлов только при полной изоляции их от агрессивной среды.
-
– Отрицательный весовой показатель, используется, когда в процессе коррозии масса образца уменьшается. Образуются либо хорошо растворимые соединения металла, либо (не сказал что).
 – масса
образца, выраженная в граммах, S
– поверхность, T
– время в часах.
– масса
образца, выраженная в граммах, S
– поверхность, T
– время в часах.
Показывает убыль массы образца с одного квадратного метра поверхности при коррозии в течении одного часа.
Если в процессе коррозии вес образца увеличивается, когда продукты остаются на поверхности металла, используют положительный весовой показатель:
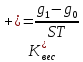

Показывает, какое количество компонента агрессивной среды вступило в реакцию, израсходовалось в процессе коррозии 1 м2 металла за 1 час.
Положительный весовой показатель легко можно пересчитать в отрицательный весовой показатель.


м – изменение валентности агрессивного компонент; к – индекс, число атомов агрессивного компонента в продукте коррозии.
Зная величину отрицательного показателя, легко перейти к глубинному показателю и определить группу и балл стойкости.

d – плотность металла, г/см3.
-
Объемный показатель коррозии
 ,
используется в тех случаях, когда в
коррозионном процессе происходит либо
выделение, либо поглощение газа, объем
которого легко контролировать.
,
используется в тех случаях, когда в
коррозионном процессе происходит либо
выделение, либо поглощение газа, объем
которого легко контролировать.
Показывает количество газа, которое выделилось или поглотилось при коррозии одного квадратного метра металла за 1 час.





-
Токовый показатель
 .
Используя закон Фарадея, токовый
показатель легко привести
.
Используя закон Фарадея, токовый
показатель легко привести



Лекция 2.
Специальные
(функциональные) показатели используются
для избирательных видов коррозии
(например, МКК), где практически нет
изменения внешнего вида, для тонкостенных
деталей удобнее пользоваться омическим
показателем
 .
.
KR – омический показатель.

R0 – сопротивление до коррозионных испытаний, R’ – после.

Для толстостенных деталей - прочностной показатель:
 -
прочностной показатель,
-
прочностной показатель,
 – предел прочности до испытаний и после.
– предел прочности до испытаний и после.
Необходимо
иметь информацию об изменении скорости
коррозии данного металла во времени
(на весь период прогнозируемой
эксплуатации). 




Химическая коррозия.
Химическая коррозия протекает либо в растворах неэлектролитов (органические жидкости, нефть) или в атмосфере сухих газов.
Высокотемпературная газовая коррозия металлов и сплавов.
Причиной химической коррозии является термодинамическая неустойчивость металлов в данной агрессивной среде.

 – процесс
окисления металла термодинамически
разрешен, процесс коррозии протекает
в сторону окисления металла.
– процесс
окисления металла термодинамически
разрешен, процесс коррозии протекает
в сторону окисления металла.
 – условие
термодинамического равновесия, когда
скорость прямой реакции равна скорости
обратной реакции и окисление металла
не протекает.
– условие
термодинамического равновесия, когда
скорость прямой реакции равна скорости
обратной реакции и окисление металла
не протекает.
 –
процесс
окисления металла термодинамически
запрещен.
–
процесс
окисления металла термодинамически
запрещен.
|
|
|
|
|
|
|
|
|
|
|
-239,5 |
-15,6 |
-127,3 |
-46,14 |
-8,51 |
+16,54 |
+62,5 |
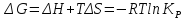
Как
правило, с повышением температуры
 становится более положительным, т.е.
термодинамическая возможность процесса
коррозии уменьшается.
становится более положительным, т.е.
термодинамическая возможность процесса
коррозии уменьшается.
Для
реакции окисления металлов кислородом
воздуха

Где
 – парциальное давление кислорода в
газовой смеси. В воздушной атмосфере
при н.у.
– парциальное давление кислорода в
газовой смеси. В воздушной атмосфере
при н.у.
 .
.
Для
реакций окисления металлов на воздухе
при различных температурах удобнее
пользоваться соотношением величин
 , где PMeO
– упругость диссоциации оксидов.
, где PMeO
– упругость диссоциации оксидов.
Если
 ,
то процесс коррозии термодинамически
разрешен, а если наоборот, то в данной
области температур сформированный
ранее оксид металла будет разлагаться
на чистый металл и кислород (т.е. реакция
пойдёт в обратном направлении).
,
то процесс коррозии термодинамически
разрешен, а если наоборот, то в данной
области температур сформированный
ранее оксид металла будет разлагаться
на чистый металл и кислород (т.е. реакция
пойдёт в обратном направлении).
Упругость диссоциации некоторых оксидов от температуры:
|
|
|
|||
|
|
|
|
|
|
|
300 |
|
- |
- |
- |
|
400 |
0,69 |
- |
- |
- |
|
500 |
|
|
|
|
|
800 |
360 |
|
|
|
|
1000 |
- |
|
|
|
|
2000 |
- |
|
|
|
Серебро при н.у. будет окислятся на воздухе, т.к. упругость диссоциации его оксида меньше парциального давления кислорода. При температуре выше 119 С процесс окисления серебра будет термодинамически запрещен, т.к. упругость диссоциации его оксида будет больше парциального давления кислорода.
Для большинства других металлов процесс окисления кислородом воздуха термодинамически разрешен до и выше температур их плавления.
Особые (частные) случаи газовой коррозии: в общем случае кроме процессов окисления металлов и сплавов кислородом воздуха, наибольшую агрессивность проявляют галогены (хлор, бром), реакции которых протекают с образованием солей, атмосферные соединения серы (SO2, SO3), но наибольший практический интерес относится к коррозии сталей, которые до настоящего времени являются основным конструкционным материалом.
В
общем виде, сталь – это сплавы железа
с углеродом с добавками легирующих
компонентов (Cr, Ni, Mo, W, V, B, Si и т.д.).
Наибольшую твердость, прочность обычной
углеродистой стали придаёт сплав типа
«химическое соединение»
 – цементит. При взаимодействии компонентов
стали с воздушной средой могут протекать
различные реакции, направление которых
может изменяться в зависимости от
соотношения компонентов в газовой
смеси.
– цементит. При взаимодействии компонентов
стали с воздушной средой могут протекать
различные реакции, направление которых
может изменяться в зависимости от
соотношения компонентов в газовой
смеси.
В присутствие в воздухе CO и CO2:
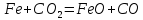

Такая реакция называется реакцией-процессом обезуглероживания сталей, который вызывает уменьшение твердости и прочности конструкционного материала.

И наоборот, при наличии в атмосфере CO будет идти процесс науглероживания, который, кроме повышения твердости стали, будет вызывать уменьшение пластичности и повышение хрупкости.
Особо выделяют так называемую карбонильную коррозию.
 – пентакарбонил
железа, который является жидкостью при
комнатой температуре. Реакция используется
для получения очень мелких порошков
Fe, Ni. Пентакарбонил возгоняют в газовую
фазу, он разлагается и начинают выпадать
очень мелкодисперсные частицы металла.
– пентакарбонил
железа, который является жидкостью при
комнатой температуре. Реакция используется
для получения очень мелких порошков
Fe, Ni. Пентакарбонил возгоняют в газовую
фазу, он разлагается и начинают выпадать
очень мелкодисперсные частицы металла.
При высокой температуре вода является газом.

Отдельно выделяют процесс коррозии металлов в среде водорода, который условно называется «водородной хрупкостью». Это обусловлено несколькими видами взаимодействий:
При
высоких температурах молекула водорода
каталитически распадается на атомы,
имеющие самый маленький возможный
размер,
 нм, и потому способны легко проникать
вглубь металла через междоузельные
пространства кристаллической решетки
или по каким-либо дефектам и вступать
в различные реакции внутри металла.
Основной вид дефектов в металлах – это
вакансии, незанятые узлы.
нм, и потому способны легко проникать
вглубь металла через междоузельные
пространства кристаллической решетки
или по каким-либо дефектам и вступать
в различные реакции внутри металла.
Основной вид дефектов в металлах – это
вакансии, незанятые узлы.