
- •Содержание
- •Введение
- •Классификация химических превращений в окружающей среде Все химические превращения загрязняющих веществ в окружающей среде можно разделить на:
- •1.2 Миграция химических элементов в окружающей среде
- •Перенос почва – вода
- •Лекция № 2 ФизиКо-химические процессы в атмосфере
- •2.1 Пыли и аэрозоли
- •2.1.1 Химический состав аэрозолей
- •2.1.2 Сток аэрозолей в тропосфере
- •2.3 Газы в атмосфере
- •2.3 Химические превращения в атмосферном воздухе
- •Состав облачных и дождевых капель. Химические процессы в жидкой фазе
- •2.4 Фотохимические реакции в нижних слоях атмосферы
- •Фотохимические реакции оксидов азота (фотохимический смог)
- •Другие химические реакции оксидов азота
- •Химические реакции соединений серы. Кислотные дожди
- •Влияние кислотных дождей на природные объекты, здания, памятники и технику
- •Окисление монооксида углерода
- •Химия парникового эффекта
- •2.5 Атмосферная химия органических веществ Окисление метана и его гомологов
- •Хлорорганические соединения. Пестициды
- •2.6 Фотохимические реакции в верхних слоях атмосферы
- •Лекция № 3 Физико-химические процессы в гидросфере
- •3.1. Сведения о свойствах воды и её загрязнении
- •Вторичное загрязнение
- •3.2 Физико-химические превращения металлов в гидросфере
- •Превращения металлов при участии микроорганизмов
- •3.5 Эвтрофирование водоемов
- •Трофический статус водного объекта
- •Эвтрофирование и сукцессия
- •Стадии эвтрофирования
- •Хозяйственные последствия эвтрофирования
- •Борьба с эвтрофированием
- •Формы нефтяных загрязнений
- •Последствия загрязнения морей и океанов нефтью
- •3.7.2 Поверхностно-активные вещества
- •3.7.3 Пестициды
- •Лекция № 4 Физико-химические процессы в литосфере и почвенном покрове
- •4.1 Поведение тяжелых металлов и их соединений в почвах
- •4.2 Поведение пестицидов в почвах
- •4.3 Загрязнение почв нефтью
- •4.4 Процессы биологического разложения твердых бытовых отходов
- •Лекция № 5 физико-химические превращения в окружающей среде суперэкотоксикатов
- •5.1 Стойкие органические загрязнители
- •5.2 Полихлорированые бифенилы
- •Полиароматические углеводороды (пау)
- •5.4 Дихлордифенилтрихлорэтан (ддт)
- •Лекция № 6 Радиоактивные вещества в окружающей среде
- •6.1 Взаимодействие ионизирующего излучения с компонентами атмосферы
- •Радиационно-химические превращения вещества под действием радиоактивных излучений
- •6.2 Искусственные радионуклиды в морских экосистемах
- •Радиолиз воды
- •6.3 Поведение радионуклидов в почвах
- •6.4 Поступление радионуклидов в растения
- •Лекция № 7 биохимические процессы трансформации загрязняющих веществ в окружающей среде
- •Процессы, протекающие при нарушении экологического равновесия в круговороте биогенных элементов
- •Список литературы Основная
- •Дополнительная
- •Физико-химические превращения загрязняющих веществ в окружающей среде конспект лекций
4.1 Поведение тяжелых металлов и их соединений в почвах
Наиболее типичными тяжелыми металлами, представляющими опасность являются: свинец, кадмий, ртуть, хром, цинк, молибден, никель, кобальт, олово, титан, медь, ванадий. Пути поступления их в почву связаны с выбросами промпредприятий и последующим осаждением их на почву преимущественно в виде оксидов или солей. Последние постепенно растворяются, переходя в гидроксиды, карбонаты или в форму обменных катионов.
На рисунке 4.1 представлена схема трансформации и миграции тяжелых металлов в почвах.
Если тяжелые металлы при этих взаимодействиях образуют в почве прочные нерастворимые соединения (обычно в тяжелосуглинистых и глинистых почвах), то это предотвращает загрязнение грунтовых и питьевых вод. Но в таком случае почва все больше накапливает загрязняющие вещества и при превышении ее емкости по данным элементам может произойти выброс тяжелых металлов в почвенный раствор.
Кислотные дожди снижают рН почв, увеличивают их кислотность и тем самым способствуют повышению содержания в почвах растворимых соединений токсичных металлов – свинца, алюминия, усилению разложения почвенных соединений.
Атмосфера
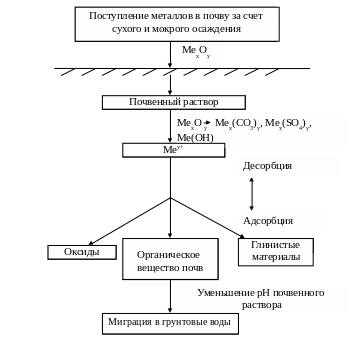
Рисунок 4.1 – Трансформация и миграция соединений тяжелых металлов в почвах
Низкие значения рН способствуют присоединению анионов к железосодержащим коллоидным частицам в почве, так как протоны сообщают комплексам положительный заряд.
Для процессов, протекающих в почвах при контакте с почвенным раствором, весьма характерна реакция ионного обмена, в результате которой происходит фиксация твердыми частицами почвы растворенных катионов водорода, тяжелых металлов, анионов кислотных остатков (рисунок 4.2).
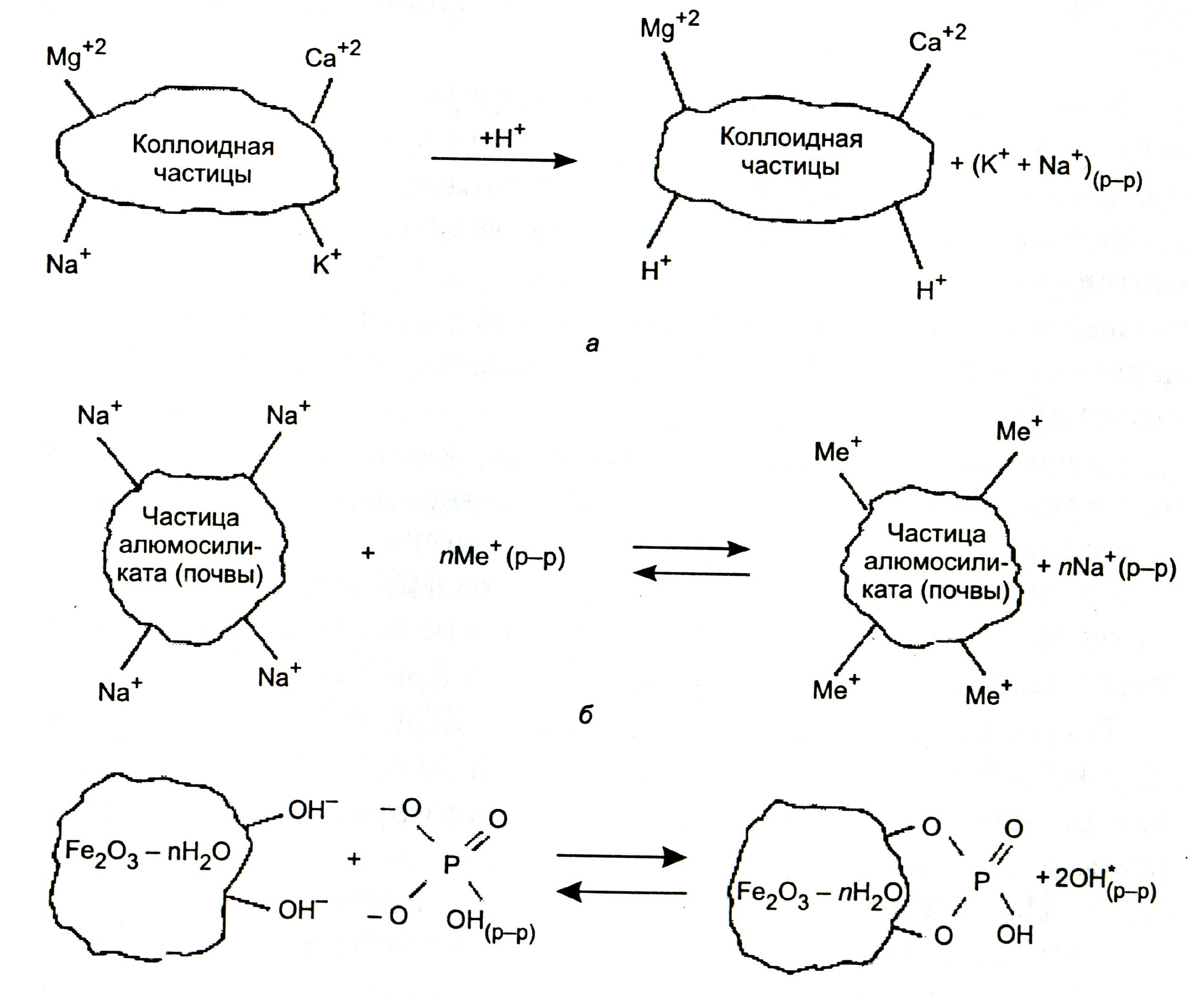
а) катионы, адсорбированные на коллоидных частицах почвы, вытесняются избытком ионов водорода;
б) катионы тяжелых металлов сорбируются на минеральных частицах почвы, вытесняя в почвенный раствор катионы натрия;
в) связывание фосфат-ионов железосодержащими коллоидными частицами почвы.
Рисунок 4.2 – Ионный обмен на коллоидных частицах почвы
Можно значительно снизить последствия этого процесса при повышении рН почвенного раствора известкованием почв или внесением большого количества таких органических удобрений, как торф.
Так, попадающие в почву протоны замещают катионы (например, К+, Na+), сорбционно-связанные с коллоидными частицами почвы, которые мигрируют в глубинные слои (рис. 4.2 а).
Катионы тяжелых металлов селективно сорбируются на алюмосиликатных и других минеральных частицах, вытесняя в почвенный раствор катионы натрия, калия, кальция (рис. 4.2 б). У фосфатов возможен обмен их кислотных остатков с ОН-группами на поверхности коллоидных частиц, при этом фосфатные остатки связываются, и дальнейшее усвоение фосфора растениями становится невозможным (рис. 4.2 в).
Для свинца характерно стремление к накоплению в почве вследствие образования ионов малорастворимых соединений, адсорбции на глинистых частицах почв. Подвижность его ионов мала даже при низких значениях рН.
Количество кадмия, поступающего в почвы, оценивается гораздо меньшими значениями по сравнению с массой свинца и его соединений. В кислых почвах со значением рН<6 наблюдается растворение соединений кадмия, ионы которого весьма подвижны и мигрируют в составе почвенного раствора. При значениях рН>6 кадмий аккумулируется в почвах вместе с гидроксидом железа, марганца и алюминия в основном в виде оксида, гидроксида, карбоната.
Соединения кадмия с гуминовыми кислотами значительно менее устойчивы, чем аналогичные соединения свинца. В условиях повышенных значений рН кадмий в почве может присутствовать в виде сульфида кадмия СdS, который образуется из сульфатов при наличии восстановительной среды. Образование карбоната кадмия CdCO3 возможно только при рН>8.
Подвижность ионов двухвалентной меди очень велика. Она легко переходит из породы в почву, а оттуда в почвенный раствор и поверхностные воды. Надо отметить, что растворимость соединений меди значительно увеличивается при значении рН<5. Подвижности меди препятствует наличие в почве сульфид-ионов, с которыми она образует нерастворимый сульфид CuS. В восстановительных условиях подвижность меди резко падает, так как соединения одновалентной меди практически нерастворимы.
Своей высокой подвижностью при рН<6 цинк обязан хорошей растворимости своих минеральных солей и органических соединений. При более высоких значениях рН, и особенно в присутствии фосфатов, подвижность цинка ввиду образования трудно растворимых соединений сильно снижается. Накоплению цинка в почве способствуют процессы адсорбции в глинах и различных оксидных минералах, определяемые значениями рН. Из лесных гумусовых почв цинк быстро вымывается благодаря постоянному естественному поддержанию кислой среды.
Сера, находящаяся в почвах в виде сульфата, может восстанавливаться микробиологическим путем до сульфид-ионов и образовывать с тяжелыми металлами (медь, кадмий, свинец, кобальт и др.) трудно растворимые сульфиды.
Марганец обычно встречается в почве в виде пиролюзита MnO2. При восстановлении он переходит в растворимый ион марганец (+2). Органические соединения (комплексы) марганца неустойчивы и легко обменивают ионы Mn+2 на другие катионы, входящие в состав нерастворимых соединений. Похожее положение складывается и с соединениями железа. В обычных условиях железо накапливается в почве в виде Fe(OH)3. При малом содержании кислорода в восстановительных условиях понижается окислительно-восстановительный потенциал почвы, что способствует переводу Fe(III) в Fe(II).
Fe(OH)3 + 3H+ + e → Fe2+ + 3H2O.
Ионы железа, марганца и ряда других металлов в восстановленной форме обладают повышенной подвижностью в почве, что способствует их переходу в раствор и обеднению почвы этими металлами.
На поверхность почвы ТМ поступают в различных формах. то оксиды и различные соли металлов, как растворимые, так и практически нерастворимые в воде (сульфиды, сульфаты, арсениты и др.). В составе выбросов предприятий по переработке руды и предприятий цветной металлургии - основного источника загрязнения окружающей среды ТМ - основная масса металлов (70-90 %) находится в форме оксидов.
Попадая на поверхность почв, ТМ могут либо накапливаться, либо рассеиваться в зависимости от характера геохимических барьеров, свойственных данной территории. Большая часть ТМ, поступивших на поверхность почвы, закрепляется в верхних гумусовых горизонтах. ТМ сорбируются на поверхности почвенных частиц, связываются с органическим веществом почвы, в частности в виде элементно-органических соединений, аккумулируются в гидроксидах железа, входят в состав кристаллических решеток глинистых минералов, дают собственные минералы в результате изоморфного замещения, находятся в растворимом состоянии в почвенной влаге и газообразном состоянии в почвенном воздухе, являются составной частью почвенной биоты.
Степень подвижности ТМ зависит от геохимической обстановки и уровня техногенного воздействия. Тяжелый гранулометрический состав и высокое содержание органического вещества приводят к связыванию ТМ почвой. Рост значений рН усиливает сорбированность катионообразующих металлов (медь, цинк, никель, ртуть, свинец и др.) и увеличивает подвижность анионообразующих (молибден, хром, ванадий и пр.). Усиление окислительных условий увеличивает миграционную способность металлов. В итоге по способности связывать большинство ТМ, почвы образуют следующий ряд: серозем > чернозем > дерново-подзолистая почва.
Загрязнение почв ТМ имеет сразу две отрицательные стороны. Во-первых, поступая по пищевым цепям из почвы в растения, а оттуда в организм животных и человека, ТМ вызывают у них серьезные заболевания. Росту заболеваемости населения и сокращению продолжительности жизни, а также к снижению количества и качества урожаев сельскохозяйственных растений и животноводческой продукции.
Во-вторых, накапливаясь в почве в больших количествах, ТМ способны изменять многие ее свойства. Прежде всего, изменения затрагивают биологические свойства почвы: снижается общая численность микроорганизмов, сужается их видовой состав (разнообразие), изменяется структура микробоценозов, падает интенсивность основных микробиологических процессов и активность почвенных ферментов и т.д. Сильное загрязнение ТМ приводит к изменению и более консервативных признаков почвы, таких как гумусное состояние, структура, pH среды и др. Результатом этого является частичная, а в ряде случаев и полная утрата почвенного плодородия.
В природе встречаются территории с недостаточным или избыточным содержанием в почвах ТМ. Аномальное содержание ТМ в почвах обусловлено двумя группами причин: биогеохимическими особенностями экосистем и влиянием техногенных потоков вещества. В первом случае, районы, где концентрация химических элементов выше или ниже оптимального для живых организмов уровня, называются природными геохимическими аномалиями или биогеохимическими провинциями. Здесь аномальное содержание элементов обусловлено естественными причинами – особенностями почвообразующих пород, почвообразовательного процесса, присутствием рудных аномалий. Во втором случае, территории называются техногенными геохимическими аномалиями. В зависимости от масштаба они делятся на глобальные, региональные и локальные.
Почва, в отличие от других компонентов природной среды, не только геохимически аккумулирует компоненты загрязнений, но и выступает как природный буфер, контролирующий перенос химических элементов и соединений в атмосферу, гидросферу и живое вещество.
Различные растения, животные и человек требуют для жизнедеятельности определенного состава почвы, воды. В местах геохимических аномалий происходит, усугубляясь, передача отклонений от нормы минерального состава по всей пищевой цепи. В результате нарушения минерального питания наблюдаются изменения видового состава фито-, зоо- и микробиоценозов, заболевание дикорастущих форм растений, снижение количества и качества урожаев сельскохозяйственных растений и животноводческой продукции, рост заболеваемости населения и снижение продолжительности жизни
По вопросу санации почв, загрязненных ТМ, существует два основных подхода. Первый направлен на очищение почвы от ТМ. Очищение может производиться путем промывок, путем извлечения ТМ из почвы с помощью растений, путем удаления верхнего загрязненного слоя почвы и т.п. Второй подход основан на закреплении ТМ в почве, переводе их в нерастворимые в воде и недоступные живым организмам формы. Для этого предлагается внесение в почву органического вещества, фосфорных минеральных удобрений, ионообменных смол, природных цеолитов, бурого угля, известкование почвы и т.д. Однако любой способ закрепления ТМ в почве имеет свой срок действия. Рано или поздно часть ТМ снова начнет поступать в почвенный раствор, а оттуда в живые организмы.
Экологические последствия загрязнения почв ТМ зависят от параметров загрязнения, геохимической обстановки и устойчивости почв. К параметрам загрязнения относятся природа металла, т.е. его химические и токсические свойства, содержание металла в почве, форма химического соединения, срок от момента загрязнения и т.д. Устойчивость почв к загрязнению зависит от гранулометрического состава, содержания органического вещества, кислотно-щелочных и окислительно-восстановительных условий, активности микробиологических и биохимических процессов и т.д.
