
- •Національний університет харчових технологій
- •В.М. Поводзинський
- •Основи проектування
- •Фармацевтичних виробництв
- •Курс лекцій
- •1. Загальні принципи проектування
- •Організаційні форми та методи проектування.
- •2. Виробництво лікарських засобів
- •3. Належна виробнича практика (gmp)
- •3.1. Національні правила gmp.
- •3.2.4. Контроль якості.
- •4. Використання Чистих Приміщень у технологіях виробництва лікарських засобів
- •5. Проектування систем підготовки води для фармації
- •1. Загальні принципи проектування
- •Організаційні форми та методи проектування
- •Ситуація, що склалася
- •1.3. Стратегія проектування
- •1.4. Стадії процесу проектування
- •2. Виробництво лікарських засобів
- •2.1 Законодавча та нормативна база виробництва лікарських засобів.
- •2.2 Реєєстраційне досьє
- •2.2.1. Аналітичний нормативний документ на лікарський засіб. Порядок побудови, викладу та оформлення
- •Склад лікарського засобу. Якісні характеристики.
- •Фізико-хімічні властивості, що впливають на біодоступність
- •2.2.1.1. Порядок побудови, викладу і оформлення анд на лікарський засіб
- •2.2.1.2. Характеристики якості, які мають бути наведені у специфікації
- •2.2.1.2. Приклад специфікації на рідкий стерильний лікарський засіб для ін’єкцій
- •2.2.2. Аналітична нормативна документація медичних імунобіологічних препаратів
- •Основні положення розробки анд
- •2.2.1.1. Побудова найменування мібп
- •Структура найменувань
- •2.2.1.2. Побудова і зміст розділів анд
- •2.2.2.4. Приклад специфікації на мібп. Специфікація
- •2.2.2.5. Вимоги до оформлення розділу “методи контролю”
- •Фармакологічна дія лікарського засобу
- •2.2.2.6. Інструкція про застосування мібп.
- •2. Загальна характеристика:
- •3. Склад:
- •5. Код анатомічно-терапевтично-хімічної класифікації "Anatomical Therapeutic Chemical classification system /who" (atc).
- •8. Спосіб застосування і дози.
- •Інформація, що наноситься на упаковку (етикетку) мібп, що вводяться людині
- •Інформація про мібп, що застосовуються in vitro
- •Інформація, що наноситься на упаковку (етикетку) мібп, що використовуються in vitro
- •2.2.3. Типи регламентів виробництва, склад регламентів виробництва лікарських засобів
- •Контроль виробництва
- •Лінія зв’язку означає факт прийняття рішення!
- •Безпечна експлуатація виробництва та охорона навколишнього середовища
- •2.2.4. Регламенти виробництва імунобіологічних препаратів медичного призначення
- •Біологічна схема виробництва
- •Наступні розділи регламенту ідентичні технічному та технологічному регламентам виробництва лз. Технологічна схема виробництва
- •Апаратурно–технологічна схема виробництва і специфікація обладнання.
- •Викладення технологічного процесу
- •Матеріальний баланс
- •3. Належна виробнича практика (gmp)
- •3.1. Історія виникнення та базові принципи gmp
- •Національні правила gmp
- •3.2. Належна виробнича практика (gmp).
- •3.2.1. Загальні вимоги належної виробничої практики (нвп)
- •3.2.2. Управління якістю
- •3.2.3. Належна виробнича практика лікарських засобів (gmp)
- •3.2.4. Контроль якості
- •3.2.5 Персонал
- •3.2.6. Приміщення та обладнання
- •Загальні вимоги стосовно проектування та експлуатації виробничих зон можна представити в наступному вигляді:
- •3.2.7. Документація
- •3.2.8. Технологічний процес
- •Загальні вимоги до технологічного процесу. Всі стадії та операції повинні здійснювати і контролювати компетентні особи.
- •Валідація. Дослідження з валідації мають сприяти реалізації нвп; їх слід проводити відповідно до встановлених методик. Результати і висновки повинні бути запротокольовані.
- •3.2.9. Контроль якості
- •Проведення випробувань. Аналітичні методи повинні пройти валідацію.
- •4. Використання Чистих Приміщень у технологіях виробництва лікарських засобів
- •Глосарій
- •4.1. Загальні принципи створення та застосування чистих приміщень
- •4.2. Класифікація чистих приміщень
- •4.2.1. Вимоги правил gмр в проектуванні чистих приміщень виробництв лікарських засобів
- •4.2.2. Чисті приміщення у виробництві стерильних лікарських засобів
- •4.2.3. Загальні вимоги до проектування виробництва стерильних лікарських засобів
- •4.4.1. Ізолюючі технології виробництва стерильних лікарських засобів
- •4.4.2. Чисті приміщення у виробництві стерильних лікарських засобів, які підлягають фінішній стерилізації у первинній упаковці
- •4.4.3. Чисті приміщення у виробництва стерильних лікарських засобів у асептичних умовах
- •4.4.4. Технологія видування-наповнення-герметизація
- •4.4.5. Проектні вимоги до приміщень у виробництві стерильних лікарських засобів
- •4.4.6. Персонал у чистих зонах (приміщеннях) виробництва стерильних лікарських засобів
- •4.4.7. Обладнання у чистих зонах (приміщеннях) виробництва стерильних лікарських засобів
- •3.5. Чисті приміщення у виробництві нестерильних лікарських засобів
- •3.5.1. Класифікація виробничих приміщень виробництва нестерильних лікарських засобів.
- •4.5.2. Підготовка вентиляційного повітря для виробничих приміщень виробництва нестерильних лікарських засобів
- •4.6. Проектування чистих приміщень. Методи забезпечення чистоти.
- •4.6.1. Потоки повітря
- •4.6.2. Швидкість однонаправленого потоку повітря
- •4.6.3. Баланс повітрообміну.
- •3.6.4. Кратність повітрообміну.
- •4.6.5. Перепад тиску.
- •4.6.5. Конструктивні і планувальні рішення чистих приміщень виробництва лікарських засобів.
- •4.6.5.1. Планувальні рішення чистих приміщень
- •4.6.5.2. Кімнати перевдягання. Приміщення підготовки персоналу
- •4.6.5.3. Конструктивні рішення будівельних елементів чистих приміщень.
- •4.6.7. Будівництво чистих приміщень.
- •4.6.5. Атестація чистих приміщень.
- •Етапи атестації Етапи створення Статус чистого приміщення
- •4.7. Підготовка стерильного вентиляційного повітря для чистих приміщень. Глосарій
- •4.7.1. Функції стерильного вентиляційного повітря
- •4.7.2 Способи стерилізації повітряних аерозолів
- •3.4.2.1. Ефект фільтрації
- •3.4.2.2. Механізм фільтрації частинок
- •4.7.2. Типи фільтрів
- •4.7.4. Схеми очистки повітря у виробництві лікарських засобів.
- •5. Проектування систем підготовки води для фармації
- •5.1. Цільове призначення води різних типів
- •5.2. Способи та технологічні схеми отримання води фармакопейної якості
- •5.2.1. Узагальнена технологічна схема очистки води
- •Підготовка виробництва
- •5.2.2. Вихідний контроль води питної
- •5.2.2 Пом’якшення води
- •5.2.3. Знесолювання води
- •5.3. Отримання води очищеної та води для ін’єкцій
- •5.4.1 Використання дистиляції для одержання води очищеної та води для ін’єкцій
- •5.5. Пірогенні речовини у фармації
- •Основи проектування конспект лекцій
4.4.1. Ізолюючі технології виробництва стерильних лікарських засобів
Вирішення проблем пов’язаних з присутністю персоналу дозволяють ізолюючі технології. Основним джерелом контамінації у виробничому приміщенні є персонал. Доцільно розглянути можливі джерела забруднення повітря чистих приміщень контамінантами різної походження.
Джерела мікрозабруднень. Оточуюче нас повітря містить велику кількість як живих (життєздатних), так і неживих частинок, що відрізняються по своїй природі і розмірам.
Мікрозабруднення виділяються персоналом, огороджуючими конструкціями, обладнанням, надходять у чисте приміщення з оточуючого простору. В чистому приміщенні 70-80 % присутніх мікрозабруднень приходиться на людину, 15-20% - на обладнання, 5-10% - на навколишнє середовище (рис. 4.1.)
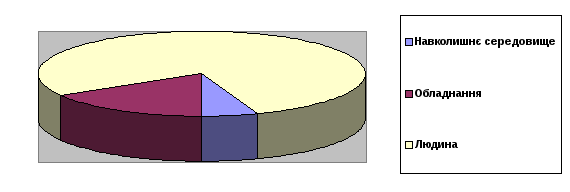
Рис. 4.1. Джерела мікрозабруднень.
З аналізу природи мікрозабруднень у повітрі і характерних для них розмірів видно, що проблема чистих приміщень носить комплексний характер. Недостатньо створити власно чисте приміщення, що забезпечує потрібний клас чистоти за відсутності технологічного устаткування і персоналу. Потрібно одночасно застосовувати устаткування, що виділяє мінімум забруднень або не виділяє їх узагалі, одягти людей у одяг, що не пропускає частинки, які виділяє людина під час фізичної активності та ін.
Остаточно з’ясовано, що основним джерелом забруднень у чистому приміщенні є людина. Це пояснюється структурою шкіри людини і динамікою її зміни. Зовнішній покрив шкіри людини має безлічі пластинок (лусочок) розміром приблизно в одиниці і десятки мікрометрів. Вони постійно відокремлюються з поверхні шкіри таким чином, що кожні кілька днів зовнішній шкірний покров цілком оновлюється. Відокремившись, вони розділяються на більше дрібні частки. У спокійному, нерухомому стані людина виділяє у хвилину приблизно 200 тис. часток розміром 0,5 мкм і більше. Навіть невеликі рухи і тертя тіла об одяг приводять до різкого збільшення викиду частинок до декількох мільйонів у хвилину. При інтенсивному русі людина виділяє приблизно 10 млн. частинок у хвилину. У середньому людина виділяє близько 3,5 кг частинок за рік або 10 г у день.
При русі в чистих приміщеннях люди в халатах і лабораторному одязі виділяють у навколишнє середовище в середньому:
два мільйони частинок розміром 0,5 мкм і більше,
триста тисяч частинок розміром 5 мкм і більше,
160 частинок, але з мікроорганізмами.
Джерелами інтенсивного виділення часток є ніс і рот людини. Інтенсивність виділення різко зростає при розмові, особливо під час голосної мови і лементу. Частинки, відділившись від людини, підхоплюються постійним природним конвекційним потоком повітря, що рухається нагору і весь час оточує людину. Далі вони поширюються по всьому об’єму приміщення й осідають на устаткуванні, матеріалах, продукті, огороджуючих конструкціях, інших працівниках і т.д. При цьому частинки можуть бути носіями мікроорганізмів.
Відповідно до статистики на 1000 зважених часток приходиться орієнтовно один мікроорганізм. У стандарті Національного агенції по дослідженню космосу США (NАSА) NНВ 5340 наводиться зразкове співвідношення між числом частинок і мікроорганізмів у повітрі (табл. 4.7.). Звичайно, з-за множинності факторів, що впливають на мікробне забруднення, ці дані носять наближений, ймовірний характер, але проте дають уявлення про взаємозв’язок між цими ключовими параметрами. Націленість одержати хоча б орієнтований зв’язок між числом частинок і числом мікроорганізмів у повітрі було викликано практичними розуміннями. Рахування частинок у повітрі проводиться швидко і легко. Це зручно при атестації чистих приміщень і поточному контролі. Аналіз же мікробного забруднення вимагає часу і затрат.
Таблиця 4.7. Зв’язок між числом частинок і числом мікроорганізмів у повітрі по стандарту NАSА NНВ 5340
|
Клас чистого приміщення по стандарту США 209 D |
Частинки |
Бактерії |
||
|
Діаметр, мкм |
Кількість, 1куб. фут (л) |
Зважені, 1куб. фут (л) |
Осаджені, 1кв. фут/нед. (1кв м/нед.). |
|
|
100 |
>0,5 |
<100 (<0,35) |
<0,1 (<0,0035) |
1200 (12900) |
|
10000 |
>0,5 |
<10000 (<350) |
<0.5 (<0.0176)
|
6000 (64600) |
|
>5,0 |
<65 (<2,3) |
|||
|
100000 |
>5,0 |
<100000 (<3500) |
<2.5 (<0.0884) |
30000 (323000) |
|
>0,5 |
<700 (<25) |
|||
Серйозним кроком вперед у забезпеченні стерильності продукту, підвищенні ефективності чистих приміщень і чистих зон і зниженні пов’язаних з ними витрат є застосування ізолюючої технології і технології видування-наповнення-герметизація.
Суть ізолюючої або бар’єрної технології полягає у фізичній ізоляції робочої зони від навколишнього простору за рахунок застосування герметичного ізолятора. Ця технологія широко впроваджується у виробництві стерильних препаратів. Правилами GМР ЄС з 1997р. установлено, що для випадку асептичного виробництва простір, що оточує ізолятор, повинен відповідати принаймні зоні D. Це істотно більше проста умова, ніж вимоги до чистоти в звичайній технології чистих приміщень. Воно дозволяє значно знизити витрати на будівництво і експлуатацію чистих приміщень.
Використання ізолюючої технології знімає необхідність присутності людини у виробничих зонах, у результаті чого значно знижується ризик контамінації продукції, виробленої в асептичних умовах, із навколишнього середовища. Існує багато типів ізоляторів і передавальних пристроїв. Ізолятор і оточуюче його середовище мають бути сконструйовані таким чином, щоб у відповідній зоні забезпечувалася необхідна якість повітря. Конструкції передавальних пристроїв можуть варіювати від пристроїв з одинарними або подвійними дверима до повністю герметизованих систем, включаючи стерилізацію.
Передача матеріалів усередину і назовні пристрою є одним із найсерйозніших потенційних джерел контамінації. Звичайно простір усередині ізолятора є обмеженою зоною для ведення операцій, що потребують мінімального ризику контамінації або його відсутності, хоча визнано, що в робочій зоні всіх таких пристроїв може бути відсутній ламінарний потік повітря. Чистоту цього простору необхідно контролювати; виробництво в асептичних умовах потребує принаймні клас чистоти D.
Експлуатація ізоляторів може бути почата тільки після проведення відповідної валідації. Валідація повинна враховувати всі критичні фактори ізолюючої технології, наприклад, якість повітря усередині та зовні (навколишнього простору) ізолятора, санітарну обробку ізолятора, процеси передачі та цілісність ізолятора. Необхідно постійно проводити контроль, який включає часті випробування герметичності ізолятора і його вузлів.
