
- •Глава 1. Методология биологии и биофизики
- •1.1. Предмет и основные задачи курса истории науки
- •1.2. Наука, научная методология. Методология и проблемы в биологии и биофизике
- •1.3. О научном методе в общем
- •1.4. О научной методологии чуть более строго
- •1.5. Что такое научное знание и как оно развивается
- •1.6. Методология об этапах развития научного знания
- •1.7. Эвристика индивидуального научного поиска
- •1.8. Определение, методология и проблемы биологии
- •1.9. Основные проблемы современной биологии
- •1.10. Определение, методология и проблемы биофизики
- •Глава 2. От протознания к естественной истории (от первобытного общества к эпохе Возрождения)
- •2.1. У истоков биологического знания
- •2.2. Культурный переворот в античной Греции: от мифа к логосу, от теогонии к возникновению природы
- •2.3. Эллинизм как синтез восточной и древнегреческой науки
- •2.4. Отношение к образованию и к науке в средневековье
- •2.5. Эпоха Возрождения и революция в идеологии и естествознании
- •2.5.1. Изобретение книгопечатания
- •2.5.2. Развитие науки в период становления капитализма
- •2.5.3. Новые организационные и материальные возможности раз-вития науки
- •2.5.3.1. Организация Академий наук
- •2.5.3.2. Открытие обсерваторий
- •2.5.3.3. Открытие ботанических садов
- •2.5.3.4. Организация музеев
- •2.5.3.5. Публикация трудов Академий
- •2.5.3.6. Создание библиотек
- •2.5.3.7. Изобретение приборов
- •2.5.3.8. Путешествия
- •2.5.4. Разработка новых принципов познания
- •2.5.5. Развитие принципов естественнонаучного познания природы в трудах Бэкона, Галилея и Декарта
- •2.5.6. Лейбниц и идея «лестницы существ»
- •2.5.6. И. Ньютон
- •2.5.7. Французский материализм XVIII века
- •2.6. Создание Российской Академии наук
- •2.6.1 Исторические условия создания ран
- •2.6.2. Первые учреждения ран
- •2.6.3. Социо-культурные условия формирования науки в России
- •Глава 3. От естественной истории к современной биологии (биология нового времени до середины XIX в.)
- •3.1. Развитие ботанических исследований
- •3.1.1. Попытки классификации растений в XVI веке
- •3.1. 2. Систематика и морфология растений в XVII веке
- •3.1.3. Развитие микроскопической анатомии растений в XVII веке
- •3.1.4. Система к. Линнея
- •3.1.5. Попытки создания «естественных» систем в XVIII веке
- •3.1.6. Зарождение физиологии растений
- •3.1.7. Развитие учения о поле и физиологии размножения растений
- •3.2. Развитие зоологических исследований
- •3.2.1. Описания и попытки классификации животных в XVI – XVII веках
- •3.2.2.Зоологические исследования в XVIII веке
- •3.2.3. Изучение ископаемых организмов
- •3.3. Развитие исследований по анатомии, физиологии, сравнительной анатомии и эмбриологии животных
- •3.3.1. Анатомия животных и человека в XVI – XVII веках
- •3.3.2. В. Гарвей и становление физиологии
- •3.3.3. Микроскопическая анатомия и изучение простейших
- •3.3.4. Физиология в XVIII веке
- •3.3.5. Становление сравнительной анатомии
- •3.3.6.Эмбриология животных. Преформизм и эпигенез
- •3.4. Господство метафизического мировоззрения в естествознании XVII – XVIII веков
- •3.4.1. Достижения биологии XVII – XVIII веков
- •3.4.2. Господство метафизического мышления
- •3.4.3. Концепция постоянства видов и преформизм
- •3.4.4. Идеалистическая трактовка органической целесообразности
- •3.5. Возникновение и развитие представлений об изменяемости живой природы
- •3.5.1. Допущение ограниченной изменчивости видов
- •3.5.2.Представление о "естественном сродстве" и "общих родоначальниках".
- •3.5.3. Фактор времени в изменении организмов.
- •3.5.4. Последовательность природных тел. "Лестница существ".
- •3.5.5. Идея «прототипа» и единства плана строения организмов
- •3.5.6. Идея трансформации органических форм
- •3.5.7. Идея самозарождения и ее отношение трансформизму
- •3.5.8. Естественное возникновение органической целесообразности
- •3.6. Первая попытка создания концепции эволюции органического мира (Ламарк и его учение)
- •3.6.1. Ламарк. Краткие биографические сведения
- •3.6.2. Философские воззрения Ламарка
- •3.6.3. Сущность жизни по Ламарку
- •3.6.4. Представления Ламарка о происхождении жизни
- •3.6.5. Развитие от простого к сложному и градация форм по Ламарку
- •3.6.6. Отрицание реальности видов
- •3.6.7. Причины развития живой природы по Ламарку
- •3.7. Основные черты учения ч. Дарвина
- •3.7.1. Зарождение эволюционной идеи ч. Дарвина
- •3.7.2. Содержание теории эволюции ч. Дарвина
- •3.8. Создание и развитие эволюционной палеонтологии
- •3.8.1. Роль теории ч. Дарвина в перестройке палеонтологии
- •3.8.2. В. О. Ковалевский и создание эволюционной палеонтологии
- •3.8.3. Попытки ламаркистского истолкования данных палеонтологии
- •3.8.4. Развитие палеонтологического метода в трудах л. Долло
- •3.8.5. Обнаружение новых ископаемых форм
- •3.9. Создание эволюционной эмбриологии животных
- •3.9.1. Сравнительное изучение эмбрионального развития
- •3.9.2. Создание а. О. Ковалевским и и. И. Мечниковым эволюционной эмбриологии
- •3.9.3. Подтверждение гомологии зародышевых листков позвоночных и беспозвоночных
- •3.9.4. Проблемы происхождения многоклеточных организмов
- •3.10. Перестройка сравнительной анатомии на основе Дарвинизма
- •3.10.1. Возникновение филогенетического направления
- •3.10.2. Учение о гомологии
- •3.10.4. Новая трактовка зоологических типов
- •3.10.5. Кризис филогенетического направления в морфологии
- •3.11. Развитие филогенетической систематики животных
- •3.11.1. Представления ч. Дарвина и э. Геккеля о принципах
- •3.11.2. Эмбриологическое направление в систематике
- •3.11.3. Пересмотр основных типов в систематике животных
- •3.12. Развитие физиологии животных и человека
- •3.12.1. Общая характеристика развития физиологии XIX веке
- •3.12.2. Новые физиологические методы
- •3.12.3. Организация первых физиологических лабораторий и
- •3.12.4. Развитие физиологии в отдельных странах
- •3.12.5. Достижение физиологии в XIX столетии
- •3.13. Развитие эмбриологии растении
- •3.13.1. Ч. Дарвин и раскрытие значения перекрестного опыления
- •3.13.2. Изучение зародышевого мешка и пыльцевых зерен. Выяснение э. Страсбургером и и. Н. Горожанкиным механизма оплодотворения
- •3.13.3. Дальнейшие исследования процесса оплодотворения. Работы в. И. Беляева, м. Трейба, с. Г. Навашина и других
- •3.13.4. Открытие с. Г. Навашиным двойного оплодотворения
- •3.14. Начало перестройки морфологии и систематики растений на эволюционной основе
- •3.14.1. Поиски свидетельств филогенетического единства
- •3.14.2. Разработка систематики низших растений
- •3.14.3. Первые попытки создания филогенетических систем в трудах э. Краузе и ю. Сакса
- •3.14.4. Филогенетические системы конца XIX века. Разработка
- •3.14.5. Позднейшие системы растений
- •3.15. Оформление физиологии растений в самостоятельную науку
- •3.15.1. Продукты и схемы процесса фотосинтеза
- •3.15.2. Пигменты растений
- •3.15.3. Фотосинтез и различные факторы среды
- •3.15.4. Почвенное питание растений
- •3.15.5. Азотное питание растений
- •3.15.6. Осмос и передвижение растительных соков
- •3.15.7. Транспирация растений
- •3.15.8. Дыхание и брожение
- •3.15.9. Рост растений
- •3.15.10. Раздражимость и движение растений
- •3.15.11. Экспериментальная морфология растений
- •3.16. Изучение процесса размножения клеток
- •3.16.2. Детальные описания митозов во второй половине 70-х годов
- •3.16.3. Выяснение невозможности «свободного образования» клеток
- •3.17. Эволюционная теория во второй половине XIX века
- •3.17.1. Дарвинизм — единственная подлинно научная теория
- •3.17.2. Борьба за утверждение дарвинизма
- •3.17.3. Неоламаркизм и его разновидности
- •3.17.4. Телеологические концепции эволюции
- •3.17.5. Предтечи мутационной теории эволюции
- •3.17.6. Особенности развития эволюционной теории в России
- •3.17.7. Гипотеза «органического», или «совпадающего», отбора
- •3.17.8. Первые экспериментальные доказательства эффективности естественного отбора
- •Глава 4. Становление и развитие современной биологии (с середины XIX в. До начала XXI в.)
- •4.1. Изучение физико-химических основ жизни
- •4.1.1. Первые попытки создать специфическую физику и химию живого
- •4.1.2. Создание теорий химического строения, жиров, углеводов и белков
- •4.1.3. Появление калориметрии
- •4.1.4. Первые успехи в изучении природы биокаталитических реакций
- •4.1.5. Разработка биохимических основ учения о питании
- •4.1.6. Открытие витаминов и коэнзимов
- •4.1.7. Открытие гормонов
- •4.1.8. Создание новых методов
- •4.1.9. Структура и функции белков
- •4.1.10. Изучение структуры нуклеиновых кислот
- •4.1.11. Биосинтез белка
- •4.1.12. Решение проблемы аэробного дыхания
- •4.1.13. Создание представлений о системе биохимических обменных процессов
- •4.1.144. Исследования в области молекулярной биоэнергетики
- •4.1.15. Попытки реконструировать предбиологическую эволюцию
- •4.2. Микробиология и ее преобразующее воздействие на биологию
- •4.2.1. Открытие микроорганизмов
- •4.2.2. Учения о брожениях, открытие анаэробиоза
- •4.2.3. Опровержение л. Пастером теории самопроизвольного зарождения микроорганизмов
- •4.2.4. Формирование представлений о микробной природе инфекционных заболеваний. Подтверждение л.Пастером микробной теории инфекционных заболеваний
- •4.2.5. Золотой век медицинской микробиологии
- •4.2.6. Фагоциторная концепция и.И. Мечникова
- •4.2.7. Развитие гуморальной теории иммунитета
- •4.2.8. Практическое применение иммунизации и химиотерапии
- •4.2.9. Открытие антибиотиков
- •4.2.10. Разработка методов микробиологических исследований
- •4.2.11. Изучение участия микробов в природных процессах.
- •4.2.12. Открытие хемосинтеза. Создание почвенной и экологической бактериологии
- •4.2.13. Физиология и биохимия микроорганизмов
- •4.2.14. Изучение фотосинтезирующих и азотфиксирующих бактерий
- •4.2.15. Теория биохимического единства жизни
- •4.2.16. Морфология и цитология микроорганизмов
- •4.2.17. Систематика микроорганизмов, построение филогенетического древа
- •4.2.18. Молекулярная палеонтология
- •4.2.19. Практическое использование биосинтетической и трансформирующей деятельности микробов
- •4.2.20. Проблема управляемого культивирования
- •4.2.21. Основные этапы развития генетики микроорганизмов
- •4.2.22. Генетика бактерий
- •4.2.23. Изучение трансформации, трансдукции, конъюгации и лизогенной конверсии
- •4.3. Возникновение и развитие вирусологии
- •4.3. 1.Открытие вирусов
- •4.3.2. Биоразнообразие вирусов
- •4.3.3. Этапы развития вирусологии
- •4.3.4. Развитие концепции о природе вирусов
- •4.3.5. Принципы организации вирусов
- •4.3.6. Вирусы бактерий
- •4.3.7. Вирусы как возбудители заболеваний человека
- •4.3.8. Вирусы и рак
- •4.3.9. Применение вирусов
- •4.3.10. Интерферон
- •4.4. Развитие клеточной теории во второй половине XIX века, начало цитологических исследований, изучение структуры клетки
- •Развитие цитологии в первой половине XX века
- •Хромосомная теория наследственности
- •Новые методы исследований
- •Ультраструктура клетки
- •Проницаемость клеток и модели мембраны
- •Цитология во 1950-1980 гг.
- •Деление клеток и его регуляция
- •Симбиотическая теория
- •Современная клеточная теория
- •4.5. От экспериментальной эмбриологии к генетике эмбриогенеза
- •4.6. Основные направления в физиологии животных и человека
- •4.7. Экология и биосфера
- •4.8. Антропология и эволюция человека
- •Библиографический список
4.1.11. Биосинтез белка
Важный сдвиг в решении проблемы биосинтеза белка связан с успехами в изучении нуклеиновых кислот. В 1941 г. Т. Касперсон (Швеция) и в 1942 г. Ж. Браше (Бельгия) обратили внимание на то, что в тканях с активным белковым синтезом содержится повышенное количество РНК. Они пришли к выводу, что рибонуклеиновые кислоты играют определяющую роль в синтезе белка. В 1953 г. Е. Гейл и Д. Фокс, как будто, получили прямые доказательства непосредственного участия РНК в биосинтезе белка.
В 1954 г. П. Замечник, Д. Литлфилд, Р. Б. Хесин-Лурье и другие обнаружили, что наиболее активное включение аминокислот происходит в богатых РНК фракциях субклеточных частиц — микросомах. П. Замечник и Э. Келлер (1953—1954) обнаружили, что включение аминокислот заметно усиливалось в присутствии надосадочной фракции в условиях регенерации АТФ. П. Сикевиц (1952) и М. Хогланд (1956) выделили из надосадочной жидкости белковую фракцию (рН 5 фракция), которая была ответственной за резкое стимулирование включения аминокислот в микросомах. Наряду с белками в надосадочной жидкости был обнаружен особый класс низкомолекулярных РНК, которые теперь называют транспортными РНК (тРНК). В 1958 г. Хогланд и Замечник, а также П. Берг, Р. Свит и Ф. Аллен и многие другие исследователи обнаружили, что для активации каждой аминокислоты необходим свой особый фермент, АТФ и специфическая тРНК. Стало ясно, что тРНК выполняют исключительно функцию адаптеров, т. е. приспособлений, которые находят на нуклеиновой матрице (иРНК) место соответствующей аминокислоте в формирующейся белковой молекуле. Эти исследования полностью подтвердили адапторную гипотезу Ф. Крика (1957), предусматривавшую существование в клетке полинуклеотидных адапторов, необходимых для правильного расположения аминокислотных остатков синтезирующегося белка на нуклеиновой матрице. Уже много позднее французский ученый Ф. Шапвиль (1962) в лаборатории Ф. Липмана (Нобелевская премия, 1953) в США однозначно показал, что местоположение аминокислоты в синтезирующейся белковой молекуле полностью определяется той специфической тРНК, к которой она присоединена.
К 1958 г. стали известны следующие основные этапы белкового синтеза: 1) активация аминокислоты специфическим ферментом из «рН 5 фракции» в присутствии АТФ с образованием аминоациладенилата; 2) присоединение активированной аминокислоты к специфической тРНК с высвобождением аденозинмонофосфата (АМФ); 3) связывание аминоацил-тРНК (тРНК, нагруженная аминокислотой) с микросомами и включение аминокислот в белок с высвобождением тРНК. Хогланд (1958) отметил, что на последнем этапе белкового синтеза необходим гуанозинтрифосфат (ГТФ).
4.1.12. Решение проблемы аэробного дыхания
Успехи химии жиров, белков и углеводов, разработка новых специальных методов анализа, привлечение методов органической и физической химии для изучения биологических объектов резко усилили интерес исследователей к проблеме метаболических процессов. В распоряжении биологии оказались методы, позволившие перейти к количественным исследованиям процессов, протекающих как в целом организме и его органах, так и в тканях и отдельных клетках. В 20-х годах XX века на первом плане были проблемы энергетики живого организма и превращения веществ в процессе их обмена.
Английский биохимик Артур Хэрден (1865 — 1940) был первооткрывателем процессов метаболизма. Он изучал ферменты дрожжевой вытяжки и в 1905 г. отметил, что эта вытяжка разлагала сахар и быстро вырабатывала двуокись углерода — однако со временем скорость процесса замедлялась. Ученый предположил, что содержание ферментов падает, однако опыт показал, что это не так. При добавлении простого неорганического вещества — фосфата натрия — ферменты начинали свою работу вновь. По мере работы ферментов содержание фосфата натрия падало. Хэрден выяснял, не образуется ли при этом какой-либо органический фосфат. Он обнаружил фосфат в виде молекулы сахара, к которой присоединились две фосфатных группы. Это положило начало химии промежуточных продуктов метаболизма.
В течение долгого времени считали, что брожение и дыхание представляют собой совершенно независимые процессы. Однако уже Э. Пфлюгер во второй половине XIX в. высказывал предположение о тесной взаимосвязи этих процессов. Окончательно представления о единстве брожения и дыхания были разработаны С.П. Костычевым (1910), согласно взглядам, которого взаимосвязь между ними могла быть представлена следующей схемой:

Работы Костычева (1907, 1911) показали, что начальные фазы аэробного дыхания должны быть сопряжены с конечными фазами анаэробного распада углеводов.
Немецкий биохимик Отто Фритц Мейергоф (1884 — 1951) показал, что при мускульном сокращении исчезает гликоген (крахмал), а в соответствующих количествах появляется молочная кислота. Энергия реакции появлялась без участия кислорода. Когда же мышца отдыхала, некоторое количество молочной кислоты окислялось. Энергия, развивающаяся таким образом, позволяла большой части молочной кислоты реконвертироваться в гликоген. Английский физиолог Арчибалд Вивиен Хилл (1886—1977) пришел к тому же заключению путем измерения количества тела, выделяемого сокращающейся мышцей.
Детали превращения гликогена в молочную кислоту были разработаны в 1930-х годах американскими биохимиками Карлом Фердинандом Кори (1896 – 1984) и Герти Терезой Kopи (1896 – 1957). Ученые выделили из мышечной ткани неизвестный компонент и показали, что это – первый продукт распада гликогена в мышцах. Они профильтровали каждый компонент на каждом этапе. Супругам Кори удалось не только расчленить процесс превращения гликогена в глюкозу па отдельные этапы, но и воспроизвести синтез гликогена из глюкозы in vitro. Глюкоза была последовательно превращена с помощью соответствующих ферментов в глюкозо-6-фосфат, глюкозо-1-фосфат и гликоген. Самым важным в этих исследованиях было выяснение роли АТФ (аденозинтрифосфорной кислоты) как донора фосфатных групп, а также открытие процесса восстановления АТФ и АДФ (аденозиндифосфата) на последней ступени (Нобелевская премия, 1947).
Итак, в XX в. было выяснено, что фосфатная группа играет важную роль в биохимии. Американский биохимик Фриц Альберт Липман (1899 — 1986) показал, что фосфатная группа встречается в молекулах в одном-двух типах размещения: низкоэнергетическом и высокоэнергетическом. Когда молекулы крахмала либо жира разлагаются, высвобождаемая энергия используется для конвертации низкоэнергетических фосфатов в высокоэнергетические. Таким образом, энергия запасается в организме в удобной химической форме. Разложение одного высокоэнергетического фосфата освобождает столько энергии, чтобы привнести различные энергопотребляющие химические изменения в организме (рис.4.1.21).

Рис. 4.1.21. Цикл молекулы АТФ в клетке, предложенный Липманом.
Этапы в разложении гликогена, требующие присутствия кислорода, стало возможно изучить при помощи новой методики, разработанной немецким биохимиком Отто Генрихом Варбургом (1883-1970). В 1923 г. он изобрел метод изготовления тонких срезов тканей (живых, абсорбирующих кислород) и сумел измерить расход ими кислорода. В малой колбе с тонкостенной U-образной трубкой он наливал на дно трубки окрашенный раствор. Углекислый газ, выработанный тканью, абсорбировался спиртовым раствором в колбе. Кислород не замещался углекислым газом, и поэтому в колбе образовывался частичный вакуум и окрашенная жидкость в трубке поднималась в колбу. По изменению уровня окрашенной жидкости, тщательно измеренному, можно было подсчитать расход кислорода.
Влияние различных компонентов по расходу ими кислорода оценивалось как участие в промежуточных продуктах метаболизма. После того как было выяснено, что фосфорные эфиры являются промежуточными продуктами распада углеводов, английский биохимик Ханс Адольф Кребс (рис.4.1.22) предложил в 1937 г. схему довольно сложного цикла превращений органических кислот, объясняющую все основные моменты их постепенного окисления и образования АТФ на узловых этапах этого процесса (Нобелевская премия, 1953).

Рис. 4.1.22. Ханс Адольф Кребс (1900—1981)
Таким образом, этот цикл, получивший название цикла трикарбоновых кислот (или цикла Кребса), связал процессы поэтапного окисления органических веществ и постепенного выделения энергии в организме. Наиболее важным в цикле Кребса был этап, связывающий процессы аэробного и анаэробного распада углеводов — декарбоксилирование пировиноградной кислоты и перенос ацетильной группы на щавелево-уксусную кислоту, являющуюся конечным продуктом окисления первого компонента цикла — лимонной кислоты (рис.4.1.23). Разработанный Кребсом цикл в дальнейшем был уточнен и подвергся гораздо большей детализации, но его основные звенья сохранили свое значение. Кребс также установил этапы образования мочи из аминокислот.
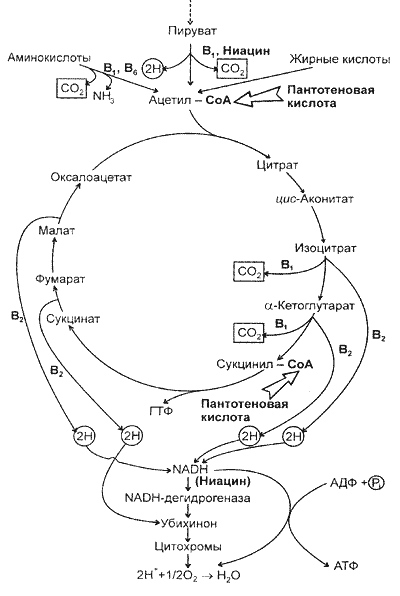
Рис. 4.1.23. Схема цикла Кребса и дыхательной цепи
На период 30—40-х годов приходится формирование основных представлений о дыхательной цепи (рис.4.1.23). После открытия Д. Кейлиным цитохромов (1925) возникла реальная возможность построения единой схемы включения кислорода в окислительные процессы. Эта схема предусматривала как активирование водорода, идею которого отстаивали еще В. И. Палладии и Г. Виланд, так и активирование кислорода, после работ А. Н. Баха развиваемое О. Варбургом. Изучение ферментов дыхательной цепи и введение понятия о переносе электронов и окислительно-восстановительном потенциале закончилось в 40-х годах построением схемы дыхательной цепи, лежащей в основе современных представлений.
В передаче водорода (электрона) от молекулы дыхательного субстрата к кислороду воздуха и в активации обоих элементов основную роль играют отдельные ферменты и ферментативные системы. В изучении дегидрогеназ и оксидаз получено много новых данных. Например, использование тяжелого изотопа кислорода 18О позволило X. Хайами и его сотрудникам в 50-х годах подтвердить опытным путем достоверность гипотезы А. Н. Баха о возможности в процессе дыхания прямого присоединения кислорода к дыхательному субстрату. При этом было доказано и существование оксидаз, активирующих молекулярный кислород и делающих его способным реагировать с органическими соединениями. Хайами назвал их фенольными оксидазами, а Г. Мезон предложил эту группу ферментов называть трансферазами кислорода.
Не менее успешно шла в последние годы также разработка проблемы энергетики дыхания. В 50-х годах были получены данные, позволившие разработать основы современных представлений по данному вопросу, согласно которым процесс окисления или восстановления можно трактовать как отнятие от дыхательного субстрата и присоединение к нему электрона.
Наравне с этими знаниями по метаболизму клетки накапливались знания о тонкой структуре клетки. Были разработаны новые методики исследований. В 1930-х годах был сконструирован первый электронный микроскоп. Он давал несравнимо большую разрешающую способность, чем самые мощные обычные микроскопы.
Американский ученый Владимир Зворыкин (1888 — 1982) приспособил электронный микроскоп к исследованиям цитологии. Можно было рассматривать частицы размером с большую молекулу; в протоплазме клетки был найден комплекс малых, но высокоорганизованных структур, названных органеллами. В 1940-х годах были разработаны методики выделения органелл разного размера. Среди крупных — митохондрии. Типичная клетка печени содержит около тысячи митохондрий, каждая около пятитысячной миллиметра длиной. Их детально исследовал американский биохимик Дэвид Эзра Грин. Он выяснил, что именно в них идут реакции цикла Кребса. Итак, крошечные митохондрии и есть «электрические станции клетки».
