- •5. Задание студентам :
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •1. Тема занятия: Линейные и циклические сопряженные системы. Ароматичность.
- •3. Задачи занятия:
- •5. Задание студентам:
- •5.1.Отчитаться за выполненные домашние задания;
- •6.4. Получить задания бумажного тестового контроля, ответить на тесты, ответы сдать
- •8. Литература для подготовки:.
- •Тюкавкина н.А., Бауков ю.И. Биоорганическая химия: Учебник.-2-е. -м., Медицина, 1991.- 528с. Стр.29 – 49.
- •Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •3. Задачи занятия:
- •5. Задание студентам:
- •5.2 Прослушать объяснения преподавателя, выполнить упражнения
- •Работа № 1. Сравнение основных свойств аммиака и мочевины. Образование нитрата мочевины.
- •К раствору, мочевины добавляют 2 капли конц. Нnо3, встряхивают содержимое. Немедленно образуется белый кристаллический осадок труднорастворимой азотнокислой мочевины.
- •Работа № 2. Сравнение кислотных свойств спиртов и фенолов.
- •8. Литература для подготовки.
- •3.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •3. Задачи занятия :
- •5. Задание студентам:
- •8. Литература для подготовки. Основная:
- •3.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •3. Задачи занятия :
- •5 . Задание студентам :
- •6. Методические указания к выполнению самостоятельной работы на занятии,
- •8. Литература для подготовки. Основная:
- •3.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •Работа № 1. Окисление первичных спиртов раствором перманганата калия.
- •Работа № 2. Окисление альдегидов гидроксидом меди (п).
- •8. Литература для подготовки.
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •2.2. Изучить важнейшие биохимические превращения карбоновых кислот.
- •3. Задачи занятия
- •5. Задание студентам
- •8. Литература для подготовки
- •2 .Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •8. Литература для подготовки
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •5. Задание студентам
- •8. Литература для подготовки
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •5. Задание студентам
- •8. Литература для подготовки
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •3. Задачи занятия :
- •4. Продолжительность занятия : 2 акад. Часа.
- •5. Задание студентам:
- •6. Методические указания к выполнению самостоятельной работы на занятии.
- •8. Литература для подготовки. Основная:
- •3.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •5. Задание студентам
- •Работа № 2. Восстановительные (редуцирующие) свойства моносахаридов - альдоз (окисление глюкозы гидроксидом меди (II) в присутствии щелочи)
- •8. Литература для подготовки
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •5. Задание студентам
- •8. Литература для подготовки
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •5. 5. Задание студентам
- •8. Литература для подготовки
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •5. 5. Задание студентам
- •8. Литература для подготовки
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
- •Биоорганическая химия
- •1 Курс. 1 семестр
- •3. Задачи занятия :
- •4. Продолжительность занятия : 2 акад. Часа.
- •5. Задание студентам:
- •6. Методические указания к выполнению самостоятельной работы на занятии.
- •8. Литература для подготовки. Основная:
- •2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
- •9. Обсуждено на заседании кафедры 29. 08. 2008 г.
8. Литература для подготовки
Основная
1.Тюкавкина Н.А. Биоорганическая химия: учебник для вузов / Н.А. Тюкавкина, Ю.И. Бауков.- 4-е изд., стереотип. - М.: «Дрофа», 2005- 542 с. С. 314 -344
2.Л.А.Каминская, И.В.Гаврилов Биоорганическая химия: Учебное пособие для самостоятельной работы студентов 1 курса очного обучения: Специальности 060101-лечебное дело, 060103- педиатрия, 060104-медико-профилактическое дело, 060105-стоматология.-Екатеринбург: Изд-во»практика», 2008.-136с С. 33- 36, 61 -63, 103 – 105
Дополнительная:
. 1. Тюкавкина. Н..А. «Биоорганическая химия» М. Медицина. 1991г. с
2.Реутов о.А., Курц а.Л., Бутин к.П. Органическая химия – м.: мгу, 1999 – с.535.
3. «Руководство к лабораторным занятиям по биоорганической химии» под ред. Тюкавкиной Н.А. – М.: Медицина, 1985..
9. Обсуждено на заседании кафедры 29. 08. 2008 г.
10. Учебное задание подготовлено. доц.. Каминской Л.А, Переваловым С.Г.
ГОУ ВПО УГМА РОСЗДРАВА
кафедра биохимии
Утверждаю
Зав. каф. проф., д.м.н.
Мещанинов В.Н.
_____‘’_____________2008 г
Биоорганическая химия
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
ДЛЯ СТУДЕНТОВ
К ПРАКТИЧЕСКОМУ ЗАНЯТИЮ № 10
Факультет: лечебно-профилактический, медико-профилактический, педиатрический
1 Курс. 1 семестр
1. ТЕМА ЗАНЯТИЯ . Пептиды и белки. Строение и биологическая роль.
2. УЧЕБНАЯ ЦЕЛЬ ЗАНЯТИЯ
Сформировать знания о строении, уровнях организации белковых молекул, физико-химических свойствах, связи между строением, составом и биологическими функциями.
3. ЗАДАЧИ ЗАНЯТИЯ:
3.1.Определить понятия «пептиды, белки» классификацию.
3.2.Изучить уровни организации белковых молекул, особенности связей, стабилизирующих виды структур.
3.3. Изучить в процессе лабораторно-практического исследования физико-химические свойства белков, качественные реакции на белки. Оценить важность проводимых реакций для постановки клинического диагноза.
4. ПРОДОЛЖИТЕЛЬНОСТЬ ЗАНЯТИЯ 2 акад. часа.
5. Задание студентам
5.1.Отчитаться за выполненные домашние задания;
5.2 Прослушать объяснения преподавателя, выполнить упражнения
5.3. .Провести контроль усвоения знаний( тестовый контроль по теме занятия)
5.4. Выполнить лабораторные практические работы:
а .Образование биурета из мочевины. Качественная реакция обнаружения биурета
б. денатурация белка
в. УИРС Обнаружение белка в составе биологических жидкостей.
6. МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ САМОСТОЯТЕЛЬНОЙ РАБОТЫ НА ЗАНЯТИИ
6.1.Составить конспект лабораторного исследования
6.2. Подготовить реактивы и лабораторную посуду
6.3. Провести лабораторное исследование, записать выводы.
6.4. Получить задания бумажного тестового контроля, ответить на тесты, ответы сдать
преподавателю.
Работа № 1. Образование биурета из мочевины. Качественная реакция обнаружения биурета
Растворы и материалы
Мочевина кристаллическая;
Раствор гидроксида натрия NaOH, 2н;
Раствор сульфата меди (II) CuSO4, 0,2 н;
Лакмусовая бумажка красная.
Ход работы
1. В сухую пробирку помещают на кончике микролопатки кристаллы мочевины и осторожно нагревают над пламенем спиртовки. (Мочевина вначале плавится, выделяются пузырьки газа - аммиака, затем масса затвердевает. Аммиак обнаруживают по посинению влажной красной лакмусовой бумажки, поднесенной к отверстию пробирки.
2. Пробирку охлаждают, добавляют 5 капель дистиллированной воды, кипятят содержимое пробирки. Раствор над осадком переливают в другую пробирку. К нему добавляют 2 капли раствора гидроксида натрия и 3 капли раствора сульфата меди. Появляется розово-фиолетовое окрашивание за счет образования комплексной медной соли биурета (название вещества указывает на присутствие двух остатков мочевины).
Химизм процесса
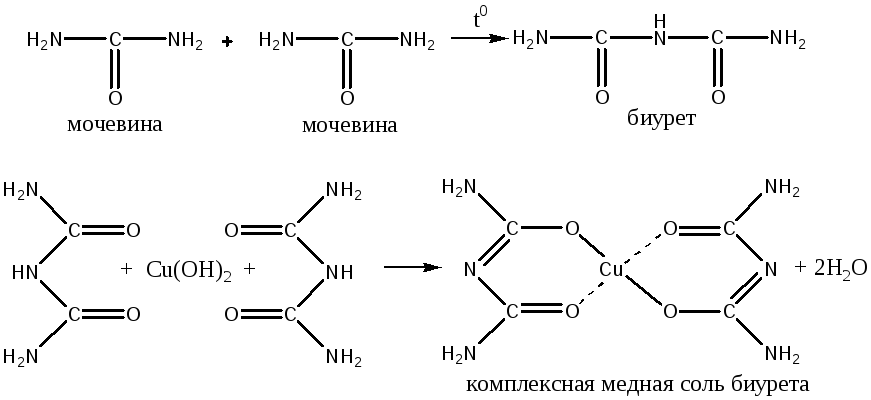
Остаток биурета в хелатном комплексе имеет имидное (лактимное) строение.
Медико-биологическое значение работы: Вышеприведенная цветная реакция носит название биуретовой. Она является одной из качественных реакций на белки и пептиды. Растворы мочевины используют в медицинских целях. Их необходимо проверять по вышеописанной методике (пункт 2) на присутствие следов биурета, который может образоваться при длительном хранении препарата, поскольку биурет вызывает гемолиз (разрушение) эритроцитов.
Работа № 2. Денатурация белка (влияние температуры, электролитов, ионов тяжелых металлов)
Реактивы и материалы
Белок сырого куриного яйца;
Раствор хлорида натрия NaCl насыщенный;
Раствор сульфата меди (П), 0,2н;
Раствор кислоты трихлоруксусной CCl3COOH, 1M;
Ход работы
В четыре пробирки помещают по 1 мл белка сырого яйца, затем в первую пробирку добавляют 1 мл раствора трихлоруксусной кислоты, во вторую – 1 мл раствора хлорида натрия, в третью – 1 мл раствора сульфата меди. Содержимое каждой пробирки перемешивают встряхиванием. Содержимое четвертой пробирки нагревают в течение 1-2 минут до кипения на пламени спиртовки. Опишите наблюдаемые изменения.
Медико-биологическое значение работы
Работа демонстрирует важнейшее свойство белков – способность к денатурации - потере своих нативных, природных (natura- природа-лат.) свойств при действии множества разнообразных факторов и чувствительность высших иерархических структур белков, а следовательно, и их свойств даже к небольшим изменениям в окружающей их среде. Особенно это касается катализаторов белковой природы – ферментов, могущих оптимально функционировать лишь в физиологических условиях при адекватном уровне поддержания гомеостаза и в узком интервале температур.
Работа № 3. УИРС. Обнаружение белка в составе биологических жидкостей
Ход работы
В пробирку отберите образец биологической жидкости (плазма крови, слюна, моча). Затем проведите две цветные реакции на белки, описанные ниже. Запишите наблюдаемые изменения. Сделайте вывод о наличии или отсутствии белка в данной биологической жидкости.
Цветные реакции на белки.
Реактивы и материалы:
Белки, водные растворы или биологические жидкости;
Гидроксид натрия, раствор 2н;
Раствор сульфата меди (П), 0,2н;
Раствор азотной кислоты HNO3, 2н.
1. Биуретовая реакция.
Ход работы
В пробирку помещают 5 капель исследуемого раствора белка, 3 капли раствора щелочи, 2 капли раствора сульфата меди. Жидкость окрашивается в розово-фиолетовый цвет.
|
Химизм процесса Биуретовая реакция связана с присутствием в белке пептидных групп |
|
|
и возникновением таутомерных форм, которые участвуют в комплексообразовании с ионом Сu2+. (См. предыдущую работу) |
|
2. Ксантопротеиновая реакция.
Ход работы
В пробирку помещают 5 капель водного раствора белка и 3 капли азотной кислоты. Появляется белый осадок. При нагревании реакционной смеси в пламени спиртовки раствор окрашивается в желтый цвет. Смесь охлаждают и добавляют 1-2 капли раствора щелочи. Желтое окрашивание переходит в оранжевое.
Химизм процесса
Азотная кислота вызывает денатурацию белка (белый осадок) и нитрование бензольных колец тирозина, фенилаланина и остатков других ароматических аминокислот (желтое окрашивание). При последующем подщелачивании среды образуются более интенсивно окрашенные анионы:
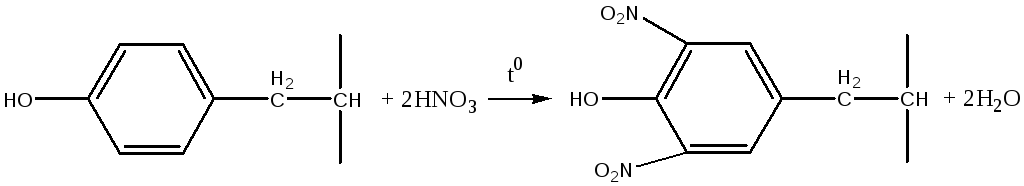
Медико-биологическое значение работы
Позволяет обнаружить присутствие белка в любых биологических жидкостях, в медицинской лабораторной диагностике проводить количественные измерения. Интенсивность окраски раствора в биуретовой реакции пропорциональна содержанию белка в растворе. Видоизмененная ксантопротеиновая реакция используется для качественного определения белка в моче при заболеваниях почек.
. 7. КОНТРОЛЬНЫЕ ВОПРОСЫ ПО ТЕМЕ ЗАНЯТИЯ смотрите задание для студентов к практическому занятию.