
- •Ароматические кислоты и их соли производные салициловой кислоты
- •Химические свойства
- •Кислота бензойная Натрия бензоат
- •Получение
- •Описанне
- •Растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Салициловая кислота и ее производные
- •Кислота салициловая Натрия салицилат
- •Получение
- •Описанне
- •Растворимость
- •Подлинность
- •6. Реакции электрофильного замещения (на фенольный гидроксил).
- •Чистота
- •Количественное определение
- •1.Методы кuслотно-основного титрования.
- •Хранение
- •Чистота
- •Количественное определение
- •Хранение
- •Примененне
- •Сложные эфиры салициловой кислоты
- •Получение
- •Описание
- •Растворимость
- •Подлинность
- •Чистота
- •Количественное определение
- •Хранение
- •Примененне
Ароматические кислоты и их соли производные салициловой кислоты
Ароматические кислоты - это производные ароматических углеводородов, у которых в бензольном ядре один или несколько атомов водорода заменены карбоксильными rpуппами «- СООН».
Простейшим представителем ароматических кислот является бензойная кислота. Введение различных функциональных групп в молекулу бензойной кислоты определяет разнообразие ароматических кислот - кислота салициловая (фенолокислота).
Введение карбоксильной группы в молекулу бензола и фенола привело к резкому снижению токсичности соединений (облагораживающее действие).
Кислоты применяются в медицине в качестве антисептических средств наружно. Применение внутрь ограничено раздражающим действием вследствие диссоциации кислот. Внутрь применяются натриевые соли бензойной и салициловой кислоты. Кислоты сами служат основой для синтеза ряда производных.


бензойная кислота салициловая кислота
Химические свойства
Кислотные свойства обусловлены наличием карбоксильной группы СООН

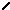 O
O
O
O


 R
– C H+
+ R – C
R
– C H+
+ R – C

 O
H
O-
O
H
O-
Ароматические кислоты – это более сильные кислоты, чем кислоты жирного ряда, что объясняется влиянием ароматического ядра (но бензойная слабее уксусной). Под влиянием заместителей в ядре кислотные свойства будут уменьшаться в ряду:
рКа = 3,00 рКа = 3,48 рКа = 4,18
Салициловая кислота Ацетилсалициловая кислота Бензойная кислота
Кдис = 1,06∙10-3 Кдис. = 6,3·10-5
Наличие сильной внутримолекулярной водородной связи между
-СООН и -ОН обусловливает более активные кислотные свойства и стабильность, образование мононатриевых солей только по карбоксильной группе кислоты салициловой.

За счёт кислотных свойств
кислоты образуются растворимые соли с гидроксидами, карбонатами и гидрокарбонатами (отличие от фенолов) щелочных металлов.
Натриевые соли в отличие от самих кислот легко растворимы в воде.
За счёт карбоксильной группы с ионами Сu2+, Со2+, Fe3+, Ag+ образуют окрашенные, трудно растворимые соли.
Минеральные кислоты как более сильные вытесняют ароматические кислоты из их солей
Ароматические кислоты образуют производные:
2.1. Сложные эфиры – со спиртами (с метанолом – метилсалицилат с резким запахом) и фенолами. Салициловая кислота может образовывать эфиры и по фенольному гидроксилу.
2.2. Амиды– с аминами, ангидриды – с уксусным ангидридом, галогенангидриды – с хлорангидридом (подобно карбоновым кислотам).
Реакции электрофильного замещения имеют значение только для фенолокислот:
Группа – СООН является электроакцепторным заместителем, т.е. стягивает электронную плотность с ядра и дезактивирует его.

Поэтому реакция электрофильного замещения замедляется и затрудняется; в анализе бензойной кислоты не используется. Если имеются ориентанты 1 рода (-OH-, -NН2), то реакции электрофильного замещения проходят в мягких условиях и количественно (аминобензойная и гидроксибензойная кислоты).
3.1 галогенирование
3.2 конденсации (салициловая кислота)
