
- •Анализ лекарственных средств производных бензолсульфониламида
- •Сульфаниламиды
- •Получение
- •1.Общая схема синтеза.
- •Растворимость
- •Физико-химические свойства
- •Химические свойства
- •Подлинность
- •1. Температура плавления.
- •Общие реакции подлинности
- •Специфические реакции подлинности
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Подлинность
- •Количественное определение
- •Описание
Анализ лекарственных средств производных бензолсульфониламида
к производным бензолсульфониламидов относится большая группа ЛВ, обладающих антибактериальной, диуретической, гипогликемической, антисептической и другими видами фармакологического действия.
Бензолсульфониламиды - это производные амидов сульфокислот ароматического ряда.
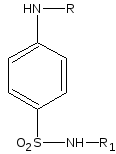


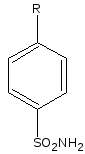


сульфокислота амид сульфокислоты
-сульфанил -сульфонил
(названия радикалов)
в
зависимости от химической структуры и
характера биологического действия
бензолсульфониламиды подразделяются
на 4 группы производных: 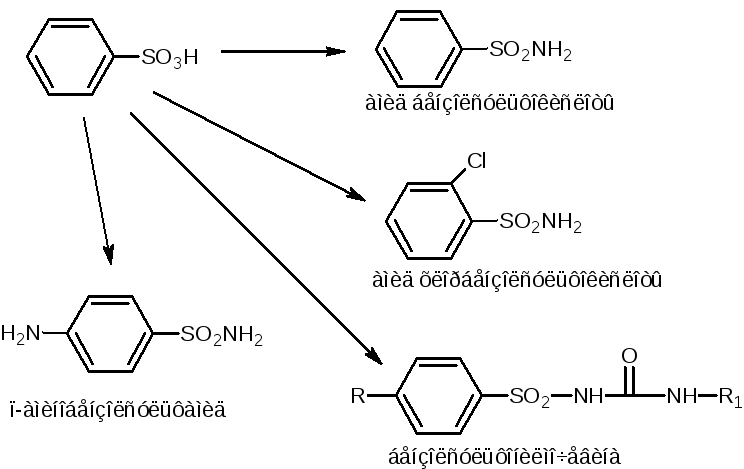
Сульфаниламиды
 сульфаниловая
кислота
сульфаниловая
кислота
Сама сульфаниловая кислота не применяется в медицине, но ее амид уже является ЛВ и служит основой целой группы ЛП, объединенных по химическому строению и характеру фармакологического действия в большую группу сульфаниламидных препаратов.
История создания в 1908 г. французский химик Гельмо в поисках лучших красителей для ткани синтезировал амид сульфаниловой кислоты, ставший основой для синтеза целого ряда азокрасителей для красильной промышленности. В 1932 г немецкий ученый Герхард Домагк получил один из таких азокрасителей – сульфамидохризоидин – пронтозил, и установил его высокую терапевтическую активность при тяжелых стрептококковых инфекциях. Мыши, получившие 10 смертельных доз гемолитического стрептококка, после введения пронтозила, остались живы, а все контрольные погибли.
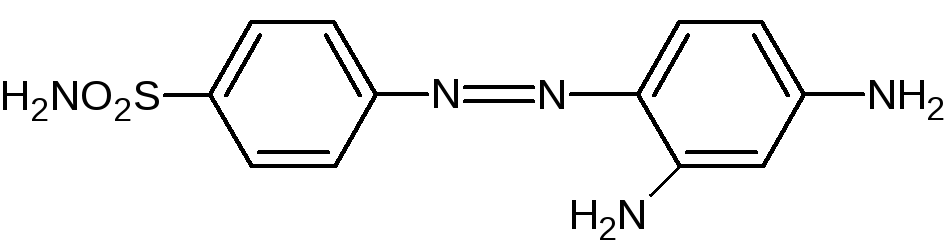 пронтозил
пронтозил
В 1935 г. в печати появилось первое сообщение Домагка о проведенных испытаниях и их результатах. Это послужило началом нового этапа в развитии химиотерапии и широких исследований в области создания химиотерапевтических средств, производных амида сульфаниловой кислоты. Уже в 1935 г. сотрудниками института Пастера было установлено, что самые различные азокрасители, содержащие сульфаниламидный фрагмент пронтозила, обладают почти одинаковой противострептококковой активностью in vivo. Однако, любые модификации сульфаниламидной части молекулы (замещение сульфамидной части молекулы на карбоксамидную или нитрильную) приводило к потере антибактериальной активности.
В нашей стране первые работы в области синтеза и изучения терапевтических свойств с/а проводились во ВНИХФИ под руководством химика-органика О.Ю. Магидсона в 1935-36 гг. Первым был синтезирован близкий по структуре к пронтозилу красный стрептоцид:
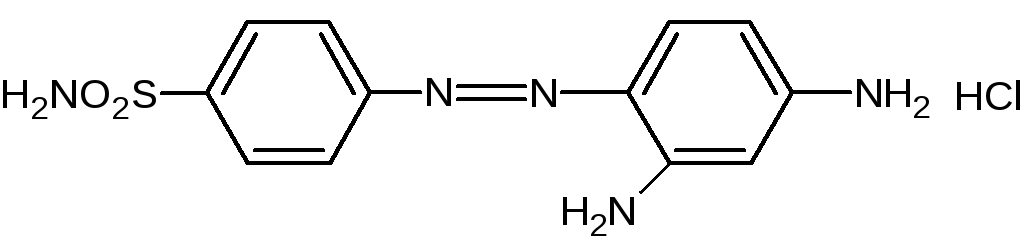
Вслед за первым важным открытием о том, что антибактериальная активность пронтозила и красного стрептоцида обусловлена сульфамидной частью молекулы последовало второе: в организме животного происходит метаболическое расщепление азогруппы с образованием следующих веществ:

I – высокоактивный в терапевтическом отношении с/а
II – 1,2,4 – триаминобензол – физиологически не активный, токсичный продукт.
Этот вывод заставил отказаться от соединений типа пронтозила (азокраситель) и начала формироваться группа ЛС на основе п-аминобензолсульфамида. Уже в 1936 г.в нашей стране начал выпускаться белый стрептоцид:
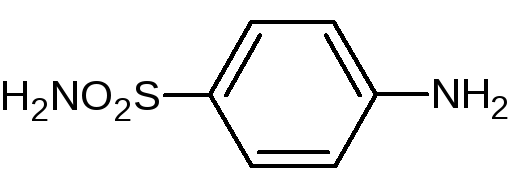
Механизм антимикробного действия с/а основан на теории конкурентного антогонизма. Для нормальной жизнедеятельности и роста микроорганизмам необходимы факторы роста – фолиевая, дигидрофолиевая кислота и другие вещества, в состав которых входит п-аминобензойная кислота: ФОЛИЕВАЯ КИСЛОТА
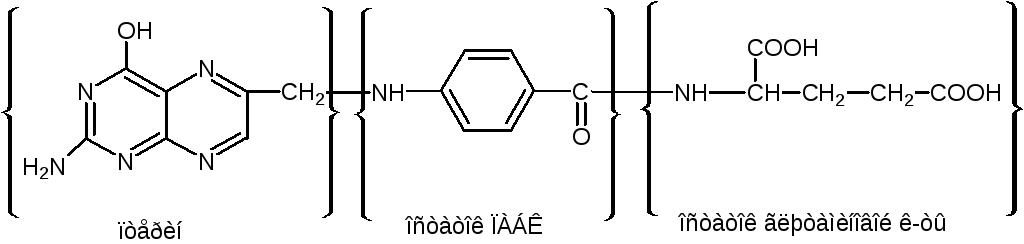
П-аминобензолсульфамид имеет близкое структурное сходство с ПАБК:

При наличии в бактериальной среде с/амидов они конкурируют с ПАБК на стадии образования птероевой кислоты и связываются с птеридиновым фрагментом, образовавшееся соединение, лишенное ПАБК, не может далее усваиваться микробной клеткой и рост микроорганизмов тормозится:

На этом основан механизм бактериостатического действия сульфаниламидов. Для того, чтобы «выиграть» в конкурентной борьбе за место в молекуле фолиевой кислоты, с/а должны применяться в больших (ударных) дозах, что является одним из недостатков препаратов данной группы. Кроме того, при назначении препаратов необходимо помнить, что ЛС, производные ПАБК – новокаин, анестезин, являются антагонистами с/а. Назначать их вместе нельзя.
ОБЩАЯ ФОРМУЛА
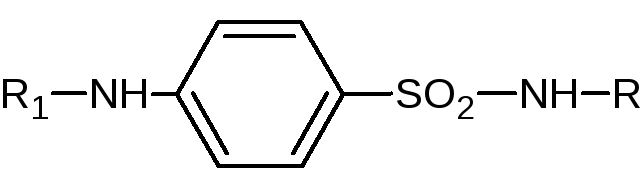
Создание группы препаратов проводилось на основе изучения взаимосвязи изменений в химической структуре с характером физиологического действия. При этом были выявлены следующие основные закономерности:
первое и основное условие – наличие сульфанильного радикала в молекуле
какие-либо манипуляции с аминогруппой в п-положении (перемещение в о- или м-положение; замещение водородных атомов радикалами, при которых в организме не может снова образовываться свободная ароматическая аминогруппа) приводят к полной потере активности.
введение заместителя в ароматическое кольцо приводит либо к снижению, либо к полной потере физиологической активности
лишь введение радикалов в сульфамидную группу позволяет получать вещества, физиологическая активность которых, в зависимости от радикала, может меняться не только в сторону уменьшения, но и в сторону увеличения
отмечено особое влияние метокси-группы на продолжительность действия препарата. Почти все препараты пролонгированного действия содержат эту группу в составе радикала сульфамидной группы
Группа ЛС, с/амидов, в своем формировании прошла несколько этапов.
В первое десятилетие с момента открытия (1935-1944 гг) интерес к данным препаратам был очень велик, велись интенсивные работы по их синтезу как в нашей стране, так и за рубежом. В это время группу формировали:
Сульфаниламид (стрептоцид) Sulfanilamide(МНН) Streptocidum(ЛН)
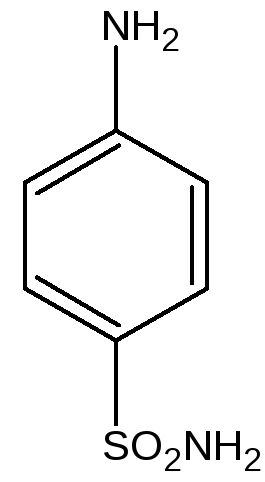 n-Аминобензолсульфамидмикроорганизмам
нтного антогонизма. Для нормальной
жизнедеятельностиС на основео стрептоцида
обусловлена сульфамидной ч
n-Аминобензолсульфамидмикроорганизмам
нтного антогонизма. Для нормальной
жизнедеятельностиС на основео стрептоцида
обусловлена сульфамидной ч
Сульфацетамид натрий ( сульфацил-натрий)
Sulfacetamide sodium(МНН) Sullfacylum-natrium(ЛН)
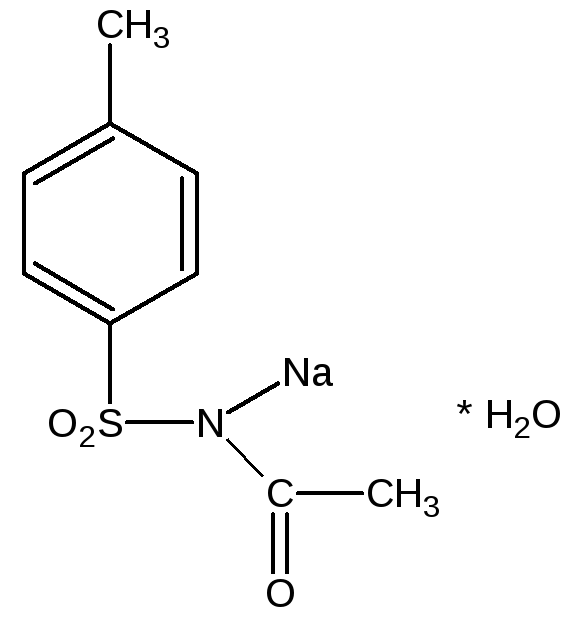 п-Аминобензолсульфонил-
ацетамид- натрий
п-Аминобензолсульфонил-
ацетамид- натрий
Сульфатиазол (норсульфазол) Sulfathiazole (МНН) Norsulfazolum(ЛН)
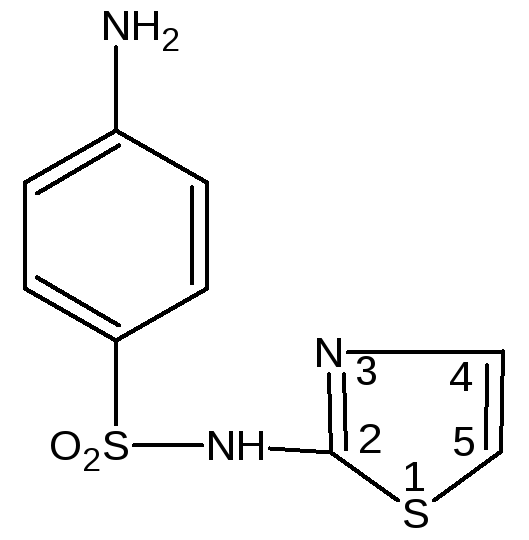 4-амино-
N-(2-тиазолил)- бензолсульфонамид
4-амино-
N-(2-тиазолил)- бензолсульфонамид
Фталилсульфатиазол (фталазол)
Phthalylsulfathiazole(МНН) Phthalazolum (ЛН)
 2-(
п-Фталиламинобензол- сульфамидо )-тиазол
2-(
п-Фталиламинобензол- сульфамидо )-тиазол
В 1944-45 гг. в связи с появлением антибиотиков (пенициллин, стрептомицин) интерес к с/а был потерян. Во многом это было связано с тем, что они быстро выводятся из организма, в связи с этим возникала необходимость приема больших доз через небольшие промежутки времени. Синтез препаратов группы с/а, обладающих длительным, пролонгированным действием, снова привлек интерес практической медицины и этим препаратам. Это следующие препараты:
Сульфадиметоксин Sdimethoxine(МНН) Sulfadimethoxinum (ЛН)
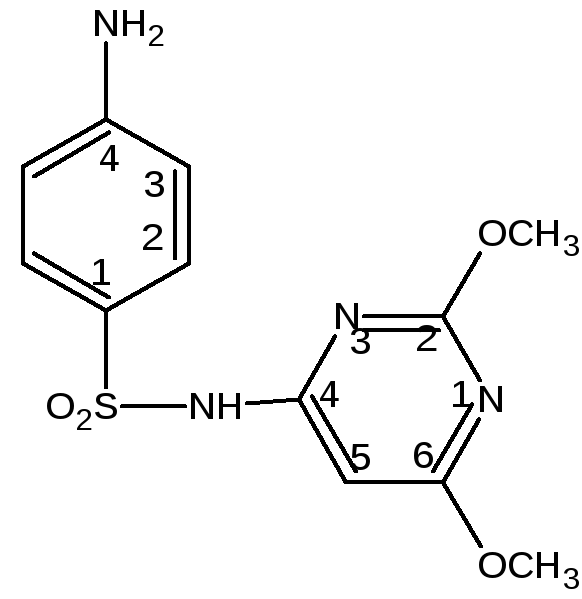
4-Амино-N-(2,6- диметокси-4- пиримидинил)- бензолсульфонамид
Сульфален Sulfalene(МНН) Sulfalenum(ЛН)

4-Амино-N-(З- метоксипиразинил )-бензолсульфонамид
В последующем исследователи вновь вернулись к азосоединениям на основе сульфаниловой кислоты. Были созданы препараты группы салазосульфаниламидов. Особенностью их действия является выраженный лечебный эффект у больных неспецифическим язвенным колитом. Накапливаясь в соединительной ткани кишечника, они постепенно распадаются по азогруппе, образуя продукты, оказывающие одновременно антибактериальное и противовоспалительное действие.
Салазопиридазин Salazopyridazinum (ЛН)
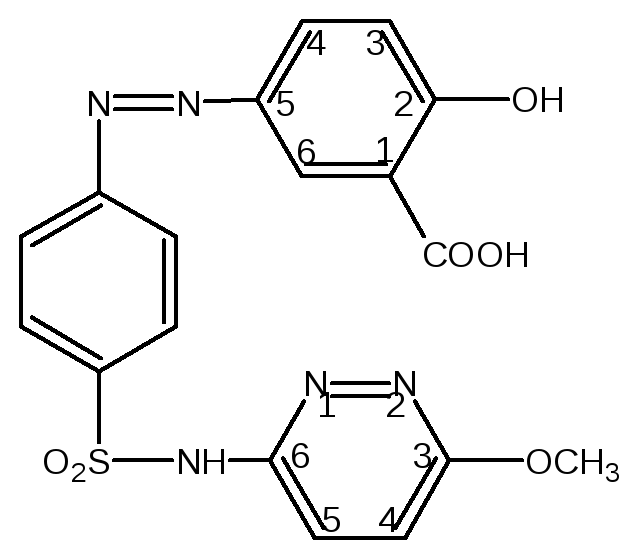
5-(п-[N-(З- метоксипиридазинил -6)- сульфамидо]-фенилазо)-салициловая кислота
В 70х годах прошлого века разработан высокоэффективный
Комбинированный препарат Сульфаметоксазол + Триметоприм
Sulfamethoxasolum + Trimetoprimum (ЛН)
синонимы – Бактрим Bactrim, Бисептол Biseptol,
«Ко-тримоксазол» Со- Trimoxazole (МНН)
 +
+
сульфаметоксазол триметоприм
4-амино-N –(-5-метил-3-изоксазалил)- бензолсульфонамид
Сочетание этих двух веществ с бактериостатическим действием обеспечивает бактерицидное действие. Количество переходит в качество.
