- •Анализ лекарственных средств производных бензолсульфониламида
- •Сульфаниламиды
- •Получение
- •1.Общая схема синтеза.
- •Растворимость
- •Физико-химические свойства
- •Химические свойства
- •Подлинность
- •1. Температура плавления.
- •Общие реакции подлинности
- •Специфические реакции подлинности
- •Чистота
- •Количественное определение
- •Хранение
- •Применение
- •Подлинность
- •Количественное определение
- •Описание
Получение
1.Общая схема синтеза.
Исходные продукты синтеза – ацетанилид и хлорсульфоновая кислота
получение хлорангидрида сульфаниловой кислоты – общая для всех с/а стадия.
получение соответствующего аминопроизводного – отличается в зависимости от характера радикала в сульфамидной группе
омыление ацетамидной группы для освобождения аминогруппы. Проводится в щелочной среде
Гидролиз,
t = 250C
HOH
- CH3OH,
-
Na2CO3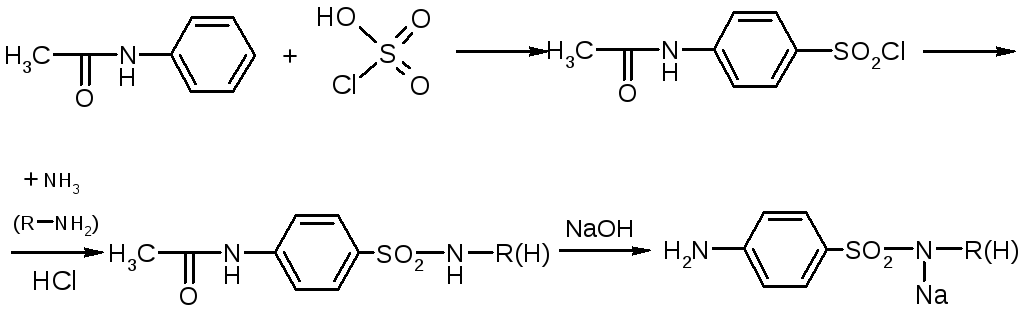
HCl
- NaCl

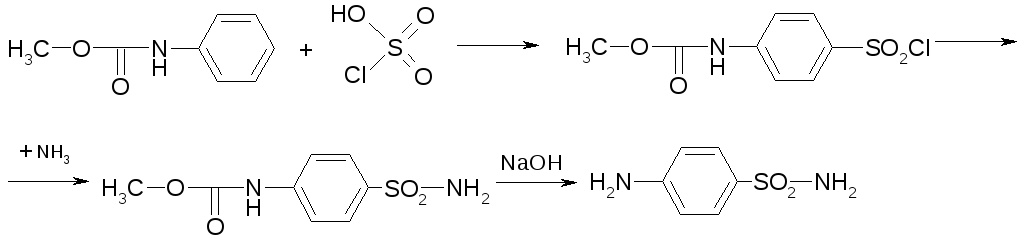
2. Синтез из N-фенилметилуретана (не касается салазопиридазина и бессептола): синтез с/амидов в промышленности наиболее рациональным |способом может осуществляться на основе одного из фенилуретанов – N-карбометоксианилина. Например, стрептоцид:
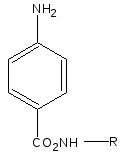
На стадии амидирования используют различные амины. Структура аминов представлена в таблице.
|
Лекарственные вещества |
R-NН2 |
Название амина |
|
Сульфаниламид СvлыЬацетамид-натрий |
NНз |
Аммиак |
|
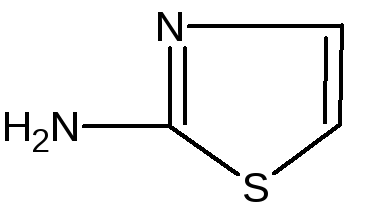
Сульфатиазол, фталилсульфатиазол |
|
2-Аминотиазол |
|
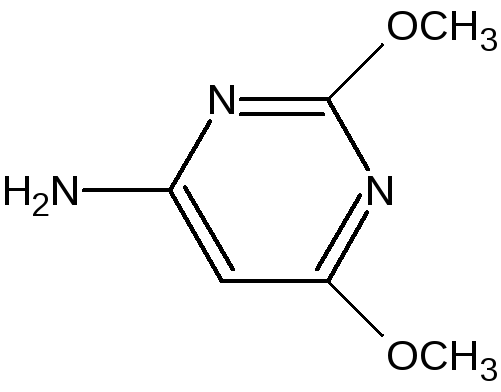
Сульфадиметоксин |
|
4-Амино-2,6- диметоксипиримидин |
|
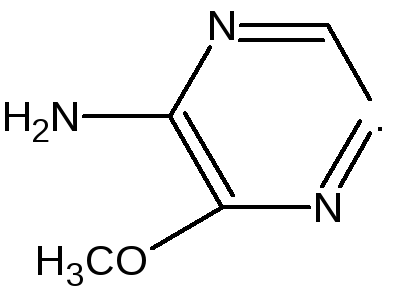
Сульфален |
|
2-метокси-3-амино- пиразин |
|
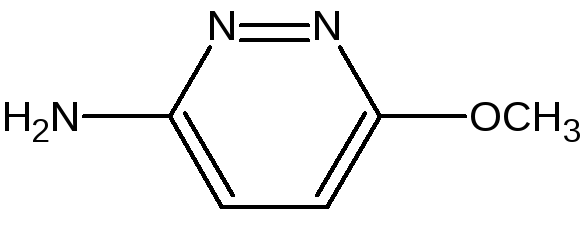
Салазопиридазин |
|
3-метокси-6- аминопиридазин |
Например, при получении сульфацетамида-натрия на стадии амидирования используют аммиак:


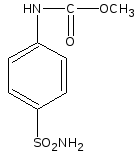
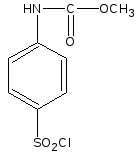
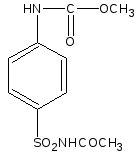
Амидирование
NH3
- HCl
Ацилирование
(CH3CO)2O
- CH3COOH


Хлорангидрид
N-карбометоксисульфаниловой
кислоты
Амид N-карбометокси-
сульфаниловой
кислоты
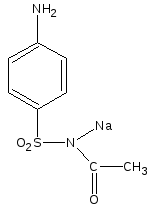
Гидролиз,
t =
250C
HOH, 3NaOH
- CH3OH
- Na2CO3

Описание Белые или с желтоватые кристаллические порошки без запаха. Салазопиридазин имеет, красно-оранжевое окрашивание, т.к. по химическому строению является азокрасителем.
Растворимость
ЛВ все кроме сульфацила натрия мало растворимы в воде, растворимы в полярных растворителях (например, в ацетоне), мало растворимы или практически нерастворимы в липофильных растворителях (хлороформе и эфире). Натриевые соли сульфаниламидов растворимы в воде и не растворимы в органических растворителях.
Физико-химические свойства
l. поглощение света в УФ-области спектра (250-320 нм), что обусловлено наличием хромофорных групп, главным образом, ароматического кольца.
2.Поглощает свет в видимой области салазопиридазин за счет наличия азо-группы.
3. в ИК-области все ЛВ имеют характерные спектры поглощения.
Химические свойства
кислотно-основные свойства. Кислотные формы сульфаниламидов обладают амфотерными свойствами с преобладанием кислотных.
И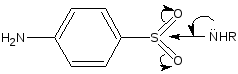 з-за
отрицательного индуктивного эффектаSO2-группы
бензолсульфониламиды обладают
NH-кислотностью.
Ацилирование
сульфамидной
группы приводит к образованию имидов
с
более выраженной NH-кислотностью
по сравнению с амидами.
Такие бензолсульфониламиды растворяются
не только в щелочах как амиды, но и в
карбонатах щелочных металлов.
з-за
отрицательного индуктивного эффектаSO2-группы
бензолсульфониламиды обладают
NH-кислотностью.
Ацилирование
сульфамидной
группы приводит к образованию имидов
с
более выраженной NH-кислотностью
по сравнению с амидами.
Такие бензолсульфониламиды растворяются
не только в щелочах как амиды, но и в
карбонатах щелочных металлов.
Натриевые соли с/амидов хорошо растворимы в воде, их растворы имеют щелочную реакцию среды.
- Кислотные свойства с/амидов обусловлены наличием замещенной (кроме стрептоцида) имидной группы (в составе сульфамидной) и выражены сильнее. За счет NH-кислотных свойств ЛВ образуют соли со щелочами и карбонатами щелочных металлов, а натриевые соли с солями тяжелых мeтaллов.
Стрептоцид как очень слабая кислота не ацилированная по сульфамидной группе натриевых солей и комплекса не образует.
- Слабые основные свойства обусловлены наличием ароматической аминогруппы и выражаются в способности растворяться в кислотах с образованием солей. Однако с/а – это слабые основания, поэтому их соли неустойчивы и в водной среде легко гидролизуются.
+3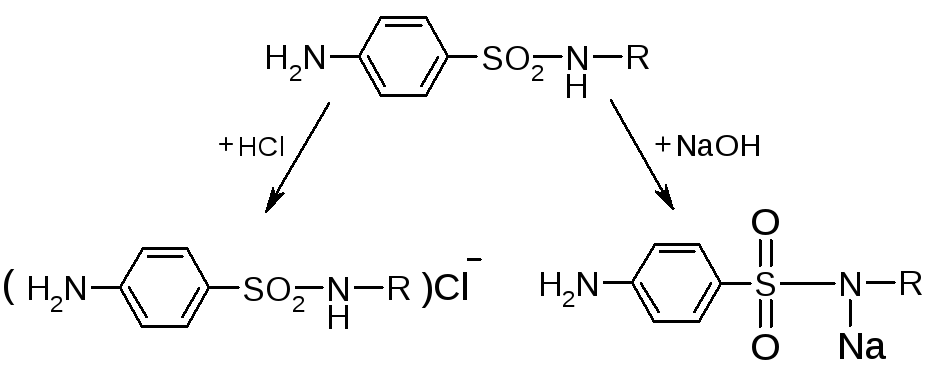
или
NaOH
HCl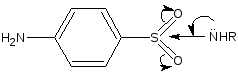
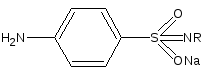


+ H2O
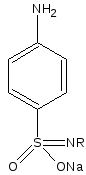
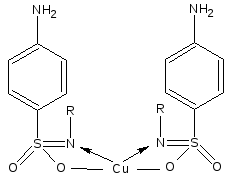
CuSO4
- Na2SO4
Сульфаниламиды дают реакции, характерные для ароматических соединений (реакция электрофильного замещения), первичной ароматической аминогруппы (реакция образования азокрасителя, конденсации с альдегидами, окисления и др.)